英文名称 :amniotic cavity infection
妊娠期由于胎膜早破(premature rupture of membrane,PROM)、细菌性阴道病(bacterial vaginosis,BV)等使病原微生物进入羊膜腔引起羊水、胎膜(羊膜、绒毛膜和蜕膜)及胎盘感染称为羊膜腔感染(intraamniotic infection,IAI)。在所有妊娠中,羊膜腔感染发病率为5%~12%,而在特殊情况下,特定高危人群中发病率则高达20%。羊膜腔感染可引起新生儿感染,导致早产、死胎、脑瘫和产褥期感染,是围产儿致病率、死亡率和产妇致病率、死亡率升高的重要原因。
1.病原体
健康育龄妇女阴道内存在各种细菌及其他微生物,常见有革兰氏阳性需氧菌、乳杆菌,如非溶血性链球菌、肠球菌及表皮葡萄状球菌,革兰氏阴性需氧菌,如大肠埃希氏菌、阴道加德纳菌,还有大量厌氧菌,如消化球菌、消化链球菌、拟杆菌等。此外,支原体、衣原体及假丝酵母菌也常存在。上述各种菌中以乳杆菌占优势。由于阴道上皮在雌激素作用下合成糖原经乳杆菌分解成乳酸形成弱酸环境,可有效地抑制其他寄生菌的过度生长。妊娠期母体受高水平雌激素的影响,使阴道上皮内糖原合成增加,加上孕期母体免疫功能下降,均有利于假丝酵母的生长。阴道内乳杆菌相对不足,在一定条件下,使正常菌群成分有所改变,而有致病可能。
引起羊膜腔感染的病原微生物很复杂。Fan等(2020c)回顾性分析580例羊膜腔感染病例,经腹部羊膜腔穿刺或胎盘组织行病原微生物分离,发现解脲支原体占30.2%,链球菌占10.5%,大肠埃希氏菌占6.9%,人型支原体占6.4%,梭形杆菌占6.0%,假丝酵母菌占4.0%,乳杆菌占4.0%,阴道加德纳菌占3.6%,假单胞菌占3.1%(图1)。Romero等(2021)报道经腹部羊膜腔穿刺羊水或胎盘组织微生物分离证实,宫内感染病例微生物分离阳性率为70%,分离微生物按占比依次为解脲支原体、人型支原体、阴道加德纳菌、B族链球菌(group B streptococcus,GBS)、咽峡炎链球菌,其中65%病例为混合感染。图1为580例羊膜腔感染病例羊膜腔穿刺羊水或胎盘组织病原微生物组成。
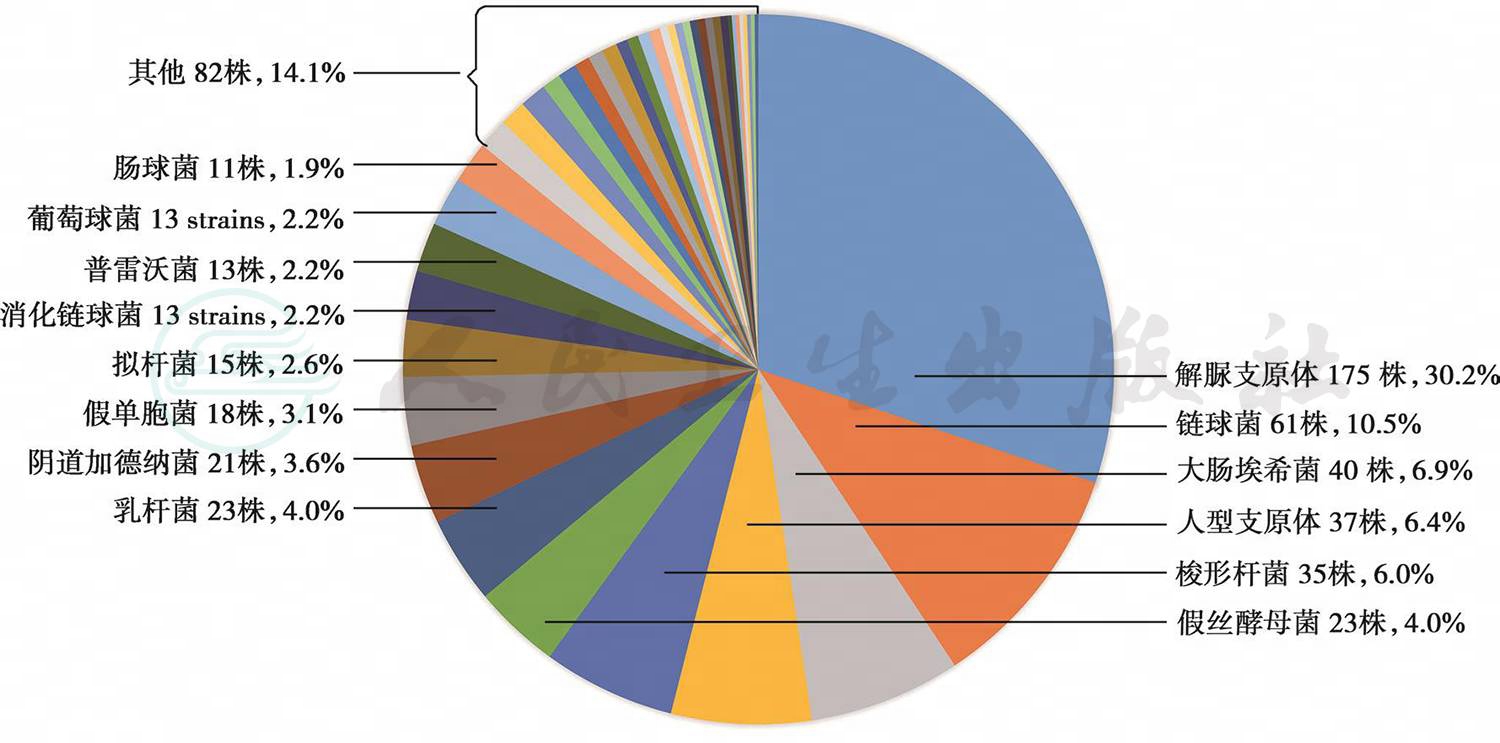
图1 580例羊膜腔感染病例羊膜腔穿刺羊水或胎盘组织病原微生物组成
孕妇和胎儿感染B族链球菌的临床表现是从无临床症状的定植到脓毒症。B族链球菌可引起不良妊娠后果,包括早产、胎膜早破、临床和亚临床绒毛膜羊膜炎以及胎儿和新生儿感染。B族链球菌也可致孕妇出现菌尿、肾盂肾炎、产后子宫炎、骨髓炎和产后乳腺炎。全球10%~30%女性阴道和下消化道携带B族链球菌,孕妇平均带菌率约18%,不同种族和地区孕妇带菌率差异大,带菌率为11%~35%,南亚和东亚孕妇带菌率较低,分别为12.5%和11%。细菌可由下消化道发展至生殖道,少数至尿道,但很少在宫颈部发现。由于肛门直肠部位的一些细菌寄生是经常的,而在阴道则是偶然的,因此,任何研究分析B族链球菌携带者时均应进行肛门、直肠和阴道的培养。有不少孕妇早中期培养阴性,到孕足月时培养为阳性。B族链球菌是西方国家胎儿新生儿羊膜腔感染、生后感染的重要病因,也是孕产妇尿道生殖道感染的主要原因,其病情的严重程度远远超过常见的大肠埃希氏菌,因而临床上已引起广泛的重视。
A族链球菌即化脓性链球菌,是引起孕妇感染的重要原因之一。A族链球菌是引起急性咽炎最常见的病原菌,并与许多全身和皮肤感染相关。化脓性链球菌可产生大量毒素和酶,引起局部和全身毒性反应。产致热外毒素菌株通常会引起严重感染,引起羊膜腔感染、子宫肌炎、腹膜炎等。
2.临床上导致感染的有关因素
(1)胎膜早破
胎膜完整对防御感染十分重要,胎膜早破使阴道条件发生了改变,由弱酸改变为弱碱性,有利于细菌的繁殖。破膜后阴道内致病原可沿生殖道上升进入宫腔及母血液循环,导致母婴感染。感染是胎膜早破的重要发病因素,存在于宫颈和阴道穹窿的某些微生物能够产生膜蛋白水解酶,水解胎膜的细胞外物质而使其抗张强度下降。感染还可使胎膜附近的过氧化酶激活,加速膜蛋白分解,白细胞弹性蛋白酶释放使羊膜中胶原纤维Ⅳ受损使胎膜脆性增高,局部感染还可导致前列腺素的产生与释放,从而引起宫缩,促使胎膜破裂的发生,因此,胎膜早破和羊膜腔感染之间互为因果,关系密切。
(2)细菌性阴道病
妊娠期细菌性阴道病的发生率波动于3.5%~50.0%。妊娠状态与BV存在相互影响,一方面,妊娠期雌、孕激素水平变化,阴道局部黏膜免疫功能变化,宫颈黏液及阴道分泌物增多,可能增加了BV的易感性;另一方面,BV可导致上生殖道感染,与不良妊娠结局及产褥期感染有关。因此,对于妊娠合并BV的管理应充分权衡患者筛查、治疗的获益与潜在的风险。
(3)医源性因素
产科医生一些操作包括内监护持续时间、破膜时间、阴道检查次数和产程长短可能与IAI的发生相关,某些阴道、宫腔操作可增加IAI的危险性。
(4)宿主抵抗力下降
阴道内的乳杆菌可降低毒性强的细菌的数量,如大肠埃希氏菌、A和B族链球菌、厌氧菌、淋病奈瑟菌和沙眼衣原体等;宿主分泌免疫球蛋白和有关酶类对细菌有很强的杀灭作用;阴道黏膜下CD4和CD8淋巴系统对下生殖道病原菌有识别和应答作用;胎膜、羊水、胎盘对病原菌入侵胎儿和羊膜腔起重要的屏障作用。在另一方面,病原微生物的产物如唾液酶,磷脂酶A、C和内毒素可激活宿主细胞酶系统,降低宿主局部免疫反应,利于更多的病原微生物生存,给羊膜腔感染的发生提供了可能性。
1.实验室检查
羊水直接检查可提供重要诊断资料。羊水标本培养是诊断羊膜腔感染的最好方法。结合胎盘胎膜组织学检查确诊绒毛膜羊膜炎或绒毛膜羊膜培养出致病菌是诊断羊膜腔感染的可靠依据。但病理检查和组织培养只能在产后进行,对临床处理已为时过晚。而羊水培养结果也至少需48~72小时,临床使用价值也受限。
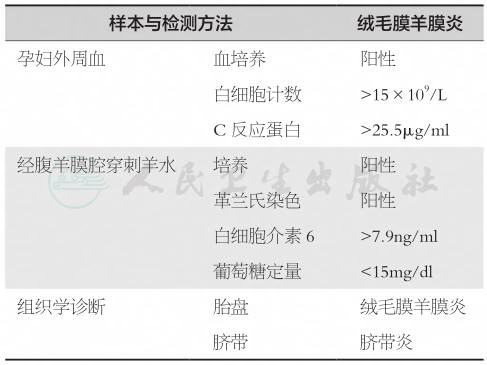
其他羊水标本快速检测方法包括羊水标本革兰氏染色、羊水葡萄糖定量和白细胞计数。有条件的实验室还可进行羊水白细胞酯酶测定、乳酸盐、异常有机酸水平和胎儿纤维蛋白原测定等对诊断羊膜腔感染均有一定的价值,但有的需时较长,有的需特殊制剂和设备。孕妇外周血白细胞计数和C反应蛋白水平测定诊断羊膜腔感染敏感性及特异性不强。联合孕妇外周血及羊水生物学标志如细胞因子(白细胞介素1、2、6、8,肿瘤坏死因子等)、羊水基质金属蛋白酶-8等可提高绒毛膜羊膜炎组织学诊断的准确性。表1总结了绒毛膜羊膜炎的实验室诊断检测方法。
表1 绒毛膜羊膜炎实验室诊断检测方法
2.胎盘病理
标准化胎盘大体检查和组织学取样对于发现胎盘异常很重要,病理切片需至少4~5张同时包括脐带、胎膜和3个部分胎盘实质的切片。胎盘、胎膜或脐带血管中发现感染或炎症的组织学证据可明确诊断。急性绒毛膜羊膜炎的母体和胎儿炎症反应分为3期2级(图3)。母体炎症反应分期:1期(早期),急性绒毛膜板下炎/绒毛膜炎;2期(非特指),急性绒毛膜羊膜炎;3期(长期),坏死性绒毛膜羊膜炎。母体炎症反应分级:1级,轻度、中度炎性改变;2级,>10~20个中性粒细胞浸润或合并绒毛膜板下微脓肿。胎儿炎症反应分期:1期,绒毛膜板血管炎或脐静脉炎;2期,累及脐静脉和1条或2条脐动脉;3期,伴有坏死性脐带炎/环脐血管周围炎。胎儿炎症反应分级:1级,轻度、中度炎性改变;2级,重度炎性改变伴有血管平滑肌坏死。慢性绒毛膜羊膜炎组织学分为2期2级:1期,淋巴细胞局限于绒毛膜滋养细胞层;2期,位于绒毛膜羊膜层;1级呈斑片状分布,2级呈弥漫分布。分期体现了炎性改变持续的时间,分级体现了炎性改变的严重程度。图3羊膜腔感染组织学改变。
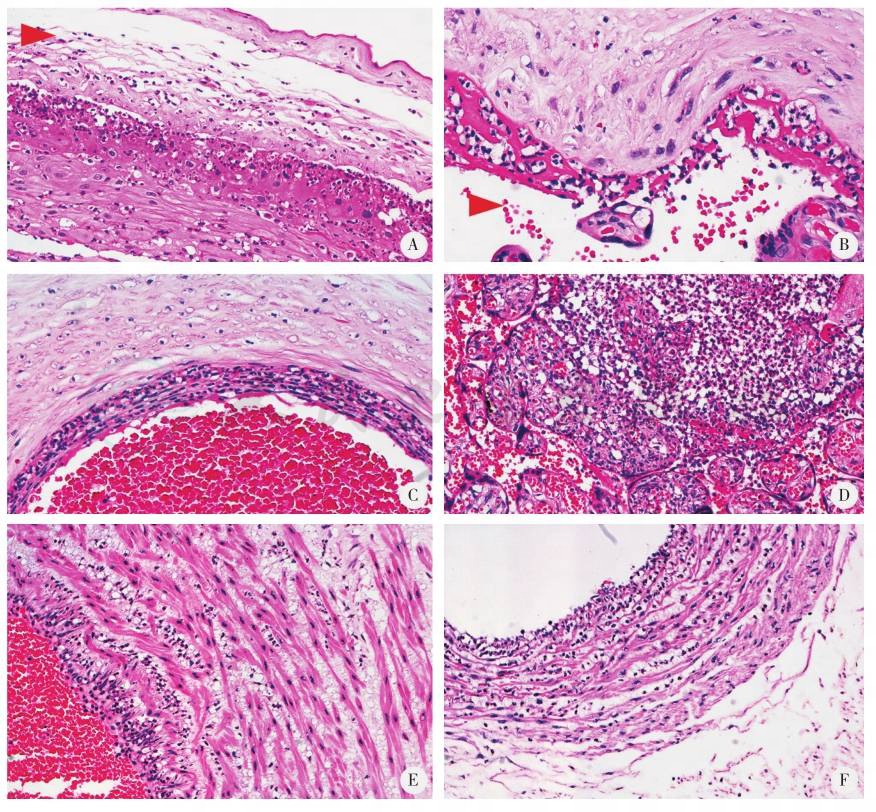
图3 羊膜腔感染组织学改变
A.母体炎症反应2期急性绒毛膜羊膜炎,中性粒细胞浸润羊膜结缔组织;B.母体炎症反应1期急性绒毛膜板下炎,中性粒细胞浸润绒毛膜板;C.胎儿炎症反应1期绒毛膜血管炎;D.急性绒毛膜板下炎/绒毛膜板下脓肿,李斯特菌感染性流产患者胎盘中见中性粒细胞浸润绒毛膜板下纤维层和绒毛间隙;E.胎儿炎症反应1期脐静脉炎胎儿中性粒细胞向脐静脉迁移浸润;F.胎儿炎症反应2期脐动脉炎。苏木精-伊红(HE)染色,放大倍数200倍。
1.抗生素
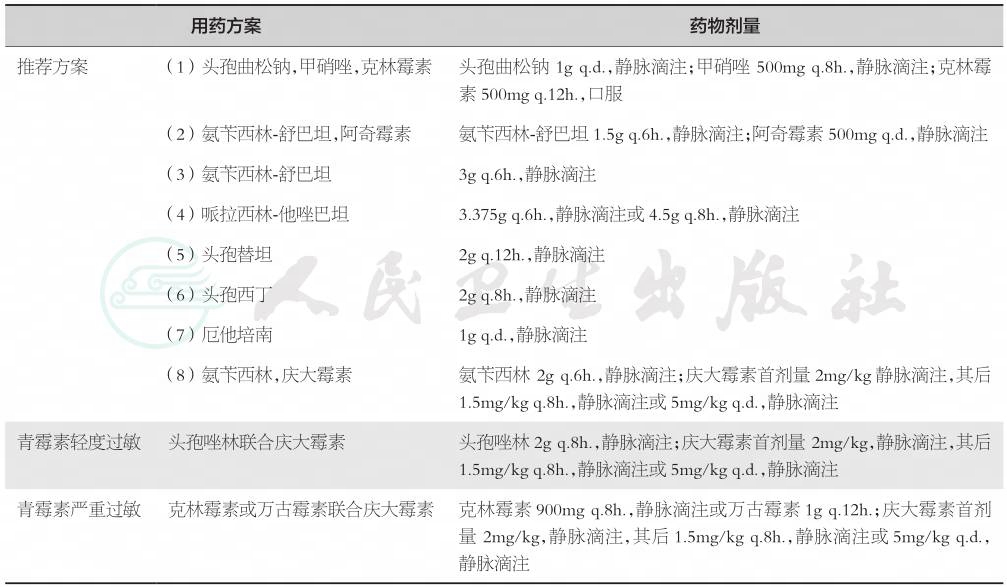
羊膜腔感染一经确诊,广谱抗生素十分必要。过去主张分娩后使用抗生素可不影响新生儿血培养结果。近几年研究证明,一旦诊断立即使用可将产妇的感染率降到最低程度。羊膜腔感染的治疗目的是降低胎/婴儿致病率和死亡率,首先需要给胎儿提供有效的抗生素,药物治疗方案见表2。
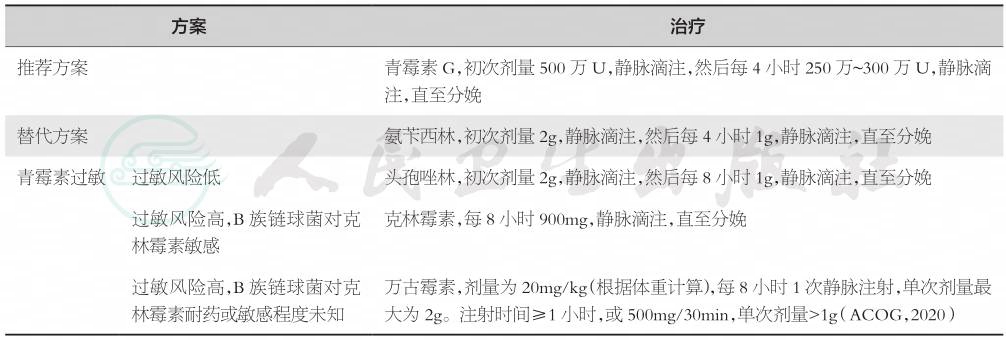
表2 羊膜腔感染治疗方案
2.终止妊娠时机
羊膜腔感染一经确诊,无论孕周大小应尽快结束妊娠。感染时间越长,产褥病率越高,对新生儿的危险性更取决于胎儿在感染环境内时间的长短,时间越长新生儿感染和死胎的可能性越大,因此羊膜腔感染人群中剖宫产率明显升高。近几年的资料证明产时静脉给予广谱抗生素可在数分钟内进入胎儿、胎膜和羊水并达到足够的抗菌浓度。但胎儿接受足够抗生素后3~5小时内尚不足以改变新生儿的预后,因此处理的关键在于及早给予足够的抗生素后行剖宫产术。临产后,产程中应连续作胎心监护。如有变异减速或晚期减速,可能预示胎儿酸中毒;胎儿心动过速除外其他原因,持续加速可能是胎儿脓毒症或肺炎的一个表现,因此应尽快结束分娩并作好新生儿复苏的准备。
3.终止妊娠方式
已诊断羊膜腔感染者,如不具备阴道分娩条件,则应以剖宫产终止妊娠。腹膜外剖宫产并不可降低产后感染及其他合并症。如术中发现感染严重,影响子宫收缩,严重出血不止,必要时须切除子宫。
4.新生儿治疗
新生儿一出生立即行咽、耳鼻、脐血等细菌培养及药敏试验。体外药敏试验表明,B族链球菌对青霉素、氨苄西林、头孢霉素、红霉素、林可霉素均敏感。不等培养结果,羊膜腔感染患者的新生儿通常联合应用青霉素和氨苄西林作为初选药物,当培养明确和症状明显时再决定其药物种类、用量和疗程。免疫疗法目前尚处于临床试验阶段,可输注少量新鲜血浆增强抗感染能力。
由于多数羊膜腔感染呈亚临床表现,不易作出早期诊断,因此没有特别有效的预防策略。当羊水或胎盘胎膜细菌培养阳性,胎盘病理检查有绒毛膜、羊膜炎症以及出现明显的感染征象时常常危及胎儿和新生儿的生命或出现严重的合并症,因此无论根据高危因素还是筛查结果,应识别哪些妇女需要预防措施。高危对象有早产、胎膜早破、胎膜早破≥18小时,既往有B族链球菌史或有发热。筛查对象为36~37周+6 B族链球菌培养(+)。
1.先兆早产、早产
早产的原因很多,羊膜腔感染是导致部分早产的原因已得到共识。泌尿生殖道炎症或病原体携带,特别是携带B族链球菌常易发生早产,且对宫缩松弛剂不敏感。对合并感染者应用抗生素可能对延长孕周及控制感染有效。尚未推荐对胎膜完整的先兆早产、早产患者常规应用抗生素。
2.胎膜早破
胎膜早破和羊膜腔感染的因果关系密切,当发生胎膜早破时,羊膜腔感染通常不明显,但需经全面检查、严密观察感染的征象。临床处理根据不同孕周作出决定,破膜时间越长,绒毛膜羊膜炎的风险越大,如胎膜早破发生在34周以后,则等待12小时不临产即行引产,否则潜伏期越长危险性越大,其间避免不必要的阴道检查和肛诊。孕周<24周,根据我国国情,胎儿生存率很低,期待疗法时间过长难以保证安全,因此征得孕妇同意,可积极引产。孕周24~28周间,符合保胎条件同时孕妇及家人要求保胎者,可期待保胎治疗,但保胎过程长风险大,需充分告知期待保胎过程中的风险。孕28~34周间,新生儿存活率随孕周增加而上升,尤其在32周以后,因此提倡期待疗法,尽量延长孕龄,同时促胎肺成熟,此期间应严密观察和管理,并使用预防性抗生素,虽然对此问题尚有争议,但目前我国仍对胎膜早破达12小时以上者常规使用抗生素。如观察期间感染征象出现,宜立即终止妊娠。
3.细菌性阴道病
尽管细菌性阴道病与包括胎膜早破、早产、羊膜腔感染和产后子宫内膜炎在内的不良妊娠结局有关,妊娠期治疗细菌性阴道病唯一确定的益处是缓解阴道感染症状和体征。潜在的益处包括降低妊娠期细菌性阴道病相关感染合并症和减少其他性传播疾病的风险。全身治疗对可能的亚临床生殖器官感染有益。多项研究和荟萃分析没有发现妊娠期应用甲硝唑增加胎儿畸形或机体细胞突变风险。替硝唑为妊娠C类药物,不用于孕妇。妊娠期BV筛查及治疗原则是无需常规对无症状孕妇进行细菌性阴道病筛查和治疗。对有症状的孕妇以及无症状但既往有感染相关流产或早产病史等高风险的孕妇均需筛查,筛查阳性者需进行治疗。用药方案:可选择口服甲硝唑和克林霉素。妊娠期阴道局部用药可能存在胎膜早破等风险,建议口服用药。可参考的用药方案包括:①甲硝唑400mg,口服,2次/d,共7天;②克林霉素300mg,口服,2次/d,共7天。
4.B族链球菌携带者的产前、产时处理
以培养为基础,孕妇在孕36~37周+6行B族链球菌定植筛查,直肠和阴道B族链球菌培养阳性的孕妇在分娩期予抗菌剂治疗。婴儿既往患B族链球菌侵入性疾病和先前确定为B族链球菌菌尿的孕妇均应考虑药物预防。对于临产和B族链球菌培养结果未知的孕妇,根据感染危险因素选择预防。虽然青霉素被推荐为一线药物,但氨苄西林也是一种可接受的替代药物。对于青霉素过敏的妇女,如果过敏反应风险低,则推荐使用头孢唑林。如过敏反应风险高,则应在B族链球菌定植筛查的时候进行克林霉素的药敏试验,对克林霉素敏感者,选择克林霉素预防;若对克林霉素耐药者,需要选用万古霉素。治疗方案选择依赖于进行药敏试验的实验室能力。在具体医疗机构,在广泛应用抗生素预防的情况下,有必要认识潜在的抗生素耐药性恶化问题。孕妇中,氨苄西林的杀菌水平能成功在脐血中持续达30分钟。分娩期抗生素预防围产期B族链球菌疾病的方案见表3。
表3 分娩期抗生素预防围产期B族链球菌疾病的方案