英文名称 :preeclampsia
子痫前期是妊娠期特有的疾病,发病率波动于2%~8%。子痫前期是一种动态性疾病,病情可呈持续性进展,这就是子痫前期-子痫严重程度的延续性。既往将子痫前期分为“轻度”和“重度”,但ACOG、IHSSP等指南认为这种划分会错误引导产科医生对该疾病严重性的认知,“轻度”子痫前期只代表诊断时的状态,任何程度的子痫前期都可能导致严重不良后果,因此不再诊断“轻度”子痫前期而诊断为子痫前期,以免造成因诊断“轻度”而对病情忽视。根据是否伴有严重表现,ACOG将子痫前期分为伴有或不伴有严重表现的子痫前期(preeclampsia with severe features),为简化疾病诊断和便于病史书写,便于和国内疾病诊断编码保持一致,本文仍按照国内既往习惯将伴有严重表现的子痫前期命名为“重度子痫前期”。参考2020年ACOG指南诊断标准见表1。
表1重度子痫前期的诊断标准

1954年Pritchard首次描述了3例出现溶血、转氨酶升高及血小板减少的子痫患者,仅1例存活。后续不少学者对此类病例进行描述和报道。1982年Louis Weinstein首次命名并报道了HELLP综合征,是指在重度子痫前期-子痫基础上发生的以溶血(hemolysis,H)、转氨酶升高(elevated liver enzymes,EL)及血小板减少(low platelet count,LP)为特点的一种综合征。自HELLP综合征被命名以来,时至今日,其定义、诊断、发病率、病因及处理均存有很多争议。争议的焦点在于HELLP综合征是一种独立的疾病,还是重度子痫前期的一组严重表现,两种疾病之间的关系以及是否同属于一种疾病。
HELLP综合征临床症状多样,可表现为腹痛、恶心、呕吐和全身不适等,因此临床表现不具有一定的特异性。尽管用于临床诊断及文献研究中涉及的HELLP综合征的诊断标准迄今尚不统一,从HELLP综合征的最初命名描述来看,其诊断的建立主要是依据实验室检查指标,但不同实验室有不同的诊断标准,并没有完全统一和标准化,另外,转氨酶升高和血小板下降的程度也没有明确界定,诊断溶血的标准之一血清结合珠蛋白临床上亦未常规开展。总之,HELLP综合征有很多不同的诊断标准。Sibai等建议的HELLP诊断标准:①溶血,应该至少有以下两种表现:外周血涂片(破裂细胞、锯齿状细胞);血清总胆红素≥1.2mg/dl(20.52μmol/L);血清结合珠蛋白≤25mg/dl;非失血性严重贫血。②转氨酶升高:血清转氨酶(AST和ALT)大于正常值的2倍;③血小板计数低:<100×109/L。
2020年ACOG建议的诊断标准需要同时符合以下三点:①乳酸脱氢酶(lactate dehydrogenase,LDH)≥600U/L;②血清转氨酶(AST和ALT)升高大于正常值的2倍;③血小板计数<100×109/L。除此之外,也有学者建议根据血小板减少的严重程度对HELLP综合征进行亚分型(Mississippi分级)见表2。不过,ACOG更新的诊断标准还没有被推广使用,临床所采用的HELLP诊断仍以Sibai的建议最为常用。
表2HELLP综合征Mississippi分级

子痫前期病因及发病机制尚未完全阐明。PE被认为是多因素、多机制及多通路发展的复杂病理过程,无法以“一元论”来解释。2009年Redman提出著名的子痫前期“二阶段模式”学说,第一阶段为病理生理变化形成过程,即临床前期,以滋养血管重塑导致胎盘血流灌注减少,胎盘缺血、缺氧为特点,亦称为胎盘形成不良或胎盘浅着床;第二阶段是第一阶段导致的临床征象的发生。随着对PE发病机制的深入研究,Redman认为“二阶段模式”学说不能充分反映PE发病机制,继而在2014年提出“六阶段模式”,本质上仍是对“二阶段模式”学说更加细化的时间分段和内容补充,也不能反映所有PE患者的发病机制和诱发疾病模式。
目前还没有任何一种单一的因素能够解释子痫前期-子痫的病因和发病机制,而是综合了母体、胎儿、胎盘等多种因素的相互影响、相互作用。研究较重要的因素包括:滋养细胞浸润异常、母-胎间免疫平衡失调、氧化应激反应导致的母体对正常妊娠炎症改变的适应不良、遗传因素及营养因素等。
1.滋养细胞浸润异常
正常着床时,固定绒毛滋养细胞侵入妊娠子宫蜕膜,深度可达子宫基层的内1/ 3,充分重塑子宫螺旋动脉,破坏血管壁中层肌弹力纤维,使弹力纤维丧失,螺旋动脉进行性扩张,变成漏斗状,使阻力减少,血流量增加;同时,子宫的自然杀伤(natural killer,NK)细胞分泌一系列涉及血管生成的细胞因子,包括(vascular endothelial growth factor,VEGF)、胎盘生长因子(placental growth factor,PLGF)、血管生成素-2等。而子痫前期-子痫时滋养细胞侵入深度仅达螺旋动脉的蜕膜段,螺旋动脉重塑不良,少数血管甚至不发生血管重塑,造成胎盘灌注相对减少及缺氧环境,这一现象又称为胎盘浅着床。
2.氧化应激反应
多方面的证据显示,氧化应激反应是第一阶段胎盘浅着床引起的后续反应。目前的研究认为,氧化应激反应是子痫前期-子痫由基本病理生理变化阶段发展至器官损害阶段的重要联系纽带。缺氧胎盘的局部氧化反应转移到孕妇全身的体循环系统,导致全身血管内皮细胞产生自由基和脂质过氧化物等,这些物质进一步损伤血管内皮细胞的结构和功能,虽然在正常的妊娠中也存在脂质过氧化物增加,但可以通过同步增加的抗氧化作用抵消,氧化-抗氧化作用仍维持平衡;在子痫前期-子痫患者中,抗氧化作用相对减弱,氧化作用占优势,导致血管内皮细胞损伤。应用抗氧化剂(如维生素E、维生素C、β-胡萝卜素等)预防子痫前期-子痫的发生已展开相应研究。
3.免疫平衡失调
流行病学研究结果显示,孕前有输血、流产、被男方淋巴细胞免疫史,均可降低子痫前期-子痫发生的危险;而初孕者、人工授精后妊娠者及工具避孕后受孕者,则会增加子痫前期-子痫发生的发病率,故又将此病称为初父亲(primipaternity)疾病。妊娠是一种成功的半同种移植现象,其成功有赖于母-胎间免疫平衡。人类白细胞抗原(human leukocyte antigen,HLA)可以与NK细胞抑制受体结合,诱导免疫抑制反应,是母-胎界面免疫耐受的重要机制之一。正常妊娠妇女对胎儿组织的细胞免疫表现为低应答,使Th1/Th2细胞之间的免疫达到平衡,即Th1所介导的细胞免疫反应和Th2所介导的体液免疫反应的平衡,而子痫前期-子痫患者滋养细胞HLA-G表达下降或缺失,血液中的NK细胞、中性粒细胞、白细胞介素2(IL-2)、IL-6、IL-12及肿瘤坏死因子-α(TNF-α)等均增加,它们可以直接作为细胞毒性因子或介导细胞毒性因子的产生而导致血管内皮损伤,并增加Th1细胞的细胞免疫活动,打破Th1/ Th2细胞之间的平衡。
4.遗传因素
流行病学研究结果显示,子痫前期-子痫有遗传易感性,但其遗传模式尚不清楚,一般认为是多因素、多基因疾病。研究发现:若母亲为子痫前期患者,其女儿中20%~40%会患子痫前期-子痫;11%~37%的子痫前期患者是姐妹;在双胎中,患子痫前期的一致性为60%。母、胎双方遗传学方面的异常对子痫前期-子痫的发病均有影响。目前已经研究出部分基因(如MTHFR、LPL等)可能与子痫前期相关。对Fas受体、HIF-α(低氧诱导因子-α)、IL-1β(白细胞介素-1β)、TGF-β3(转化生长因子-β3)、ApoE(载脂蛋白E)和TNF-α的基因多态性也有研究。因子痫前期的遗传易感性,特别是其他基因和环境因素的相互作用引起复杂性表型表达,所以任何候选基因都可能引起子痫前期。多基因与子痫前期发病的相关性是今后子痫前期遗传学研究的一个方向。
5.营养因素
孕期补充锌、钙、镁,对预防子痫前期-子痫有一定作用。研究显示,进食丰富蔬菜和水果可以提高机体抗氧化功能,有助于降低血压,而缺乏维生素C可增加子痫前期-子痫发病的危险性。
综上所述,子痫前期-子痫可能的发病机制是,由于某些遗传因素导致母体对胎儿滋养细胞膜抗原的低识别,造成防护性的免疫减弱和排斥反应的增强,使滋养细胞功能受损和胎盘浅着床,从而引起胎盘缺血缺氧和代谢障碍,表现为胎盘源性细胞毒性因子增加,并进而造成血管内皮损伤,血管活性物质平衡失调,导致全身小动脉痉挛,最终发生子痫前期-子痫,如图1所示。
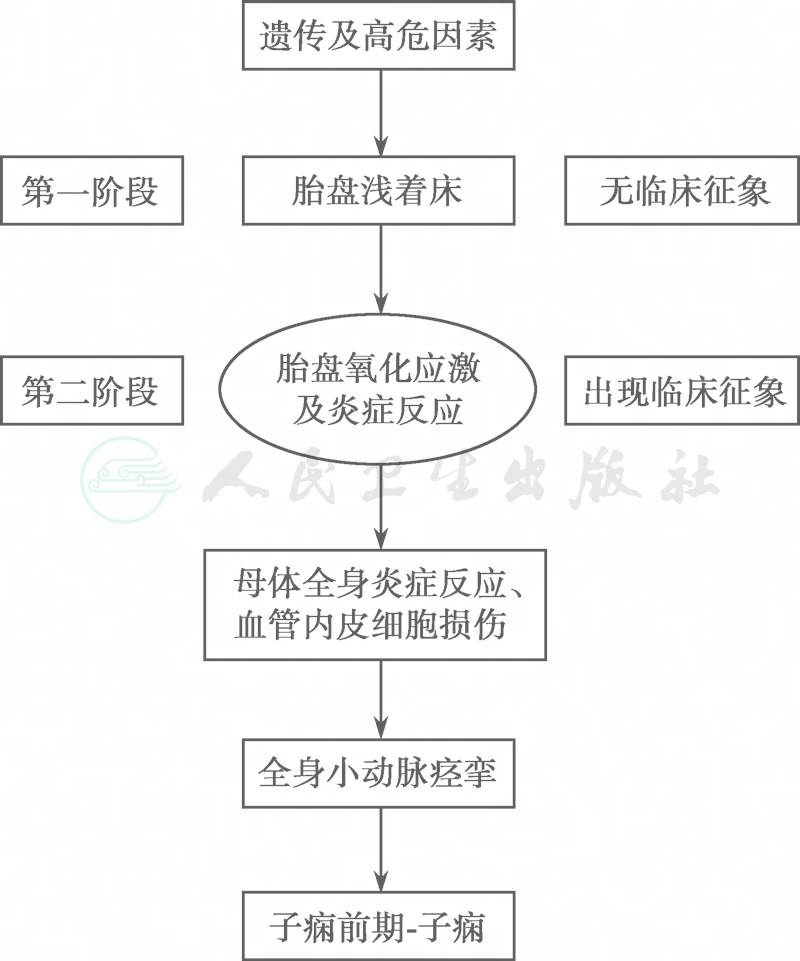
图1子痫前期二阶段发病机制
子痫前期-子痫的基本病理生理改变是全身小动脉痉挛,导致各系统靶器官血流灌注不足,造成组织细胞缺血缺氧,并呈现相应脏器功能损害的临床表现。
1.脑
脑部病理改变包括脑水肿、充血、局部缺血、血栓形成及出血等。子痫前期脑血管阻力和灌注压均增加,以保持正常脑部血运;子痫时,脑血流由于脑血管自我调节功能丧失,灌注压明显增加。临床表现为头痛、头晕、呕吐、烦躁不安、视物模糊、意识障碍甚至昏迷等。而子痫的发生与脑血管自身调节功能丧失相关。
2.肾脏
肾脏病理改变为肾小球毛细血管内皮增生,内皮细胞肿胀、增大,内皮下纤维素沉积。子痫前期肾脏血流灌注降低25%~30%,肾小球滤过率减少,肾小球基底膜受损,通透性增加,出现尿蛋白。患者可出现尿酸及肌酐水平升高,可表现少尿、无尿,甚至急性肾衰竭(主要是急性肾小管坏死引起的)。
3.肝脏
肝脏细胞缺血、缺氧、坏死,病情严重时,肝内小动脉痉挛后随即扩张松弛,血管内突然充血,使静脉窦内压力骤然升高,门静脉周围可能发生局限性出血,甚至肝被膜下血肿形成,自发性肝破裂。临床表现为上腹部不适,特别是右上腹不适,恶心、呕吐,肝区叩痛。肝功能异常时,肝转氨酶水平升高,血浆碱性磷酸酶升高。
4.血液
(1)凝血:
子痫前期-子痫患者全身小动脉痉挛,血管内皮损伤,引起血小板激活、聚集并且破坏和消耗增加,活化的血小板激活凝血因子Ⅻ,并释放多种血小板因子加速凝血过程。重度子痫前期患者由于胎盘缺血、缺氧及梗死,则可使大量破碎绒毛的滋养叶细胞进入母体循环被溶解而释放大量的凝血活酶,从而进一步导致凝血功能障碍,如凝血酶原时间(PT)、部分凝血活酶时间(APTT)、凝血酶时间(TT)可明显缩短,纤维蛋白原(Fg)明显增加;D-二聚体(D-D)、纤维蛋白降解产物(FDP)含量升高;抗凝血酶Ⅲ(ATⅢ)明显降低。
(2)血容量、渗透压:
子痫前期-子痫患者由于血管收缩、内皮细胞损伤、通透性增加等原因,导致水分丢失血液浓缩,实际有效循环血量减少,表现为血细胞比容增加,血液黏度增加等。由于肾脏、肝脏等器官功能损害,白蛋白生成能力及功能低下且排出增多,肠胃血管痉挛使蛋白质吸收减少,因而可引起严重的低蛋白血症。患者血浆胶体渗透压降低,导致细胞内外滤过压不平衡,细胞内液移至细胞间隙,严重者可出现全身明显水肿,甚至浆膜腔积液(腹腔、胸腔、心包)。
5.心血管
子痫前期患者全身小动脉包括冠状动脉广泛痉挛,外周血管阻力增加,而发生一系列心血管和血液流变学的改变:平均动脉压升高,左心室舒张末期压力升高,收缩功能下降;冠状动脉广泛痉挛、内皮细胞损伤导致重度子痫前期患者出现不同程度的心肌损害,心肌细胞肥大,心肌间质局限性纤维变化,重者尚可见点状出血和局灶性坏死。再加上不同程度的贫血、低蛋白血症,血浆胶体渗透压降低,种种因素使子痫前期患者形成低排高阻型血流动力学改变,容易发展成急性左心衰竭。而子痫前期的内皮损害和胶体渗透压降低引起了组织液向肺间质和肺泡渗漏,尤其是产后存在严重的低蛋白血症时,极易发生急性肺水肿。左心衰竭和外周血管阻力升高是肺水肿的危险因素,合并原发性高血压者更易发生肺水肿。
6.胎盘-胎儿单位
血管痉挛及子宫蜕膜和基底层血管发生急性动脉粥样硬化,管腔变窄,极易引起子宫螺旋小动脉栓塞,导致胎盘功能下降,胎儿生长受限,胎儿宫内缺血、缺氧,甚至胎儿窘迫、宫内死亡。若胎盘血管破裂出血,可导致胎盘早剥。
治疗目的是控制病情、延长孕周、尽可能地保障母儿安全。治疗原则主要为降压、解痉、镇静等;密切监测母儿情况;适时终止妊娠是最有效的处理措施。
表3子痫前期高危因素与阿司匹林的使用

1.评估和监测
子痫前期病情复杂、变化快,分娩及产后生理变化及各种不良刺激均可导致病情变化,因此,对产前、产时及产后病情进行密切评估和监测十分重要,以便了解病情进展情况,及时进行干预治疗,避免不良妊娠结局发生。评估和监测的内容和频率需根据病情严重程度决定。
妊娠37周前,在初始诊断性评估后,对于病情稳定且不伴严重表现的子痫前期患者可选择门诊治疗及监测,这部分患者应能够依从频繁的母体和胎儿监测,并作好随时入院准备。重度子痫前期患者建议住院治疗,便于母胎评估,当病情进展迅速时有助于迅速干预。
评估内容主要包括严密监测子痫前期的发展或恶化情况。对于没有严重表现的子痫前期患者,建议每周1~2次产检,每周检查血小板计数、血肌酐和转氨酶水平,每周至少1次胎心监测及评估羊水量,每3~4周超声评估胎儿生长发育情况。若有病情恶化时,应尽早重复以上检查,必要时增加24小时动态血压、孕妇超声心动图、胎儿脐动脉血流、生物物理评分等。监测过程中应仔细询问有无严重表现的子痫前期症状(如头痛、视觉改变、上腹痛和气促等)。监测中进行患者宣教,所有子痫前期患者应了解重度子痫前期的症状和体征,并应每天监测和自我血压监测。若发生头痛、视觉改变、呼吸急促、右上腹或上腹痛,应立即告知医护人员。
产时进行连续母胎监测,以识别如下情况:高血压加重;母体肝、肾、心肺、神经或血液系统功能恶化;胎盘早剥;胎心异常。同时严密监测液体平衡,以免过度补液导致肺水肿、心力衰竭等严重并发症的发生。
妊娠期高血压可延续至产后,也可在产后首次出现,亦可进展为子痫前期甚至子痫,因此,产后仍需加强血压、子痫前期严重表现症状及体征的监测,以便及时降压、解痉等治疗。
2.一般治疗
(1)适当休息:
因为目前没有证据表明卧床休息对改善妊娠结局的有效性,并且卧床休息可增加住院患者静脉血栓栓塞症的风险,因此不建议严格卧床休息。
(2)饮食:
注意营养丰富而又不过度,保证充足的蛋白质和热量,适当补充多种维生素,如维生素C、维生素E、钙剂等。不限制盐和体液,对于全身水肿者应适当限制盐的摄入。
(3)精神和心理治疗:
加强与患者及其亲属的沟通,尽量解除思想顾虑,避免不良刺激影响。
3.降压治疗
(1)降压治疗时机:
有效治疗妊娠期重度高血压可以降低母亲的脑卒中、心力衰竭和其他严重并发症。因此,目前一致认为对妊娠期重度高血压(收缩压≥160mmHg和/或舒张压≥110mmHg)应予以积极降压治疗。
对于妊娠期非重度高血压是否降压治疗,各个国家的学术组织并没有达成共识。2018年国际妊娠期高血压研究学会(ISSHP)推荐妊娠期高血压患者降压时机为医院测量血压≥140/ 90mmHg或家庭测量血压≥135/85mmHg。2019年NICE推荐,无论是妊娠期高血压还是子痫前期患者,收缩压≥140mmHg或舒张压≥90mmHg均应予降压治疗,控制目标血压≤130/80mmHg。2020年ACOG对血压<160/ 110mmHg的妊娠期非重度高血压的药物治疗未做推荐。2021年中华医学会妊娠期高血压疾病血压管理专家共识推荐,对于血压<150/ 100mmHg者可密切观察,暂不应用降压药物治疗。只有当收缩压≥150mmHg或舒张压≥100mmHg或出现靶器官受损时方考虑应用药物治疗,目标血压为:无器官功能损伤,酌情将收缩压控制在130~155mmHg,舒张压控制在80~105mmHg;伴有器官功能损伤,则收缩压应控制在130~139mmHg,舒张压应控制在80~89mmHg;血压不可低于130/80mmHg,以保证子宫胎盘血流灌注。2022年SOGC建议对收缩压≥140mmHg或舒张压≥90mmHg的所有孕妇均应该给予降压治疗,并指出可显著降低孕妇脑卒中的发生率。2015年Magee等在NEJM上发表了一项多中心、开放式随机对照研究,即妊娠期高血压控制研究(the control of hypertension in pregnancy study,CHIPS),评估比较了妊娠期高血压严格控制舒张压至85mmHg与非严格控制舒张压至100mmHg对妊娠结局的影响,结果显示两组围产儿结局虽无显著差异,但当舒张压严格控制至85mmHg可降低13.1%母体发生重度高血压的风险。也正是基于这项研究,2022年SOGC将妊娠期高血压的控制阈值140/90mmHg中的目标舒张压更改为85mmHg。
尽管各国学术组织的观点不一,但基于CHIPS的研究证据和国内现状,为减少母胎并发症,我们建议:收缩压≥160mmHg和/或舒张压≥110mmHg的重度高血压必须尽快降压治疗;收缩压≥140mmHg和/或舒张压≥90mmHg的非重度高血压可考虑降压,尤其是并发脏器功能损伤时。目标血压:收缩压控制在130~139mmHg,舒张压控制在80~89mmHg,降压过程力求平稳,不可波动过大。为保障子宫胎盘血流灌注,血压不建议低于130/80mmHg。
(2)降压药物选择:
目前降压药物种类并不少,应首先选择不减少肾脏、胎盘血流灌注,同时对胎儿影响小的药物。降压药物选择时,也要根据产科医生的经验选用熟悉的药物,注意规范应用。一般不首先推荐使用阿替洛尔和哌唑嗪,并建议禁止使用血管紧张素转换酶抑制剂(ACEI)和血管紧张素Ⅱ受体拮抗剂。此外,2013年一篇Cochrane系统评价分析了治疗妊娠期重度高血压的药物,结果表明应用尼莫地平和硫酸镁降压治疗后,持续性高血压的发生率均较高,分别为46%和65%,且尼莫地平还可能增加新生儿出生后低血压的发生风险(RR 3.12,95%CI 0.63~15.40),因此,不推荐尼莫地平和硫酸镁作为降压药物使用。临床上常用的降压药物有:
1)拉贝洛尔:
为α、β肾上腺素受体阻滞剂,降低血压而不影响肾脏及胎盘血流量,并可对抗血小板凝集,促进胎儿肺成熟。该药起效快(1~2分钟),不引起血压过低或反射性心动过速。用法:口服,50~150mg,3~4次/d,30~60分钟起效,2~3小时达峰值;静脉注射,初始剂量20mg,10分钟后若无有效降压则剂量加倍,最大单次剂量80mg,直至血压控制;静脉滴注,50~100mg+5%葡萄糖250~500ml,根据血压调整滴速,待血压平稳后改口服,每天最大总剂量1200mg。脑出血、哮喘患者禁用;心脏及肝肾功能不全者慎用。
2)硝苯地平:
为钙离子通道阻滞剂,可解除外周血管痉挛,使全身血管扩张,血压下降,由于短效硝苯地平降压作用迅速,一般不主张舌下含服。用法:口服10mg,3~4次/d,必要时可加量,一般一天30~90mg,每天最大剂量不超过120mg。其副作用为心悸、头痛,使用时需监测血压,警惕低血压造成严重并发症。禁用于动脉粥样硬化性心血管疾病史。硝苯地平可选择短效、缓释或控释制剂,既往常用短效制剂降压,但由于短效硝苯地平降压过快,可能会影响子宫胎盘血流灌注,增加母胎不良预后的风险。因此,在治疗非重度妊娠期高血压时,开始更倾向于使用缓释或控释制剂。
3)甲基多巴:
可兴奋血管运动中枢的α受体,抑制外周交感神经而降低血压,妊娠期使用效果较好。用法:250mg口服,3~4次/d,每天最高不超过2g。其副作用为嗜睡、便秘、口干、心动过速。相比其他降压药物,其对胎儿的长期安全性已经得到更广泛的证实,常被一些国际权威组织作为一线用药推荐。但由于作用温和,起效缓慢,单纯口服该药可能无法降到目标血压。另外,受药物供应短缺的影响而使一些国家包括中国临床使用有限。
4)肼屈嗪:
是一种直接小动脉血管扩张剂,使外周血管阻力降低。用法:口服10~20mg,2~3次/d;5mg静脉或肌内注射,随后每20~40分钟给予5~10mg,最大剂量可至20mg;或持续静脉泵入,0.5~1.0mg/h。降压过快可导致低胎盘灌注;有心动过速、头晕、恶心、呕吐、震颤、上腹痛、体液潴留等不良反应。由于口服可导致反射性心动过速和液体潴留限制其临床应用,主要是静脉用药治疗妊娠期急性重度高血压。
5)尼卡地平:
二氢吡啶类钙离子通道阻滞剂。用法:起始剂量20~40mg口服,3次/d;静脉滴注1mg/ h起,根据血压变化每10分钟调整剂量。
6)乌拉地尔:
为α肾上腺素受体阻滞剂,同时作用于中枢与外周,降压效果快。用法:50~100mg+0.9%生理盐水250ml,4~8滴/min起静脉滴注。其易引起直立性低血压;若用药前已予以其他降压药,则使用时保证充分间隔时间,必要时减量;疗程不超过7天。
7)酚妥拉明:
为α肾上腺素受体阻滞剂。用法:10~20mg+5%葡萄糖100~200ml,以10μg/min静脉滴注。
8)硝酸甘油:
作用于氧化亚氮合酶,可同时扩张动脉和静脉,降低前后负荷,主要用于合并心力衰竭和急性冠脉综合征时高血压急症的降压治疗。起始剂量10mg+5%GS(0.9%NS)500ml,20滴/min起静脉滴注。
9)硝普钠:
强效血管扩张剂,扩张周围血管使血压下降。由于药物能迅速通过胎盘进入胎儿体内,并保持较高浓度,其代谢物(氰化物)对胎儿有毒性作用,在妊娠期使用要谨慎。分娩或产后血压过高,应用其他降压药效果不佳时,方考虑使用。用法:50mg+5%GS(0.9%NS)500ml,静脉滴注,0.6ml/ h起滴,每次调整0.3~0.6ml/ h直至目标血压,最大剂量400μg/ min。妊娠期仅适用于其他降压药物无效的高血压危象孕妇,使用时请注意避光,减少分解为氰化物的风险。用药期间,严密监测血压及心率。
(3)急性重度高血压的治疗:
2019年ACOG发布了急性重度妊娠期高血压的处理指南,对产时及产后高血压急症建议硝苯地平、肼屈嗪和拉贝洛尔降压治疗,但由于国内不常使用肼屈嗪,故主要讲述硝苯地平和拉贝洛尓的具体使用方法,见图2及图3。
急性重度高血压是发生脑出血及脑梗死的重要危险因素,迅速控制急性重度高血压对子痫前期和子痫的临床结局至关重要。确认重度高血压后,应在30~60分钟内给予一线降压药物,以减少脑出血和脑梗死的风险。重度高血压不能突然降至正常范围,收缩压应控制在140~150mmHg,舒张压控制在90~100mmHg。初始降压达标后,应继续给予降压药物,保持血压稳定。
值得注意的是,短效硝苯地平的使用仍存在争议。有学术组织对于妊娠期急性重度高血压的降压治疗,推荐的一线药物是拉贝洛尓和肼屈嗪,而并非短效硝苯地平。主要的原因是,有研究发现若按上述方案治疗,可能会出现降压过快、母体交感神经系统反射性激活致心率过快及头痛,严重可发生脑卒中、心肌梗死、心律失常等心脑血管并发症。鉴于此,2018年ISSHP推荐硝苯地平治疗急性重度高血压时每次口服剂量更改为10mg,共计2次,间隔时间延长为45分钟。2022年,Magee等人也推荐了不同的硝苯地平治疗方案,即每次口服10mg,共计使用4次,使用间隔时间延长至30~60分钟。
鉴于上述争议,根据临床使用现状,笔者建议首选静脉给药作为急性重度高血压的一线用药,仅在无法建立静脉通道时,首先选择短效硝苯地平口服,但使用剂量及间隔时间建议延长至30~60分钟。若拉贝洛尔降压效果不满意或医疗机构缺乏该药时,应根据母体因素、医疗机构的药物种类及医师用药习惯决定降压药物的使用,主要目标是降压平稳有效,力求减少严重并发症的发生。
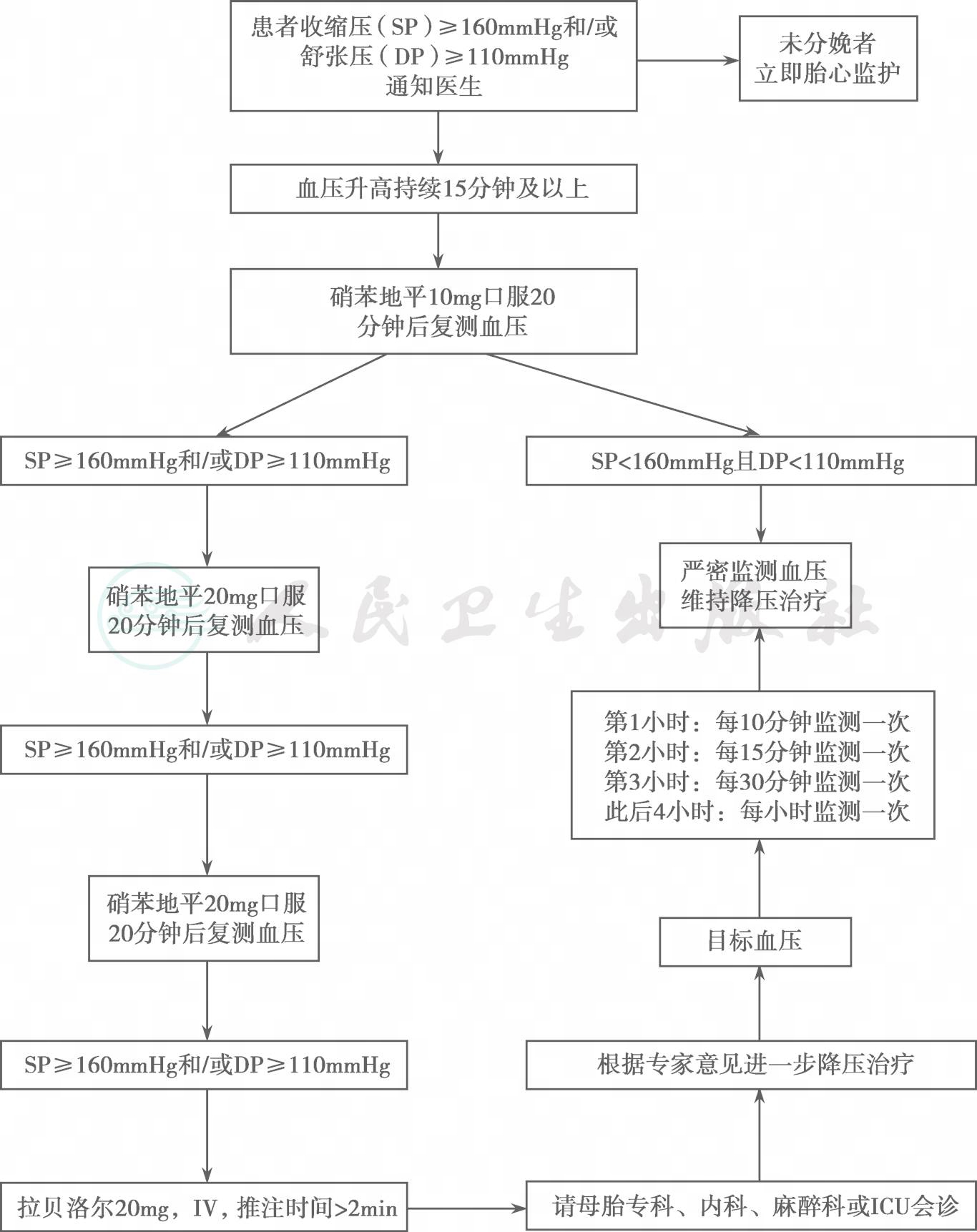
图2急性重度高血压硝苯地平给药方案
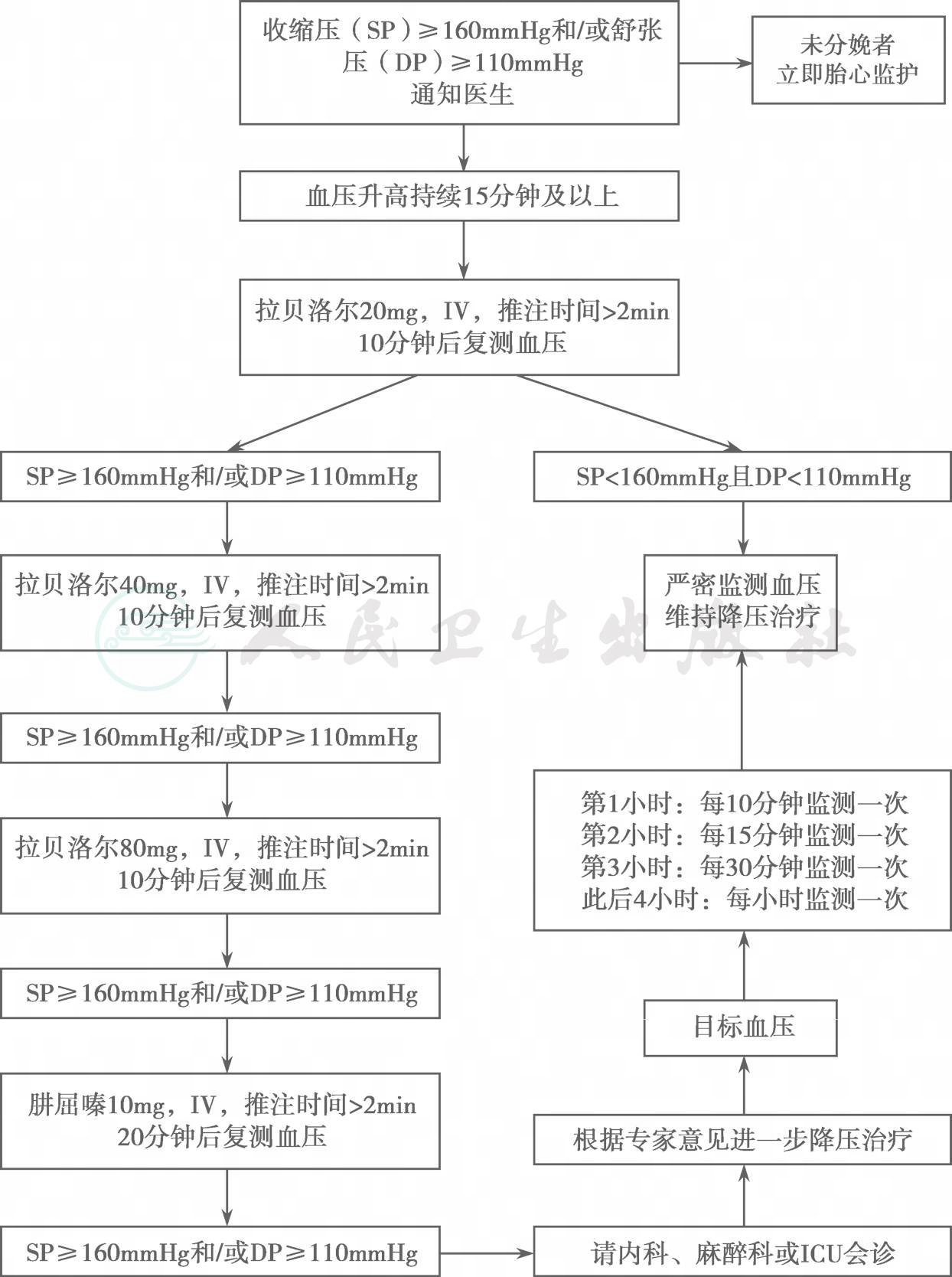
图3急性重度高血压拉贝洛尔给药方案
(4)降压治疗的注意事项:
1)降压药的效果有很大的个体差异性,故无法精确地预测出降压效果。对每位患者需要根据用药后的反应进行药物种类和剂量的调整。关键是能否及时发现血压升高或变化,在病程的最早阶段就进行平稳的血压控制。除非是重度高血压患者,否则不需要开始就静脉应用降压药。即使是静脉应用降压药的患者,在血压控制稳定后建议改口服用药。口服降压时,建议采用联合用药,一则联合用药的效果比单一用药好,再则联合用药可以减少每种药物的剂量,避免单一大剂量用药带来可能的副作用。
2)在应用降压药物时注意平稳降压,减少血压波动,尤其要注意清晨血压波动峰值,从而防止或减缓重度子痫前期患者心脑血管并发症及胎盘早剥等的发生。降压太快或幅度太大会导致胎盘灌注以及氧输送减少,引起胎儿窘迫,特别是在胎儿生长受限或监护有异常的情况下更是如此,同时也增加孕妇脑血管意外、胎盘早剥等严重并发症的风险。在与硫酸镁同时应用时,因为其外周血管扩张作用,降压药物的效应可能被放大。血压测量同时要确保患者夜间得到充分休息。
3)对于需要行剖宫产终止妊娠的患者,需要减缓降压速度或是停用降压药,因为硬膜外麻醉可以降低大约15%的血压。而且麻醉效果比较好的情况下,容易出现仰卧位低血压综合征,所以通常不需要在手术时应用降压药,但术后30分钟,应注意麻醉效果过后的血压回升,及时应用降压药物控制血压波动。
4)慢性肾衰竭患者的高血压比较难以控制,其中部分原因是血容量过多。既往有肾脏或心脏病史者可适当加用利尿剂。
5)重度高血压患者治疗过程中出现长时间昏迷、视神经盘水肿、偏瘫或在硫酸镁治疗时发生抽搐,或产后48小时后发生抽搐,应做CT检查,除外脑血管意外的发生。
4.解痉治疗
2002年发表在Lancet上经典的Magpie Trial试验发现,硫酸镁预防重度子痫前期患者发生子痫而需要治疗的人数(number need to treat,NNT)为90,也就是说仅需要治疗90个患者就能够预防1例子痫的发生。因此,截至目前,硫酸镁仍被公认是预防子痫前期发生子痫和治疗子痫疗效最确切、应用最广泛的药物。研究发现,硫酸镁控制子痫再次发作的效果优于地西泮、苯巴比妥和冬眠合剂等镇静药物,故除非存在硫酸镁应用禁忌证或硫酸镁治疗效果不佳,否则不推荐使用苯巴比妥和苯二氮类用于子痫的预防或治疗。
(1)作用机制:
镁离子可通过以下机制解痉:①抑制运动神经末梢对乙酰胆碱的释放,阻断神经和肌肉间的传导,使骨骼肌松弛,从而能有效地预防和控制子痫的发作;②使血管内皮合成前列腺素增加,抑制内皮素合成,降低机体对血管内皮紧张素Ⅱ的反应,缓解血管痉挛状态;③通过阻断谷氨酸通道阻止钙离子内流,解除血管痉挛、减少血管内皮损伤;④提高孕妇和胎儿血红蛋白的亲和力,改善氧代谢。
(2)用药指征:
①控制子痫抽搐或防止再抽搐;②预防重度子痫前期发展成子痫;③重度子痫前期围分娩期用药,预防产时或产后子痫。硫酸镁不可作为降压药使用。
(3)治疗时机:
对于决定进行保守治疗的重度子痫前期女性,应考虑给予硫酸镁。硫酸镁的应用在剖宫产或阴道分娩时应持续使用,并维持到产后24小时。
(4)治疗方案:
首次负荷剂量4~6g,溶于25%葡萄糖20ml静脉推注(15~20分钟),或溶于5%葡萄糖100ml快速静脉滴注(15~20分钟),随后1~2g/ h静脉滴注维持。若静脉通道建立困难时,可选择深部肌内注射:初始剂量10g(每侧臀部注射5g),随后每4小时注射5g,为减少肌内注射的疼痛,可将25%硫酸镁20ml溶于2%利多卡因2ml中。硫酸镁24小时用药总量不超过25g,治疗过程中监测尿量、呼吸、腱反射和氧饱和度。
(5)注意事项:
血清镁离子的有效治疗浓度为1.8~3.0mmoL/ L,>3.5mmol/L即可出现中毒症状。使用硫酸镁必备条件:①膝腱反射存在;②呼吸≥16次/min;③尿量≥25ml/h(即≥600ml/ d);④备有10%葡萄糖酸钙。镁离子中毒时停用硫酸镁并缓慢静脉推注(5~10分钟)10%葡萄糖酸钙10ml。如患者同时合并肾功能障碍、心功能受损或心肌病、重症肌无力等,则硫酸镁应慎用或减量使用。若有条件者,建议用药期间监测孕妇的血清镁离子浓度。
(6)治疗副作用:
应用硫酸镁常见的轻度副作用有自觉发热、面颊潮红、恶心、呕吐、肌肉无力、头晕和注射部位刺痛感等,发生率在15%~67%。严重副作用包括:运动麻痹、腱反射消失、呼吸抑制、心律失常(传导时间延长)等,因此,重症肌无力患者禁用。当患者出现消化系统症状和疲乏无力时要警惕药物过量中毒,临床表现与HELLP综合征相似,应注意鉴别以免贻误治疗。
5.其他治疗
(1)镇静治疗:
镇静药物可以缓解孕妇紧张、焦虑情绪,改善睡眠,预防和控制子痫。
1)地西泮:
2.5~5mg口服,2~3次/d,或者睡前服用,可缓解患者紧张、失眠等症状,保证充足的休息。地西泮10mg肌内注射或静脉注射(>2分钟)用于控制子痫发作和再次抽搐。但有学者认为,地西泮控制子痫发作有心搏骤停的风险,故不推荐使用。
2)苯巴比妥:
镇静时口服剂量为30mg /次,每天3次,控制子痫时肌内注射0.1g。
3)冬眠合剂:
冬眠合剂由氯丙嗪(50mg)、哌替啶(100mg)和异丙嗪(50mg)组成,可抑制中枢神经系统,有助于解痉、降压、控制子痫抽搐。通常以1/3~1/2量肌内注射,或以半量加入5%葡萄糖溶液250ml静脉滴注。由于氯丙嗪可使血压急剧下降,导致肾及胎盘灌注降低,且对母胎肝脏有一定损害,故仅应用于硫酸镁治疗无效时。
(2)纠正低蛋白血症:
重度子痫前期患者普遍存在低蛋白血症,循环血量减少和血液浓缩。尽管扩容治疗可增加容量负荷,易致肺水肿和脑水肿而被认为弊大于利,但是严重的低蛋白血症,血浆胶体渗透压明显降低,可导致严重的胸、腹腔积液和心包积液,孕妇循环不稳定而造成难以控制的心力衰竭、肺水肿等。及时有效地补充蛋白质和血浆,纠正低蛋白血症对于重度子痫前期的治疗十分重要。分娩期和产后的血流动力学变化最为明显,血浆胶体渗透压可以从足月时的22mmHg降到产后16mmHg,而在子痫前期患者则是从足月时18mmHg降到产后14mmHg。血浆胶体渗透压的改变在产后6~16小时达到最低点,在产后24小时后恢复到产时水平。血管内外的胶体渗透压和流体静水压的平衡在重度子痫前期伴有严重低蛋白血症时被破坏,当产后回心血量增加时,胶体渗透压更进一步下降,此时最易发生心力衰竭和肺水肿。无论是在产前、产时还是产后,在心力衰竭控制平稳后,都可以给予人血清白蛋白或血浆,以提高胶体渗透压来稳定微循环,但需要警惕循环血量增加而再次诱发心力衰竭的可能,重要的是,应用白蛋白或血浆时,应严密监测病情和经静脉给予呋塞米。在分娩前注意逐步纠正低蛋白血症是稳定产时和产后微循环和防止心力衰竭发生的措施之一。
(3)糖皮质激素治疗:
大量循证医学证据已证实糖皮质激素对于早产胎儿促进胎肺成熟的作用。糖皮质激素在早发型重度子痫前期的应用,亦可以明显降低新生儿呼吸窘迫的发生,同时降低新生儿脑室内出血、感染和死亡的发生,并且并不增加母亲的并发症(用法详见第九章第三节早产。)
(4)利尿:
子痫前期孕妇不主张常规应用利尿剂,仅当孕妇出现全身性水肿、肺水肿、脑水肿、肾功能不全、急性心力衰竭时,可酌情使用呋塞米等快速利尿剂。甘露醇主要用于脑水肿,有心力衰竭或潜在心力衰竭时禁用,甘油果糖适用于有肾功能损害的孕妇。严重低蛋白血症伴有胸腹腔积液者,可补充白蛋白后给予利尿剂。
终止妊娠的原则和方法:终止妊娠是子痫前期治愈的最根本方法,终止妊娠的时机和方法应根据患者妊娠周数、严重并发症发生情况、家庭经济状况和当地医疗条件综合决定。
1.终止妊娠时机
下列情况可以考虑终止妊娠:①妊娠期高血压、无严重表现的子痫前期患者可期待至37周终止妊娠。②重度子痫前期患者:妊娠<24周,经治疗病情不稳定者建议终止妊娠;妊娠24~28周,根据母胎情况及当地母儿诊疗能力,决定期待治疗是否可行;妊娠28~34周,若病情不稳定,经积极治疗24~48小时病情仍加重,应终止妊娠;若病情稳定,可考虑期待治疗,并建议提前转至早产儿救治能力较强的医疗机构;妊娠≥34周者应考虑终止妊娠。
2.分娩方式的选择
分娩方式的选择应对孕妇和胎儿的整体状况包括病情和生育、家庭状况进行充分评估,进行个体化处理,如无剖宫产指征,原则上阴道试产。但如果无法短时间内阴道分娩,病情有加重可能,可考虑放宽剖宫产指征。
3.麻醉方式的选择
在阴道分娩的产程镇痛中,若没有其他禁忌证的情况下,子痫前期患者首选椎管内镇痛。
对于子痫前期患者的剖宫产手术,可以采用椎管内麻醉或全身麻醉,前者包括腰麻、腰硬联合麻醉(combined spinal epidural,CSE)或硬膜外麻醉。过去,硬膜外麻醉是一直被肯定应用的麻醉方法,腰麻被认为因快速发生交感神经阻滞出现严重低血压而限制使用。但近年来研究发现,与硬膜外麻醉相比,腰麻产生的血压下降幅度相似,腰麻患者因低血压而需要升压药物比例也并不增加。因此,腰麻在重度子痫前期患者中的使用是安全和有效的。腰麻操作通常比硬膜外麻醉快,可快速产生充分且可靠的双侧麻醉,但腰麻单次注射后的麻醉持续时间有限,且无法在应急情况下扩大和延长麻醉。硬膜外麻醉可通过逐步增加药量延长麻醉时间,但其效果弱于腰麻,不如腰麻可靠,起效也更慢。因此,CSE不仅具有腰麻和硬膜外麻醉的优点,同时也弥补了各自缺陷,已被临床广泛应用,也可作为重度子痫前期选择的一种麻醉方式。
在无椎管内麻醉禁忌情况下,子痫前期患者剖宫产应首选椎管内麻醉。若存在凝血功能障碍或有潜在出血风险时,椎管内麻醉有导致硬膜外血肿的风险,可以考虑选择全身麻醉。血小板减少有导致硬膜外血肿的风险,但目前各国关于血小板数值下限与禁忌使用椎管内麻醉的关系尚无统一定论,最近一项来自19个医疗机构84 471名孕妇的回顾性研究表明,血小板≥70×109/ L时硬膜外血肿的发生率极低(<0.2%)。因此,ACOG认为当血小板≥70×109/ L,并且病情平稳,无血小板继续减少风险及未使用抗血小板或抗凝治疗时,可以选择椎管内麻醉。
迄今为止,虽然早发型和晚发型的界定标准以34孕周为界、还是以32孕周为界尚未统一,但明确的是两者的病因和发病机制是不同的。早发型被认为是一种胎源性疾病,伴有较高的胎盘功能不良和胎儿生长发育受限发生率,围产儿死亡率较高,母儿预后差;晚发型被认为是一种母源性疾病,可能为潜在的母体疾病,胎盘功能及形态多数正常,并不影响胎儿的生长,故母儿预后较好。对于重度早发型子痫前期,既往的处理是不考虑孕周大小均提倡终止妊娠,结果导致因胎儿不成熟所致的围产儿死亡率大大增加。近年来,对于已经出现严重并发症者终止妊娠仍不容置疑;对无严重并发症的早发型重度子痫前期延迟分娩的保守治疗,可以延长孕周,改善围产儿妊娠结局。
早发型重度子痫前期患者建议住院治疗,入院后经过充分评估病情,明确有无严重的器官损害表现,决定是否进行期待治疗。
1.病例选择
严格选择适合的病例是采取期待治疗方案的第一步,病例的选择取决于胎儿和母亲两方面,包括孕周、胎儿情况以及评估母亲的病情严重程度和重症发生时间、医疗环境和救治条件,患方的意愿和经济状况都是应考虑的影响因素。原则上,母儿安全的前提下,病情相对稳定即可以继续期待治疗。
2.转诊
所有早发型重度子痫前期患者应在具备母儿重症监护的三级医疗保健机构进行严密监护,若所属医院不具有上述条件和资质,在决定保守治疗方案后,应及时转诊。
3.临床监测
在期待治疗过程中应当严密观察母体终末器官受累症状、体征和相应实验室指标的动态变化及其异常发生时间,同时严密监测胎儿生长情况。监测项目依具体病情而定,包括每天的胎心和胎动计数,在某些严重病例或胎盘功能受影响的病例,必要情况下进行每天2~3次NST。注意胎儿生物物理评分、胎儿生长发育情况和羊水量估计及脐动脉血流检查等。脐血管胎盘病变和眼底检查、脐动脉血流S/D比值之间呈平行关系。脐动脉舒张期血流波形是一种无创的胎儿安危监护手段,当出现脐动脉舒张末期血流缺失或反流时,需要进行干预治疗,当宫内环境已经不利于胎儿继续生长时,需及时终止妊娠。
4.期待治疗期间终止妊娠的指征
当出现以下母儿病情恶化时终止妊娠,母体指征有:持续重度高血压;头痛、上腹痛或视觉障碍等重度子痫前期症状的反复发作或加重;脑卒中;心肌梗死;HELLP综合征;肺水肿;子痫;疑似胎盘早剥或非前置胎盘引起的持续阴道出血。胎儿指征有:胎儿窘迫;死胎;孕周太小胎儿无法存活者。
5.终止妊娠的方式
如无产科剖宫产指征,原则上考虑阴道试产。但如果不能短时间内阴道分娩、病情有可能加重,可考虑放宽剖宫产指征(图4)。

图4早发型子痫前期的管理
HELLP综合征的治疗原则为在积极治疗子痫前期的基础上的对症治疗,适时终止妊娠。对症治疗包括:
1.预防出血
当血小板<50×109/L且血小板数量迅速下降或存在凝血功能障碍时应考虑备血及血小板;当血小板<20×109/L以及患者有明显出血倾向时,应输注新鲜的血小板悬液。也有学者建议,如果患者血小板<40×109/ L,在准备剖宫产前常规输注血小板,但预防性输注血小板并不能预防产后出血的发生。
2.保护肝脏功能
肝功能明显异常时,可以应用保护肝脏药物,如葡醛内酯、谷胱甘肽等。
3.糖皮质激素的应用
对于糖皮质激素在HELLP综合征中的应用仍没有一致的观点。既往观察性研究认为,糖皮质激素可快速改善HELLP综合征患者的实验室及临床指标,但在Cochrane发表的一篇纳入11项随机对照试验的研究中,比较了糖皮质激素与安慰剂或不治疗对HELLP综合征患者的效果,结果发现糖皮质激素并未显著改善孕妇严重并发症的发生及降低母儿死亡率,但能提高孕妇血小板计数。因此,糖皮质激素治疗HELLP综合征的证据仍不够充分,但当血小板<50×109/L时,可考虑糖皮质激素治疗。
4.产科处理
终止妊娠时机:当妊娠≥34周,或出现多器官功能障碍、DIC、肝脏梗死或出血、肾衰竭、胎盘早剥、胎儿状况不良等情况下应立即终止妊娠。对于母体状况稳定而仅有血液实验室检查轻度异常,并且胎儿状况良好时的处理原则仍有分歧:一些学者建议,糖皮质激素促胎肺成熟后可终止妊娠(图5);也有学者建议可继续保守治疗,直至母亲或胎儿方面出现新的终止妊娠指征,或妊娠至34周再终止妊娠。最根本的原则应视个案分析处理。
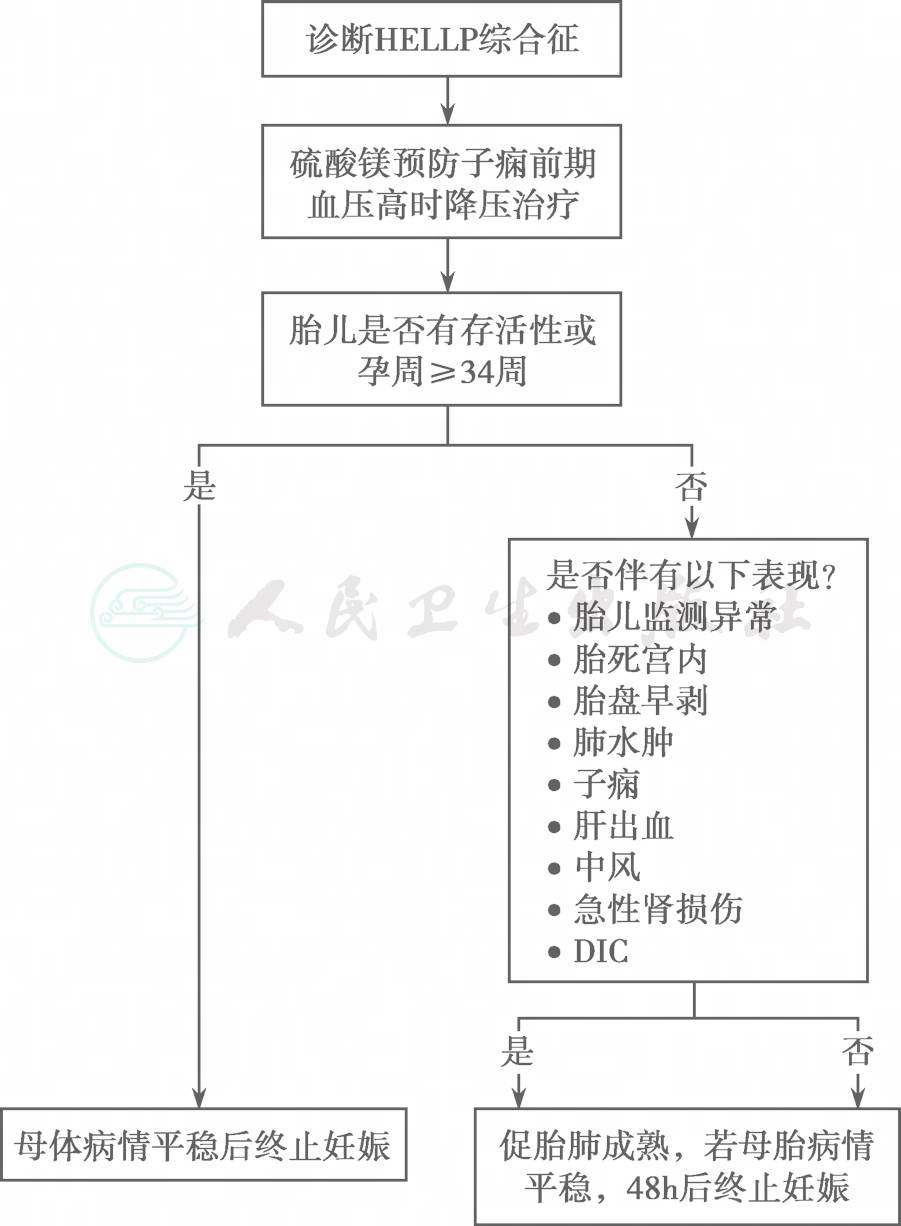
图5HELLP综合征的处理流程
1.预测
首次产检应进行危险因素评估,主张联合多项指标综合评估预测。
(1)危险因素:
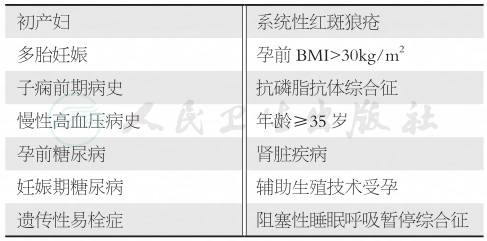
根据现有的研究证据,可将子痫前期的危险因素分为高危因素和中危因素。高危因素包括子痫前期病史、CKD、慢性高血压、糖尿病、自身免疫疾病(如抗磷脂抗体综合征或系统性红斑狼疮)。中危因素包括初产妇、初次产检BMI>30kg/m2、年龄≥35岁、多胎妊娠、妊娠间隔时间≥10年以及子痫前期家族史(母亲或姐妹)。当合并有1项高风险因素或1项以上中危因素则发生子痫前期的风险增加。2020年ACOG指南关于子痫前期风险因素见表4。
表4子痫前期的危险因素
(2)物理预测指标:
1)子宫动脉多普勒超声检查:
基于子痫前期病因的胎盘浅着床、免疫适应不良学说,1983年Campbell等首次运用多普勒超声检查子宫胎盘血流,发现子宫动脉的阻力随着孕龄的增加而降低,而在子痫前期的孕妇中,子宫动脉血流的频谱呈高阻状态。妊娠20~24周时行子宫动脉多普勒血流检测,如子宫动脉搏动指数(uterine arteria pulsatile index,UTPI)和阻力指数(resistance index,RI)持续升高或出现子宫动脉舒张早期切迹等异常波形,有助于预测子痫前期的发生。尽管有系统评价发现在发生子痫前期风险较高的女性中,中期妊娠评估子宫动脉搏动指数及子宫动脉切迹可最佳预测子痫前期的风险(敏感性19%、特异性99%),子宫动脉阻力指数增加可最佳预测重度子痫前期的风险(敏感性80%、特异性78%)。但基于现有的大量研究证据并不支持常规使用多普勒超声检查筛查子痫前期,因为研究者们使用的多普勒分析技术、异常血流速度波形的定义、研究人群、筛查孕周以及子痫前期的诊断标准都不相同,无论是使用单一指标还是与其他指标组合,对早发型子痫前期的预测率都较低,而对晚发型子痫前期的预测率则更低。
2)眼动脉多普勒检查:
不同于子宫动脉,眼动脉多普勒血流的改变并不是直接由胎盘滋养细胞浸润导致,可能与孕妇血流动力学改变有关。一项系统评价评估了眼动脉多普勒血流对子痫前期的预测作用,发现初始眼动脉舒张期峰值流速>23.3cm/s时,可预测早发型子痫前期的发生(敏感性为61%、特异性为73.2%,AUC 0.68),但预测晚发型子痫前期价值较低。与子宫动脉多普勒检查相似,其在独立预测早发型或晚发型子痫前期方面,临床价值有限。
(3)生物标志物预测指标:
1)血管生成调节因子:
弥漫性内皮细胞损伤和毛细血管通透性增加是子痫前期的病理生理性标志,而血管生成调节因子的异常表达对子痫前期的发病机制具有重要作用。近年来有大量关于血管生成调节因子预测子痫前期的研究,其中最为热点的是血管内皮生长因子(vascular endothelial growth factor,VEGF)和胎盘生长因子(placental growth factor,PLGF)以及2种抗血管生成蛋白:可溶性内皮因子(soluble endoglin,sEng)和可溶性fms样络氨酸激酶1(soluble fms-like tyrosine kinase 1,sFlt-1)。妊娠中期,这些血管生成调节因子在血液和尿液中的浓度变化会在子痫前期临床症状出现前数周或数个月发生变化,所以将它们作为预测子痫前期的潜在生化标志物,并可在一定程度上反映病情的轻重。2016年一项具有里程碑意义的多中心临床试验发现sFlt-1/PLGF比值对短期预测子痫前期具有临床价值。当sFlt-1/ PLGF比值≤38时1周内发生子痫前期的阴性预测值为99.3%,sFlt-1/ PLGF比值>38时4周内发生子痫前期的阳性预测值为36.7%,推测sFlt-1/ PLGF比值可能最有益于预测子痫前期。但上述生物指标能否在子痫前期相关的不良妊娠结局的早期预测,尚缺乏有效证据,在这一作用得到更好的证实之前,目前不常规推荐临床应用。
2)其他实验室检查:
母体血清分析物检测是唐氏综合征筛查项目的一个重要组成部分。越来越多的研究证据表明,在妊娠早期和中期,若发生原因不明的母亲血清分析物浓度异常,如妊娠相关血浆蛋白A(pregnancy-associated plasma protein A,PAPP-A)以及游离胎儿DNA水平异常,可能与胎盘功能异常相关,可用于筛查不良妊娠结局,包括子痫前期。尽管这些指标存在一定的相关性,但预测的准确性,无论是单独使用还是与其他危险因素联合,仍然低于临床有效筛查试验的理想水平。此外,尿酸、纤维连接蛋白、氧化应激标志物和促炎症细胞因子等指标异常也与子痫前期发生有关,但其预测价值仍需进一步的研究。
3)多因素联合预测模型:
鉴于单个指标预测价值有限,目前更多的研究倾向于多因素联合预测子痫前期发生风险。尽管许多研究者已创建了多种基于母体因素、多普勒超声指标、生物化学指标等多因素联合预测子痫前期模型,然而,大多数预测模型未进行效能验证或未通过效能验证。
值得关注的是英国胎儿医学基金会(Fetal Medicine Foundation,FMF)的早期妊娠预测模型。FMF使用贝叶斯理论,结合通过孕妇特征和病史计算的前涉风险和孕期不同孕周、不同生物物理、生化指标进行风险计算。效能验证发现,妊娠11~13周,在假阳性率10%的情况下,联合母体因素、平均动脉压(MAP)、子宫动脉搏动指数(UTPI)、PLGF,可以预测90%的早发型子痫前期、75%未足月子痫前期及45%足月子痫前期。该模型在亚洲人群中验证表明,在筛查假阳性率分别为5%、10%、15%和20%时,未足月子痫前期的检出率为48.2%、64%、71.8%和75.8%,明显优于英国国家卫生与临床优化研究所(NICE)指南和ACOG指南传统筛查模型(基于母体特征、产科因素及既往病史联合预测)PE的检出率(前者假阳性率为5.5%时检出率26.3%,后者假阳性率为20.4%时检出率54.6%)。当然,筛查方式的最终选择不仅取决于筛查效果,也需要考虑到当地卫生经济条件及实施的可行性。2019年国际妇产科联盟(FIGO)指南推荐对所有孕早期女性进行PE风险筛查,当风险≥1%时,则为PE高风险孕妇,可给予150mg/d阿司匹林口服预防PE。如果所在地区医疗资源有限,推荐采用二阶段筛查策略,即对所有孕妇常规使用母体危险因素和MAP进行未足月PE筛查,对于筛查出的危险人群再进行PLGF和UTPI或PAPP-A测量。一项纳入12万单胎妊娠女性的前瞻性研究发现,在筛查假阳性率为10%时,两阶段的PE检出率仍可高达71%。多因素联合预测模型虽然提高了预测PE的效果,但相关预测指标检测成本较高,目前仍未广泛应用于临床实践,还需结合中国国情开展前瞻性、大样本量的多中心临床研究以制订适合中国的方案。
2.预防
随着子痫前期的发病机制认识的深入,人们对于子痫前期的预防措施进行了广泛的研究,但大多数研究结果都不太理想。迄今为止,除低剂量阿司匹林的使用得到国内外广泛认可外,其他的预防措施都被认为不能起到有效的预防作用。
(1)一般预防措施:
子痫前期高风险孕妇妊娠期应适度锻炼,合理安排休息,以保持妊娠期身体健康。不推荐严格限制盐的摄入,也不推荐肥胖孕妇限制热量摄入。
(2)低剂量阿司匹林:
依据目前大量的研究证据,低剂量阿司匹林是最有效的药物预防方法。在孕早期进行子痫前期风险筛查和评估后,明确具有高风险的孕妇建议在妊娠11~14周开始每晚口服阿司匹林,剂量75~150mg,服用至妊娠36周或分娩时或确诊子痫前期时。不同指南对于阿司匹林的使用条件、起止时间及剂量的要求略有不同,总体而言预防措施的施行原则是低剂量、早使用、近全程,但获益程度取决于个体的多种因素,如使用药物的依从性等。目前就高危PE风险的确切标准尚未达成共识,而这对于指导用药人群具有重要意义。FIGO指南推荐妊娠早期使用FMF联合预测模型进行PE风险评估,对计算风险≥1%的孕妇,推荐孕11~14周起每晚口服阿司匹林150mg。美国预防服务工作组(United States Preventive Services Task Force,USPSTF)和ACOG指南则是基于临床危险因素的风险评估标准,推荐以下人群使用低剂量阿司匹林预防PE见表2-9-11,使用的阿司匹林剂量为81mg*。虽然基于临床危险因素预测PE简单、经济,但研究发现其预测敏感度不足40%,可能会造成临床上很多孕妇接受不必要的治疗,同时增加孕妇服药的焦虑以及非甾体类药物应用的副作用。因此,作者更倾向于多因素联合预测后给予小剂量阿司匹林预防PE。
(注:*不同国家阿司匹林的剂量略有不同。在美国,成人阿司匹林的剂量为325mg,小剂量阿司匹林又被称为“宝宝阿司匹林”,其剂量为成人剂量的1/4,常被用于各种慢性疾病的预防。目前美国“宝宝阿司匹林”的剂量为81mg,这就是ACOG指南中指定剂量的由来。而在英国,成人阿司匹林的剂量则为300mg,对应的小剂量“宝宝阿司匹林”为75mg。因此,在各国指南中我们可以看到不同的应用剂量。)
(3)钙剂补充:
最早由Belizan等于1980年报道低钙饮食的孕妇发生子痫前期的危险增加,随后多项研究显示,妊娠期补钙可降低血压并预防子痫前期的发生。2010年WHO提出建议,对于钙摄入量低(<800mg/d)的女性,补充钙替代制剂(钙元素≤1g/ d)或钙补充剂(钙元素1.5~2g/d)可能会降低子痫前期的发生风险。2018年WHO再次验证了这一结论,并推荐在初次产检时就开始指导补充钙剂。Cochrane一项关于低钙摄入地区孕妇子痫前期预防措施荟萃分析发现,子痫前期和妊娠期高血压发生风险在钙剂补充后显著降低,但其预防效果对于正常钙摄入女性收效甚微。
(4)其他预防措施:
若高风险孕妇对阿司匹林过敏或不耐受,且缺乏其他证据支持的干预措施,则应密切监护和期待治疗,包括频繁的门诊或家庭血压监测以早期识别和诊断子痫前期。其他的治疗方法,如增加镁,锌,叶酸,维生素C、D、E或鱼油的摄入,口服他汀类药物、二甲双胍对于预防子痫前期的效果尚缺乏可靠的研究证据。













