英文名称 :hypertensive disorder in pregnancy
中文别名 :妊娠期高血压疾病;妊娠期高血压
妊娠期高血压疾病是妊娠期特有的疾病,其患病率约占孕妇的5%~10%,可导致胎盘破裂、脑卒中、弥散性血管内凝血、多器官功能衰竭、胎儿生长受限等并发症,是孕产妇、胎儿死亡的主要原因之一。
妊娠期高血压疾病的发病原因至今尚未阐明,但是,在临床工作中确实发现有些因素与妊娠期高血压疾病的发病密切相关,称之为易发因素。其易发因素及主要病因学说如下:
(一)易发因素
依据流行病学调查发现,妊娠期高血压疾病可能与以下因素有关:① 初产妇。② 年轻孕产妇(年龄≤18岁)或高龄孕产妇(年龄≥35岁)者。③ 精神过度紧张或受刺激致使中枢神经系统功能紊乱者。④ 寒冷季节或气温变化过大,特别是气温升高时。⑤ 有慢性高血压、慢性肾炎、糖尿病等病史的孕妇。⑥ 营养不良,如贫血、低蛋白血症者。⑦ 体形矮胖者,即体重指数[体重(kg)/身高(m)2]>24者。⑧ 子宫张力过高(如羊水过多、双胎妊娠、糖尿病巨大儿等)者。⑨ 家族中有高血压史,尤其是孕妇之母有重度妊娠期高血压史者。
(二)病因学说
1.免疫学说
妊娠被认为是成功的自然同种异体移植。从免疫学观点出发,认为妊娠期高血压疾病病因是胎盘某些抗原物质免疫反应的变态反应,与移植免疫的观点很相似。但与免疫的复杂关系有待进一步证实。
2.子宫-胎盘缺血缺氧学说
临床发现妊娠期高血压疾病易发生于初产妇、多胎妊娠、羊水过多者。本学说认为是由于子宫张力增高,影响子宫血液供应,造成子宫-胎盘缺血缺氧所致。此外,全身血液循环不能适应子宫-胎盘需要的情况,如孕妇有严重贫血、慢性高血压、糖尿病等亦易伴发本病。
3.血管内皮功能障碍
研究发现妊娠期高血压疾病者,细胞毒性物质和炎性介质如氧自由基、过氧化脂质、血栓素A2等含量增高,而前列环素、维生素E、血管内皮素等减少,诱发血小板凝聚,并对血管紧张因子敏感,血管收缩致使血压升高,并且导致一系列病理变化。此外,气候寒冷、精神紧张也是本病的主要诱因。
4.营养缺乏及其他因素
据流行病学调查,妊娠期高血压疾病的发生可能与钙缺乏有关。妊娠易引起母体缺钙,导致妊娠期高血压疾病发生,而孕期补钙可使妊娠期高血压疾病的发生率下降,但其发生机制尚不完全清楚。另外,以白蛋白缺乏为主的低蛋白血症、锌、硒等的缺乏与子痫前期的发生发展有关。此外,其他因素如胰岛素抵抗、遗传等因素与妊娠期高血压疾病发生的关系亦有所报道。
我国妊娠期高血压发病率报道为9. 4%,国外报道为7%~12%,近年因产前保健的普及及临床诊治的规范化推广,发病率呈下降趋势。2006年WHO数据统计显示,发达国家中16%孕产妇死亡归因于妊娠期高血压疾病;2000~2005年对我国31个省、自治区、直辖市的监测资料分析,妊娠期高血压疾病造成的孕产妇死亡率为4. 2/10万,占死亡总数的9. 3%。故妊娠期高血压为孕产妇死亡的主要原因之一。
尚未完全阐明,环境、免疫、遗传学因素均可在子痫前期发病过程中发挥作用。
目前较为公认的是子痫前期发病机制的“两阶段学说”,即:第一阶段,在孕早期,由于免疫、遗传、内皮细胞功能紊乱等因素可造成子宫螺旋小动脉生理性血管重铸障碍,滋养细胞因缺血导致侵袭力减弱,造成胎盘浅着床,子宫动脉血流阻力增加,致使胎盘灌注不足,功能下降。第二阶段,孕中晚期缺血缺氧的胎盘局部氧化应激反应,诱发内皮细胞损伤,从而释放大量炎症因子,形成炎症级联效应和过度炎症的发生,引起子痫前期、子痫各种临床症状。
1.滋养细胞侵袭异常
正常妊娠时,胎盘的细胞滋养层细胞分化为绒毛滋养细胞(villous trophoblast)和绒毛外滋养细胞(extravillous trophoblast,EVT)。EVT浸润子宫内膜基质直至子宫肌层的内1/3处,并可进入子宫螺旋动脉管腔逐渐替代血管壁平滑肌细胞、内皮细胞。充分的子宫螺旋动脉重铸使血管管径扩大,动脉由高阻力低容量血管转变为低阻力高容量血管,胎盘的血流量提高以满足胎儿生长的需要。相比之下,在子痫前期病人中,EVT浸润过浅,仅达螺旋动脉的蜕膜部分,造成“胎盘浅着床”,导致子宫螺旋动脉重铸不足,其管径为正常妊娠的1/2、血管阻力增大,胎盘灌注减少,从而引起子痫前期的一系列症状。
滋养细胞分化缺陷是导致螺旋动脉EVT浸润缺陷的一种可能机制。在内皮细胞浸润过程中,滋养细胞分化涉及许多分子表达的改变,包括:细胞因子、黏附分子、细胞外基质分子、金属蛋白酶、Ⅰb类主要组织相容性复合体分子(人类白细胞抗原human leukocyte antigen,HLA-G)。在正常分化过程中,入侵的滋养层细胞可改变其本身黏附分子的表达,从上皮细胞特征(整合素α6/β1、整合素αⅤ/β5和E-钙黏着蛋白)转变为内皮细胞特征(整合素α1/β1、整合素αⅤ/β3和VE-钙黏着蛋白),该过程被称为假性血管发生。而子痫前期病人的滋养层细胞无黏附分子表达的上调或假性血管发生。对重度子痫前期病人的滋养层细胞进行的转录组学和培养研究表明,信号蛋白3B可能是一个候选蛋白,它通过抑制血管内皮生长因子的信号传递,可导致滋养层细胞的分化和浸润受损。
2.免疫学因素
胎儿是一个同种异体半移植物,成功的妊娠要求母体免疫系统对其充分耐受,其实质是母胎界面上的母体免疫细胞对胎盘滋养细胞呈低反应性。对可能促进胎盘发育异常的免疫学因素的关注,部分基于以下观察:①之前暴露于父系/胎儿抗原似乎可抵抗子痫前期的发生;②未经产的女性、在不同妊娠中变换性伴侣的女性、两次妊娠间隔时间较长的女性、使用屏障避孕的女性以及通过卵细胞质内单精子注射妊娠的女性,其暴露于父系抗原较少,发生子痫前期的风险较高;③通过卵母细胞捐赠妊娠的女性与使用自体卵母细胞妊娠的女性相比,前者子痫前期的发生率更高。以上结果支持以下假设:母亲和胎儿之间的免疫不耐受可能在子痫前期的发病机制中发挥作用。
在EVT侵入螺旋动脉的过程中,会与蜕膜自然杀伤(dNK)细胞、母体血液中的NK细胞(CD56+CD16+)和T细胞接触。EVT表达HLA-C和HLA-G,两者可作为NK细胞表达的杀伤细胞免疫球蛋白样受体(KIR)的配体,以免被NK细胞杀伤。EVT如减少或缺乏HLA-G表达,将不可避免地被细胞毒性NK细胞杀伤,引起滋养细胞侵入过浅及螺旋动脉管腔狭窄。特异性免疫研究集中在T细胞,正常妊娠时母体Th1/Th2免疫状态向Th2偏移,但子痫前期向Th1型偏移。这些都使母体对胚胎免疫耐受降低,引起子痫前期。
3.血管内皮细胞受损
所有子痫前期的临床特征均可解释为机体对全身内皮功能障碍的临床反应。例如,高血压是由内皮细胞对血管张力的控制发生紊乱导致的,蛋白尿和水肿是由血管通透性增加导致的,凝血病是内皮异常表达促凝物质的结果。头痛、癫痫发作、视觉症状、上腹痛和胎儿生长受限是靶器官血管内皮功能障碍的后遗症,这些靶器官包括脑、肝、肾和胎盘。
胎盘形成需广泛的血管生成以建立一个合适的血管网,为胎儿提供氧气和营养。发育中的胎盘可产生各种促血管生成因子和抗血管生成因子,这些因子之间的平衡对胎盘的正常发育很重要。抗血管生成因子的产生增加打破了促血管生成因子如血管内皮生长因子(vascular endothelial growth factor,VEGF)、胎盘生长因子(placental growth factor,PlGF)和抗血管生成因子(sFlt-1)之间的平衡,导致子痫前期特征性的全身血管内皮功能障碍。其中sFlt-1通过与循环中的VEGF和PlGF结合并阻止这两种因子与其内源性受体相互作用,可拮抗这两种因子促血管生成的生物学活性。研究发现胎盘表达和分泌sFlt-1增加在子痫前期的发病机制中起关键作用。
但目前尚不清楚触发胎盘产生sFlt-1增加的因素。最可能的触发因素是胎盘缺血。而sFlt-1分泌的增加是子痫前期特征性的早期胎盘发育异常的原因,还是机体对某种其他因素导致胎盘缺血的继发性反应,目前尚无定论。遗传学因素和胎盘的大小(如,多胎妊娠)在sFlt-1过量产生中也可能发挥作用。
子痫前期的另一种重要介导因子是胎盘来源的可溶性内皮因子(soluble endoglin,sEng),它是转化生长因子-β(transforming growth factor,TGF-β)的一个辅助受体,在血管内皮细胞和合体滋养细胞的细胞膜上高表达。研究表明,sEng是一种抗血管生成蛋白,作为sFlt-1的协同因子在子痫前期的全身内皮功能障碍的发病机制中发挥作用。
4.遗传因素
子痫前期的家族多发性提示该病可能存在遗传因素。
研究发现,13号染色体携带有sFlt-1和Flt-1基因。携带该染色体额外拷贝的胎儿(如,13-三体)与该染色体正常的胎儿相比,在前者中产生的这些基因的产物更多,从而导致其子痫前期的风险增加。12q中的一个不同位点可能与HELLP综合征有关,但与不伴HELLP综合征的子痫前期无关,这表明在HELLP综合征中重要的遗传学因素可能不同于那些在子痫前期中的遗传学因素。研究表明,12q23中长非编码区RNA的改变是可能导致HELLP综合征的一个潜在机制。该长非编码RNA调控一大组基因,这些基因可能对EVT的迁移发挥重要作用。
其他候选基因有血管紧张素原基因变异型(T235)、内皮型一氧化氮合酶基因、肾素-血管紧张素-醛固酮系统基因、Fas/FasL基因、V Leiden基因、凝血酶原基因、凝血酶原调节蛋白(TM)、亚甲基四氢叶酸还原酶(MTHFR)基因、线粒体DNA突变、脂蛋白脂肪酶基因(LPL)、载脂蛋白E基因、TNF-α基因、HLA-G、HLA-DR4、印迹基因等。因子痫前期的遗传易感性,特别是其他基因和环境因素的相互作用引起复杂性表型表达,所以任何候选基因都可能引起子痫前期。
目前妊娠期高血压疾病分为4类,包括妊娠期高血压、子痫前期和子痫、妊娠合并慢性高血压和慢性高血压并发子痫前期。
(1)妊娠期高血压:
妊娠期高血压(gestational hypertension)是指妊娠20周后首次出现的高血压(收缩压≥140mmHg和/或舒张压≥90mmHg),并于产后12周内恢复正常,尿蛋白检测阴性。当收缩压≥160mmHg和/或舒张压≥110mmHg时称为重度妊娠期高血压。
(2)子痫前期和子痫:
子痫前期(preeclampsia)是指妊娠20周后出现收缩压≥140mmHg和/或舒张压≥90mmHg,且伴有下列任一项:①尿蛋白≥0.3g/24h,或尿蛋白/肌酐比值≥0.3,或随机尿蛋白≥(+);②无蛋白尿但伴有以下任何一种器官或系统受累:心、肺、肝、肾等重要器官,或血液系统、消化系统、神经系统的异常改变,胎盘-胎儿受到累及等。当血压和/或尿蛋白水平持续升高,发生母体器官功能受损或胎盘-胎儿并发症的风险也增高,子痫前期孕妇出现下列任一项可诊断为重度子痫前期:①血压持续升高,收缩压≥160mmHg和/或舒张压≥110mmHg;②持续性头痛、视觉障碍或其他中枢神经系统异常表现;③持续性上腹部疼痛及肝包膜下血肿或肝破裂表现;④肝酶异常,血谷丙转氨酶或谷草转氨酶水平升高;⑤肾功能受损:尿蛋白>2.0g/24h、少尿或血肌酐>106μmol/L;⑥低蛋白血症伴腹腔积液、胸腔积液或心包积液;⑦血液系统异常:血小板计数呈持续性下降并低于100×109/L、微血管内溶血;⑧心功能衰竭;⑨肺水肿;⑩胎儿生长受限或羊水过少、胎死宫内、胎盘早剥等。
子痫(eclampsia)是指在子痫前期基础上发生不能用其他原因解释的抽搐。子痫是妊娠期高血压疾病最严重的阶段,前驱症状短暂,表现为抽搐、面部充血、口吐白沫、深昏迷,随后深部肌肉僵硬并迅速发展成全身高张阵挛惊厥,有节律的肌肉收缩和紧张,持续1~1.5min,期间患者呼吸动作停止。发作后抽搐停止、呼吸恢复、意识恢复,但患者易激惹和烦躁。
(3)妊娠合并慢性高血压:
是指既往存在高血压或在妊娠20周前发现收缩压≥140mmHg和/或舒张压≥90mmHg,妊娠期无明显加重;或妊娠20周后首次诊断高血压并持续到产后12周以后。
(4)慢性高血压并发子痫前期:
是指妊娠合并慢性高血压的孕妇,出现下列任一项:①孕20周前无蛋白尿,孕20周后出现尿蛋白≥0.3g/24h或随机尿蛋白≥(+);②孕20周前有蛋白尿,孕20周后尿蛋白定量明显增加;③出现血压进一步升高。
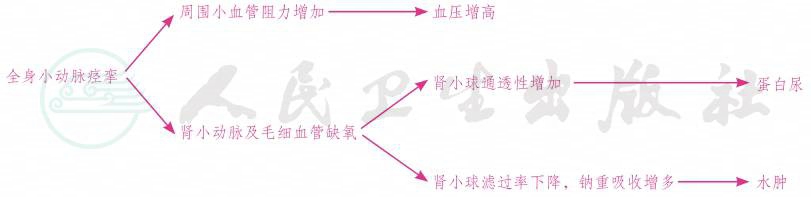
本病的基本病理生理变化是全身小动脉痉挛。由于小动脉痉挛,造成管腔狭窄,周围阻力增大,内皮细胞损伤,通透性增加,体液和蛋白质渗漏,表现为血压上升、蛋白尿、水肿和血液浓缩等。全身各组织器官因缺血、缺氧而受到不同程度损害,严重时脑、心、肝、肾及胎盘等的病理生理变化可导致抽搐、昏迷、脑水肿、脑出血、心肾衰竭、肺水肿、肝细胞坏死及被膜下出血,胎盘绒毛退行性变、出血和梗死,胎盘早期剥离以及凝血功能障碍而导致DIC等。主要病理生理变化简示如下:
1.应定期进行以下常规检查
(1)尿液检查:
应测尿比重、尿常规,当尿比重≥1.020时说明尿液浓缩。
(2)血液检查:
含全血细胞计数、血红蛋白含量、血细胞比容、血黏度,根据病情轻重可反复检查。血浓缩支持子痫前期的诊断,是疾病严重程度的指标。若合并有溶血的情况,血红蛋白降低,涂片可见破损的红细胞。血小板降低提示为重度子痫前期。
(3)肝功能测定:
肝细胞功能受损可致ALT、AST升高。胆红素检查不仅能反映肝脏损害的程度,而且对黄疸的鉴别具有重要意义。肝细胞损害引起的黄疸,因为同时有摄取、结合、排泄的障碍,因此直接和间接胆红素均可升高,但一般直接胆红素升高比间接胆红素升高的幅度大。乳酸脱氢酶升高提示存在有溶血。血清白蛋白降低说明内皮细胞渗漏的程度(低白蛋白血症),可出现白蛋白缺乏为主的低蛋白血症,白/球蛋白比值倒置。
(4)肾功能测定:
肾功能受损时,血清肌酐、尿素氮、尿酸升高,肌酐升高与病情严重程度相平行。血清肌酐升高尤其是合并有少尿时,提示重度子痫前期;尿酸在慢性高血压病人中升高不明显,因此可用于本病与慢性高血压的鉴别诊断。
(5)心电图检查:
了解有无心肌损害或传导异常以及可以发现高血钾或低血钾的波形变化。
(6)胎心监护:
胎儿电子监测,NST或宫缩刺激试验、缩宫素刺激试验。
(7)产科超声检查:
评价胎儿生长发育情况、多普勒脐动脉血流监测评价胎儿是否存在宫内缺氧。
2.子痫前期及子痫病人视病情发展和诊治需要,应酌情增加以下检查项目
(1)凝血功能测定:妊娠期高血压疾病的凝血功能的变化越来越受到重视,目前认为子痫前期-子痫处于高凝状态,称为易栓症。
(2)血清电解质测定:重度子痫前期与子痫冬眠合剂治疗,可导致出现低血钾;酸中毒时细胞内K+外游导致高血钾。
(3)腹部超声等影像学检查肝、肾等脏器及胸腹水情况。
(4)动脉血气分析:重度子痫前期与子痫应测定电解质与二氧化碳结合力,以早期发现酸中毒并纠正。
(5)超声心动图及心功能检查。
(6)超声检查胎儿生长发育、脐动脉、大脑中动脉等血流指数。
(7)眼底检查:视网膜小动脉可以反映体内器官的小动脉情况。视网膜小动静脉比例可由2:3变为1:2或1:3,且有反光增强、并可有视网膜水肿、有渗出物及视网膜剥离、亦可有点状或火焰状出血。
(8)必要时行X线胸片确定有无肺水肿,头颅CT或MRI检查确定有无颅内出血、脑水肿、可逆性后部脑病综合征。
妊娠期高血压疾病治疗的目的:预防重度子痫前期和子痫发生,降低母儿围产期病率和死亡率,改善围产结局。治疗时需综合考虑孕周、疾病的严重程度及治疗效果。终止妊娠是最有效的治疗措施,其他治疗手段只是缓解病情,为胎儿成熟赢得时间。
治疗基本原则是休息、镇静、预防抽搐、有指征地降压和利尿、密切监测母儿情况,适时终止妊娠。应根据病情的轻重缓急和分类进行个体化治疗:
(1)妊娠期高血压:
一般采用休息、镇静、对症等处理后,病情可得到控制,若血压升高,可予以降压治疗。
(2)子痫前期:
预防抽搐,有指征地降压、利尿、镇静,密切监测母胎情况,预防和治疗严重并发症,适时终止妊娠。
(3)子痫:
需要及时控制抽搐的发作,防治并发症,经短时间控制病情后及时终止妊娠。
(4)妊娠合并慢性高血压:
以降压治疗为主,注意预防子痫前期的发生。
(5)慢性高血压并发子痫前期:
兼顾慢性高血压和子痫前期的治疗。
对轻度妊娠期高血压疾病病人,应进行饮食指导并注意休息,以左侧卧位为主,加强胎儿监护,自数胎动,掌握自觉症状,加强产前检查,定期接受产前保护措施;对重度妊娠期高血压疾病病人,应使病人掌握识别不适症状及用药后的不适反应。还应掌握产后的自我护理方法,加强母乳喂养的指导。同时,注意家属的健康教育,使孕妇得到心理和生理的支持。
对预测发现的高危人群,可能有效的预防措施有:
1.适度锻炼
孕期适度锻炼,合理休息及饮食以保证孕期身体健康。
2.补钙
低钙摄入(摄入量<600mg/d)的孕妇建议补钙。每日内服1.5~2.0g。
3.阿司匹林
有子痫前期高危因素者,推荐使用阿司匹林抗凝治疗。用法:于妊娠11~13+6周,最晚不超过20周开始使用至36周,或者终止妊娠前5~10d每晚睡前口服低剂量阿司匹林100~150mg。













