规律的月经及排卵是女性性激素产生及生殖健康所必需的。随着女性年龄的增长,卵巢功能逐渐衰退,表现为卵巢储备功能下降和生育能力降低。20岁初期生育力达到高峰,37~38岁后开始急速下降,最终绝经来临标志着生殖寿命的终止。近年来,由于女性生育年龄的推迟、恶性肿瘤治疗手段的改善及带瘤生存期的延长,卵巢功能降低甚至衰竭的发生率显著增加,成为不孕症的常见病因之一。
初始卵泡池过小,卵泡耗竭加速或功能障碍都会导致卵巢功能减退和卵巢衰老。既往使用多个术语定义此病理生理过程,较常用的术语是卵巢早衰(premature ovarian failure,POF)、原发性卵巢功能不全(primary ovarian insufficiency,POI)和早发性卵巢功能不全(premature ovarian insufficiency,POI)。
1.卵巢早衰(premature ovarian failure, POF)
卵巢早衰是既往临床广泛接受和应用的专业术语,指女性40岁之前闭经,伴有FSH水平升高(>40IU/L)、雌激素水平降低等内分泌异常及不同程度围绝经期症状。POF在40岁之前女性发生率约为1%;30岁之前约为1‰;目前尚缺乏大样本中国人POF发生率的报道。针对POF尚缺乏可靠的指标预测其发生,确诊时卵巢功能多数已丧失;临床治疗棘手,无有效的措施改善卵巢功能,只能依赖激素替代治疗和供卵解决生育问题,严重影响患者的生活质量和家庭和谐。
近年来,随着病因研究的深入和临床病例的积累,国际学者认为“卵巢早衰(POF)”的概念存在明显的局限性。首先,“衰竭”顾名思义指卵巢功能完全衰竭,这一概念和诊断给患者造成巨大的精神压力和创伤,扰乱其生育甚至人生规划。其次,POF仅代表卵巢功能衰退的终末阶段,无法体现疾病的进展性和多样性。虽然POF是POI的终末阶段,临床发现不同于自然绝经,POF患者卵巢功能不是永久性、不可逆转性丧失。约50%的患者会出现间歇性卵泡发育和排卵现象,5%~10%的患者甚至在确诊多年后仍可自然妊娠,因此不是严格意义上的卵巢衰竭。
2.原发性卵巢功能不全(primary ovarian insufficiency, POI)
2008年经美国国立卫生研究院(NIH)和美国生殖医学协会(ASRM)会议讨论,提出用原发性卵巢功能不全(POI)替代POF的倡议。POI这一术语最初于1942年由著名内分泌学家Fuller Albright提出,强调卵巢功能障碍是导致POI患者闭经的原发因素,而非继发于下丘脑和垂体异常。POI概念的更新是对这一疾病更科学准确的诠释,代表不同严重程度的卵巢功能障碍的连续谱,揭示了疾病的本质特征。以基础FSH水平、生育能力和月经情况为参数,将POI疾病进程分为正常、隐匿期、生化异常期和临床异常期四个阶段(表1)。
表1原发性卵巢功能不全分期
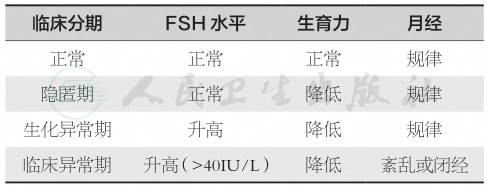
隐匿期FSH水平正常、月经规律,但生育力开始降低;生化异常期月经仍表现规律,但FSH水平开始升高,生育力显著降低;临床异常期是出现月经紊乱甚至闭经,FSH水平进一步升高,类似POF表现。也有学者将隐匿期和生化异常期合并,进而将POI分为“隐匿性原发性卵巢功能不全”(occult primary ovarian insufficiency,occult POI)和“临床性原发性卵巢功能不全”(overt primary ovarian insufficiency,overt POI)。POI对整个卵巢功能衰退过程的诠释更为全面,契合了疾病表型复杂、高度异质性的特征;同时也让临床医生更多关注POI早期表现,注重隐匿期和生化异常期患者的早期发现、早期干预和生育咨询。但是,关于隐匿期和生化异常期的诊断和FSH界定标准,国内外一直没有统一的标准,使临床医生对POI的早期诊断、对患者生育力的早期预警、预后评估仍存在困惑。
3.早发性卵巢功能不全(premature ovarian insufficiency, POI)
2015年欧洲人类生殖及胚胎学会(ESHRE)发布了“早发性卵巢功能不全的处理指南”(ESHRE Guideline Group on POI,2016)。该指南建议在基础研究和临床诊疗中应用早发性卵巢功能不全(POI)这一术语,并对POI重新进行了严格定义。早发性卵巢功能不全(POI)是指女性在40岁以前出现卵巢功能减退,表现为月经异常(闭经、月经稀发或频发),伴有促性腺激素水平升高、雌激素水平波动性下降,发生率约为1%。其诊断需同时具备月经异常和生化指标异常:月经稀发或闭经至少4个月;两次血清基础FSH>25U/L(间隔>4周)。2017年中国妇产科专家组制定的“早发性卵巢功能不全的临床诊疗中国专家共识”沿用指南中POI的定义和诊断标准,并将亚临床期POI的FSH诊断阈值界定为15~25IU/L。POI患者FSH诊断阈值的降低及亚临床期患者FSH阈值的界定,让早期阶段的患者得到充分的重视和必要的干预,同时亦增加了疾病的表型异质性。
POI正逐渐取代POF成为临床广泛接受和应用的术语。但针对于POI病因研究,卵巢功能衰退早期阶段患者的纳入,有可能增加病因的混杂性,进一步导致POI遗传学病因的异质性。此外,目前国内外均缺乏POI各阶段发生发展过程及持续时间的权威数据,仍有待于长期的随访观察和研究,以期为POI疾病转归、生育结局随访,以及远期并发症的防治提供循证医学证据。
POI是一种临床高度异质、病因混杂性疾病。研究资料显示染色体核型异常、基因突变、免疫性因素、代谢异常或药物作用、手术及放化疗损伤、病毒感染及环境污染物等都可能导致POI。这些因素可影响卵泡发育各阶段,导致始基卵泡池过小、卵泡募集异常,或影响卵泡闭锁、破坏加速,致卵泡过早耗竭,最终引起卵巢功能衰竭;但大多数患者病因不清,属特发性POI。
1.遗传因素
(1)染色体异常
染色体异常是POF最主要的遗传学病因之一,约占10%~15%。X染色体数目异常[45,X/46,XX和/或47,XXX]、X染色体部分缺失及X-常染色体易位是较常见的核型异常。最易发生X染色体缺失和易位的区域是POFl(Xq23-q27)和POF2(Xql3-q21)。起始于Xq13的染色体缺失多导致原发性闭经,而起始于Xq25或Xq26的染色体缺失所引发的临床表型较轻。位于Xq27.3的FMR1基因5′UTR动态突变与脆性X综合征和POI发生相关。FMR1前突变(CGG重复次数为55~200)携带者中13%~26%发生POI。由于FMR1基因5′UTR的CGG重复在传代过程中可发生动态扩增,前突变携带者的子代及其家族成员发生脆性X综合征的风险明显升高,因此,FMR1前突变检测不仅有利于发现POI病因,而且对其家族成员的脆性X综合征发病风险具有一定的预测价值。但值得注意的是,在中国汉族POI人群中,FMR1前突变的发生率仅为0.5%,提示FMR1前突变具有显著的地域和种族差异,并非中国汉族POI的主要遗传学病因,其临床检测价值有待进一步探讨。此外,由于参与卵巢功能维持的重要基因聚集于X染色体的关键区域,如DIAPH2、XPNPEP2、DACH2、POF1B和PGRMC1等,X染色体部分缺失导致的基因单倍剂量不足,染色体片段重排对邻近基因的“位置效应”及由此导致的减数分裂同源染色体联会异常可能引起卵子发生障碍及卵泡发育异常,进而导致卵泡闭锁加速,诱发POI。
(2)单基因突变
遗传因素导致的POI不仅发生在染色体水平,还可源于单基因突变。随着基因测序技术的发展和二代测序的广泛应用,已发现近90个基因通过不同作用机制和致病途径参与POI的发生,但是每种基因致病性突变在POI中的贡献度均不超过5%。
1)减数分裂相关基因
卵母细胞在胚胎期进入减数分裂,完成并停滞于第一次减数分裂前期的细线期,随后颗粒细胞包裹卵母细胞形成原始卵泡,构成女性生殖储备的基本单位。因此,第一次减数分裂前期的顺利完成对原始卵泡池的建立至关重要。第一次减数分裂前期的主要生理过程包括程序性双链DNA断裂(DSB)和同源重组修复(HR),已发现的POI致病基因不同程度地影响了以上过程:PRDM9和ANKRD31是重要的DSB形成基因,在一定程度上决定同源染色体的重组位置。中国汉族POI患者中首次发现PRDM9和ANKRD31杂合突变,并证实突变导致的单倍剂量不足可能通过DSB形成异常而影响减数分裂进程。此外,参与减数分裂同源重组的POI致病基因还包括:DSB末端修饰基因NBS1、EXO1、RECQL4和BLM;单链入侵基因DMC1、RAD51、BRCA2、BRCA1、PSMC3IP、XRCC2、MND1、MEIOB和HSF2BP;促进HR和Double Holiday Junction形成及稳定的基因SPIDR、MSH4、MSH5、MCM8、MCM9和HFM1。其中,基因DMC1、PSMC3IP、MEIOB、HSF2BP、SPIDR、MSH4、MSH5和HFM1均在生殖细胞减数分裂过程中特异性表达,基因缺陷导致单一表型POI,无其他躯体症状。其余HR基因由于同时参与体细胞DSB修复,其功能受损除了影响卵母细胞减数分裂,还往往导致其他体细胞DNA损伤积累,并由此引发细胞功能异常或凋亡。因此,突变携带者常伴发肿瘤、神经退行性疾病和皮肤损害等临床表现,称为综合征型POI,如NBS1隐性致病突变引发共济失调-毛细血管扩张症,BRCA2、MCM8和MCM9基因突变影响体细胞基因组稳定性,增加肿瘤易感性。此外,维持联会复合体结构稳定的基因SYCE1、C14ORF39和SYCP2L及控制姐妹染色单体之间连接的粘连蛋白复合体基因STAG3、REC8和SMC1B突变也参与POI的发生。值得注意的是,REC8和SMC1B基因缺陷可引起减数分裂时染色体不均等分离,产生非整倍体卵子,因此,该基因也是胚胎发育异常、反复胚胎种植失败及复发性流产的可疑病因。
2)范科尼贫血(FA)相关基因
范科尼贫血是一种罕见的基因组不稳定综合征,与骨髓衰竭、肿瘤易感性增加和严重的生殖障碍有关。已确定的FA蛋白有22个,协同参与S期DNA交联损伤修复和复制压力应答。FA基因缺陷雌性小鼠表现出不同程度生育力下降,其中多个小鼠模型出现原始生殖细胞(PGC)减少,提示FA通路可能参与调控PGC的基因组稳定性和卵巢储备建立。但目前为止,仅有5个FA基因被证实与POI相关,包括BRCA2/FANCD1、FANCM、FANCU/XRCC2、FANCA和FANCL。研究表明BRCA2、FANCM和XRCC2突变造成卵母细胞的减数分裂同源重组异常,但由于缺乏PGC表型的观察,并不能排除因PGC发育异常引起的卵巢储备下降。动物模型和体外实验表明FANCA和FANCL的杂合突变通过单倍剂量不足影响了细胞的交联损伤修复能力,提示FA基因突变对卵巢储备的影响可能是剂量依赖性的。此外,除BRCA2外,其他各研究中的突变携带者均未出现血液系统疾病或实体肿瘤,提示不同FA基因的特异位点突变可能存在表型差异,其机制尚待解析。
3)卵泡激活与卵泡发育相关基因
原始卵泡池建立之后,原始卵泡绝大多数处于休眠状态,进入青春期后在促性腺激素刺激下逐步激活形成初级卵泡。因此原始卵泡激活及卵泡发育的准确调控对于女性的生育寿命至关重要。在这一过程中,卵母细胞特异性的转录因子FIGLA、NOBOX、POU5F1、SOHLH1、SOHLH2和LHX8及颗粒细胞特异性转录因子FOXL2参与原始卵泡激活;NOTCH2介导卵母细胞与前颗粒细胞之间的信息交流;卵母细胞表达的转化生长因子TGF-β家族基因BMP15、GDF9和NOG通过旁分泌的方式调节颗粒细胞增殖;甾体激素合成基因FSHR、AMH、AMHR、INHA和KHDRBS1,转录因子NR5A1和BNC1及颗粒细胞分化调控基因WT1促进卵泡发育成熟。以上基因突变均不同程度地诱导卵母细胞凋亡和卵泡闭锁,参与POI发生。此外,自噬相关基因ATG7和ATG9突变通过单倍剂量不足效应导致卵母细胞和颗粒细胞自噬水平降低,加速卵泡丢失,也是POI的重要遗传致病因素。
4)能量合成及代谢相关基因
成熟卵母细胞是人体内线粒体含量最丰富的细胞,线粒体功能失调可引发氧化应激过度,导致卵母细胞及其周围体细胞凋亡,进而加速卵泡耗竭。目前发现的线粒体基因突变多导致综合征型POI,例如:POLG纯合或复合杂合突变导致进行性外眼肌麻痹(progressive external ophthalmoplegia,PEO)合并POI;HARS2、LARS2、CLPP、C10orf2和HSD17B4的 纯合或复合杂合突变导致Perrault综合征合并POI;AARS2纯合或复合杂合突变导致卵巢型脑白质营养不良综合征(ovarioleukodystrophies disease,OLD),表现为中枢神经系统退化和卵巢功能衰竭;RCBTB1纯合突变引发遗传性视网膜营养不良综合征(inherited retinal dystrophies,iRDs)合并POI。此外,部分基因突变也可导致单一表型POI,例如MRPS22纯合突变及POLG、GALT和PMM2杂合突变。
5)转录和翻译调控相关基因
母源mRNA的翻译和降解与卵母细胞减数分裂进程息息相关。CPEBl通过与靶基因mRNA 3′-UTR的CPE元件结合促进poly(A)尾的延长并启动蛋白翻译,是调控卵母细胞mRNA翻译的重要蛋白。目前通过微阵列-比较基因组杂交(aCGH)已至少发现7例原发或者继发性POI患者携带CPEB1基因缺失,而在中国人群POI的研究中发现,CPEB1基因杂合缺失的发生率仅为0.3%,提示CPEB1微缺失可能并非中国POI患者的常见遗传学病因。真核翻译启动因子EIF2B2和EIF4ENIF1是卵母细胞中高表达的翻译调控基因,其中EIF4ENIF1杂合无义突变参与家族性POI的发生,而EIF2B2基因纯合或复合杂合突变携带者多表现为OLD合并POI,但也有突变携带者仅表现为单一表型POI。
6)全基因组关联分析(genome-wide association studies, GWAS)和拷贝数变异(copy number variations, CNV)相关候选基因研究
近年来,GWAS和aCGH等技术也为寻找新的POI易感位点或候选基因提供了高通量、高效率的的筛查手段。GWAS是指基于人类全基因组范围内存在的单核苷酸多态(SNP),从中筛选出与疾病或性状相关的SNPs。2008年,Kang团队对韩国POI患者进行GWAS研究,发现相关位点7p14和候选基因PTHB1。高加索POI人群的GWAS研究发现ADAMTS19基因与POI存在显著关联,但该位点未能在另一独立荷兰人群中得到证实。中国汉族POI人群的GWAS研究发现了新的易感区域8q22.3。然而,POI发病率低,病例数偏少,基于POI的GWAS研究无法获得大量可靠的关联SNPs。自然绝经年龄(AANM)是一种连续性状,与早绝经(EM)和POI有共同的遗传易感因素。近期针对AANM和EM的大规模GWAS研究发现关联基因显著富集于DNA损伤修复通路,提示DNA损伤修复基因缺陷可能也是POI的重要致病机制)。进一步的多基因模型还提示POI不仅是一个孟德尔遗传疾病,也存在多基因遗传的倾向。
aCGH能以高分辨率检测全基因组范围内的1kb以上的大片段缺失或重复,寻找与POI相关的拷贝数变异(CNV)。2009年首次在99例法国POI患者中识别8个CNVs,发现5个与女性生殖相关的候选基因DNAH5、NAIP、DUSP22、AKT1及NUPR1。之后,通过联合X染色体芯片及SNP芯片等技术,中国、英国、德国、新西兰、美国、荷兰等多个国家相继发现与POI相关联的CNVs及可能的候选基因,所发现的候选基因可能影响减数分裂(如SYCE1、CPEB1、SGOL2等)和卵泡发育(如GDF9、BNC1等)的全过程。但CNV的研究结果仍然需要在另一独立群体中进行验证,并通过家系或对照研究,以及功能实验进一步证实其与POI的相关性。在最新一项研究中,Alexandar Rajkovic团队利用X染色体高分辨率aCGH比较了111名POI女性和269名生育力正常的对照女性的CNVs差异,研究结果显示,POI女性发生罕见CNVs的风险是对照女性的2.5倍,涵盖卵巢特异性表达基因,免疫应答基因和凋亡信号通路基因。此外,缺失片段也富集于X染色体失活逃脱区域,非编码RNAs和基因间DNA区域,提示POI和正常女性的X染色体存在结构差异。
(3)非编码RNA
非编码RNA(non-coding RNA,ncRNA)是一类不具备蛋白编码功能的RNA,包括转运RNA、核糖体RNA、微小RNA(microRNA,miRNA)、长非编码RNA(long noncoding RNA,lncRNA),以及环装RNA(circular RNA,circRNA)等。近年来,有学者发现内源性microRNA存在于哺乳动物的卵巢中,并且其表达模式随着卵泡发育过程动态变化,提示miRNA在卵巢功能维持中可能具有重要作用。已有研究表明,miR-146a、miR-23a、miR-379-5p、miR-21、miR-127-5p等多个miRNA在POI患者的卵巢颗粒细胞中差异表达。除了卵巢体细胞,miR-22-3p、miR-127-5p在POI患者外周血中也存在差异性表达,提示以上miRNA有可能成为POI的外周血诊断标志物。
LncRNA是一类长度大于200nt的RNA分子,已有研究在POI患者的卵巢皮质中发现了多个差异表达的lncRNA,且与其在外周血中的表达趋势一致,提示这些lncRNA分子也可能成为POI早期诊断的分子标志物。LncRNA参与POI发生发展的机制比较复杂,近年来多项研究发现在POI患者颗粒细胞中差异表达的lncRNA HCP5、GCAT1、PVT1、ZNF674-AS1等可能通过影响颗粒细胞的增殖、能量代谢、凋亡等生物学过程导致卵泡耗竭加速,参与POI的发生。
circRNA主要通过“分子海绵”样作用吸附miRNA,从而解除miRNA对其靶基因的抑制作用,间接提升靶基因的表达水平。有研究在POI患者颗粒细胞中发现了hsa_circ_003785等多个异常表达的circRNA,并且通过构建circRNA-miRNA-mRNA表达网络,发现其主要通过影响FoxO信号通路和细胞衰老通路导卵母细胞和颗粒细胞功能异常,导致POI发生。
2.免疫性因素
约5%~30%的POI与自身因素相关,因此认为POI是一种自身免疫性疾病或全身自身免疫性疾病累及卵巢后的表现,相关依据包括:伴发自身免疫性疾病、循环中存在自身免疫抗体和细胞免疫异常、自身免疫性卵巢炎的组织学表现等。但目前尚无自身免疫性POI的预测和诊断指标,自身免疫失调导致卵巢损伤和功能障碍的机制亦不明确。
POI常伴发或继发于其他器官特异性或非特异性自身免疫性疾病(表2),特别是多种内分泌腺自身免疫性疾病。甲状腺自身免疫异常(thyroid autoimmunity,TAI)是POI患者最常见的自身免疫疾病之一,在POI女性中发生率约为14%~27%,显著高于正常育龄期女性。而自身免疫性Addison病(Addison disease,AD)是与POI关联度最高的自身免疫病,有研究报道10%~20% AD伴发POI,多发生于伴发自身免疫性多腺体综合征患者,且其POI表型通常比肾上腺症状提前发生,可能与两者具备共同的类固醇生成相关抗原(17α-羟化酶和P450侧链裂解酶)有关。
表2与POI有关的自身免疫疾病

类固醇生成细胞抗体(StCA)是AD相关POI的敏感指标,其靶抗原包括17α-羟化酶17-OH和侧链裂解酶P450scc等。约>85%的AD伴发POI患者中出现StCA、17-OHAb、P450sccAb阳性;仅3%特发POI出现StCA阳性。而17-OHAb和/或P450sccAb仅在21OHAb阳性的伴发AD的POI患者中可检测到。有研究发现高StCA水平可预测AD发生POI的风险。此外,亦有研究发现POI患者血清中存在抗卵巢抗体、抗卵浆抗体、抗透明带抗体等,但不同研究结果异质性大,抗体特异性低,且其致病作用尚不明确,目前无一项能够证实自身免疫性POI的临床诊断。
此外,细胞免疫异常尤其是T细胞亚群失衡,亦可参与自身免疫性POI的发生。自身免疫性卵巢炎,尤其是StCA阳性POI患者卵巢组织学检査发现T淋巴细胞、浆细胞及巨噬细胞等大量炎性细胞的浸润,主要分布在较大的窦卵泡、排卵前卵泡及黄体阶段。POI患者外周循环和卵巢局部均存在TH(helper T cell)1型炎性反应亢进,促炎性细胞因子IFN-γ和TNF-α分泌增加;同时调节性T细胞(regulatory T cell,Treg)数量下降,免疫抑制功能受损,免疫调节因子TGF-β水平降低,POI患者存在TH1/Treg失衡。TH1炎性反应可引起卵巢颗粒细胞凋亡增加,雌激素合成障碍,导致卵巢功能不全。此外,也有POI患者自然杀伤细胞减少、杀伤能力下降,B细胞数量增加、抗体产生能力增强的报道。
3.医源性因素
近年来随着医疗手段的改善,乳腺癌、白血病、淋巴瘤及其他恶性疾病的生存率和治愈率显著提升,但放化疗导致的卵巢功能不全发生率亦增加。
放疗对卵巢的影响取决于放疗的范围,盆腔放疗发生POI的概率相对较高。同时患者年龄及放疗剂量也是重要风险因素。青春期前卵巢对放疗相对不敏感,当卵巢受到的直接照射剂量在0.6Gy以下时,卵巢功能几无影响,0.6~1.5Gy,对40岁以上妇女的卵巢功能有一定影响,1.5~8.0Gy,约50%~70%的15~40岁妇女可出现卵巢功能衰竭,放射剂量超过8Gy(800rad)时,所有年龄的妇女卵巢功能出现衰竭。放射线照射后,卵巢出现卵泡丢失,间质纤维化和玻璃样变,血管硬化和门细胞潴留,照射2周左右,血Gn水平开始上升。年轻妇女因卵泡数量相对较多,卵巢血运丰富,抗放射线损伤能力强于年长妇女,同等剂量的放射线照射,POF发生率相对较低。
化疗药物对卵巢的损害与患者年龄、化疗药物种类、剂量、用药长短相关。以烷化剂明显,如环磷酰胺、白消安、左旋苯丙氨酸、氮芥等属于高风险性腺毒性药物。此类药物不需细胞增殖即可发挥细胞毒性效应,所以可以破坏静止卵母细胞,甚至是始基卵泡的前颗粒细胞。化疗药物可通过影响卵泡成熟,促进始基卵泡耗竭而损害卵巢。而氨甲蝶呤等作用于分裂细胞的抗代谢药物及顺铂等类烷基化铂复合物,其性腺毒性相对较小。目前认为加用GnRH-a可降低化疗药物对卵巢的性腺毒性作用,但仍需循证医学的证实。
盆腔手术,如单/双侧卵巢切除术,卵巢楔切术、打孔术、囊肿剥除术、子宫切除术、子宫动脉栓塞术、输卵管结扎等,可能破坏卵巢血供或皮质,或引起炎症反应,对卵巢功能造成不可逆性损伤。临床观察发现术后1~5年是卵巢功能减退的高发期,有研究报道卵巢子宫内膜异位囊肿剥除术,尤其是双侧手术,术后AMH水平显著降低,卵巢功能受损,POI发生风险显著增高。
4.其他因素
吸烟或被动吸烟:大量流行病学数据显示吸烟女性绝经年龄较非吸烟人群提前1~2年。烟草中的二甲基苯丙蒽能够与颗粒细胞和卵母细胞的多环芳烃受体结合,激活促凋亡因子;另外尼古丁具有抑制芳香化酶的活性,影响雌激素的合成。烟草中的多环烃对生殖细胞有毒性作用,可导致卵泡耗竭。
此外,病毒或细菌感染也可导致POI发生。3%~7%的流行性腮腺炎感染者发生POI,乙型脑炎、腮腺炎病毒等均可损伤卵巢组织,既往也有免疫抑制患者患巨细胞病毒性卵巢炎的报道。长期服用抗类风湿药物如雷公藤也可能引起POI;环境中毒物、内分泌干扰物,如有机溶剂、杀虫剂、塑化剂、工业化学制剂等,及PM2.5长期暴露也可导致卵巢功能损害。













