1.直接扩散
浆液性乳头状囊腺癌直接蔓延扩散的机会较多,如腹膜、腹腔壁腹膜及腹腔脏器的腹膜,包括横膈、大网膜、小肠、直肠、子宫直肠窝、结肠、膀胱返折腹膜,以及输卵管和子宫的浆膜层等。约有2/3的患者合并有腹水,因而引起的症状已如前述,有的患者可能无任何不适,仅仅感觉腹部腹围增大。有无合并腹水与预后非常相关,近期报道Ⅲ及Ⅳ期卵巢癌无腹水的5年生存率较有腹水者可高出5倍。腹水的形成与淋巴管阻塞(主要是右侧横膈淋巴管)、腹膜受刺激,以及腹腔内液体流动不平衡等有关。癌细胞不仅可随液体流动而种植,而且腹壁穿刺放腹水的部位可出现穿刺部位癌瘤生长,形成皮下小结节或团块。有的患者因腹水误诊为结核性腹膜炎和肝硬化,在穿刺部位发生癌种植包块尚未能引起警惕。
2.淋巴转移
淋巴转移以卵巢浆液性乳头状癌发生率最高,较黏液性癌高。病理分级似影响不大,而临床分期有腹膜后淋巴结转移者即属Ⅲc期。盆腔淋巴结与腹主动脉旁淋巴结的转移率相似,Di Re等报道分别为29.0%及22.5%。横膈转移除直接种植外,也受淋巴引流阻塞的影响,局限于盆腔的卵巢癌横膈转移率为57%,超出盆腔时则达77%;有横膈转移者84.4%有盆腔淋巴结转移,而腹膜后淋巴结转移者55.9%有横膈转移。Petru进行37例左锁骨上淋巴结活检,仅1例临床可触及,其中32例为Ⅲ及Ⅳ期,Ⅲ期阳性率12%,Ⅳ期57%。
3.血行扩散
血行扩散过去认为肺及肝实质转移不多,但近期报道也非罕见,甚至手术、化疗至一定时间也有又出现转移者。1995年Geisler报道脑转移的发生率为3.3%。阴道转移发生较少。北京大学人民医院妇科肿瘤中心曾收治过卵巢浆液性乳头状癌患者,由外院转来时已行子宫及附件切除,入院后发现阴道断端有菜花状组织,病理证实为卵巢浆液性乳头状腺癌转移,也有可能系手术时癌细胞脱落种植形成。
包括浆液性腺癌、浆液性乳头状腺癌及浆液性乳头状囊腺癌。浆液性腺癌为米勒管型上皮的恶性肿瘤,其癌细胞常以形成囊腔和乳头为特征,但或多或少仍保留原来的组织形态。有的肿瘤形成大且不规则的小囊腔,有时上皮突入腔内形成上皮簇或乳头的倾向(图1)。
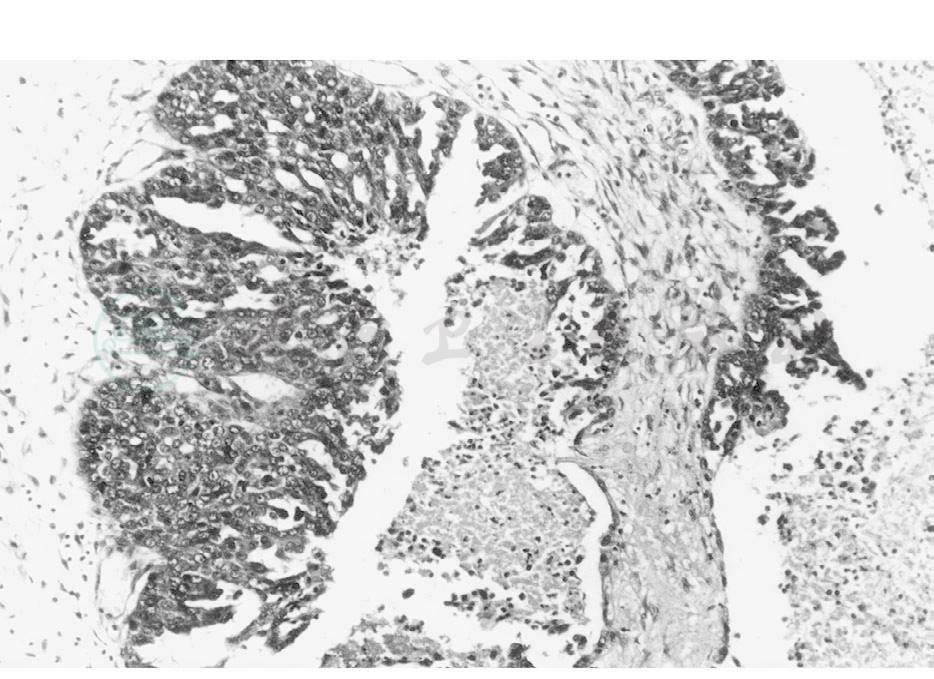
图1 卵巢浆液性乳头状囊腺癌
传统的形态学组织分级分为三级:
(1)高分化(Ⅰ级)
上皮增生4层以上,异型性明显。大部分有乳头,乳头分支极细,乳头的上皮间变明显。有时上皮增生堆积,复制成大量新的小腺体。在乳头或间质内可见砂粒体。
(2)中分化(Ⅱ级)
有乳头状结构,但形态怪异,呈手指状或簇状。部分区域为腺管状或筛状,小部分为实质性细胞团。细胞异型性大,分化差,分裂象多。
(3)低分化(Ⅲ级)
乳头状结构消失,肿瘤细胞呈实质性片状或团块状,即实质性腺癌。细胞异型性大,分裂象多,间质极少。
根据新的基于分子生物学改变和肿瘤细胞的生物学行为的分级则分为Ⅰ型和Ⅱ型,Ⅰ型起源于恶性潜能未定的浆液性瘤,而Ⅱ型则发展快,没有经过交界的过程。Ⅰ型通常低级别,高比率的Ras基因通路突变,大约35%的高分化浆液性癌有KRAS基因突变。超过30%的低级别浆乳癌中有BRAF基因的突变,这两种突变均可激活MAP激酶通路及其下游的基因。这两种突变都未在高级别的浆液性乳头状囊腺癌中发现。此外,Ⅰ型肿瘤中很少TP53突变。而Ⅱ型则高TP53突变,很少Ras基因突变。高级别的浆液性卵巢癌导致的死亡则占到所有卵巢癌相关死亡的2/3。在所有亚型当中,只有高级别内膜样癌和高级别浆液性癌分子改变相似。
根据患者肿瘤经手术及病理明确临床分期(FIGO),考虑年龄和对生育的要求决定手术方式。保留生育的卵巢癌分期手术包括患侧附件切除术及全面的手术分期,保留生育能力的手术则限于年轻有生育要求并且应当经过全面分期后证实没有卵巢外的转移播散的早期卵巢癌患者。保留子宫及对侧卵巢应当限于Ⅰa期,并且G1和G2的患者。尽管盆腔和腹主动脉旁淋巴结的切除术对于早期卵巢癌患者的生存是否有意义一直还存在争议,但FIGO明确的分期需要了解有无盆腔及腹主动脉旁淋巴结有无转移。
除Ⅰa G1可行保守性手术外,其余则应按卵巢癌FIGO分期手术并辅以化疗。包括:子宫全切、双附件切除术、大网膜切除术、淋巴结切除术、阑尾切除术、腹膜活检及腹腔冲洗液的细胞学检查。对于晚期EOC,手术包括初次肿瘤细胞减灭术(primary cytoreductive surgery)及其后的辅助化疗。对于Ⅲ期和Ⅳ期的患者不需要细胞学的评估,但所有腹膜表面,包括膈面、盆腹腔器官的浆膜面、整个胃肠道的系膜均应当进行仔细检查有无种植病灶,并应仔细检查大网膜并切除大网膜。一部分晚期患者会有上腹部大块的肿瘤转移灶,如果需要,可进行脾切除、胰尾切除、肝切除,及切除门静脉部位的病灶、胆囊切除、全结肠切除、盆腔腹膜切除及膈面病灶去除,以获得满意的肿瘤细胞减灭术。最近有研究显示在手术技术改善后对于Ⅳ期患者进行上腹部根治性手术并达到满意的肿瘤细胞减灭术后可以提高患者的生存率。在卵巢癌几项预后因素中,残存病灶大小是唯一可以通过医者的能力而改善争取的。但值得注意的是,手术的并发症不应当影响患者的术后化疗,因为手术后化疗的敏感与否则是最重要的预后因素。
二次大战后化疗药物的应用显著改善了卵巢癌这一致命疾病的预后,20世纪90年代顺铂的发现更使卵巢癌的生存率得到了显著的提高,到90年代末期,顺铂+紫杉醇的联合应用成为治疗EOC的标准治疗。经过上述满意的肿瘤细胞减灭术和6~8个疗程的一线化疗,许多晚期患者能达到完全缓解,但其中会有3/4的患者会复发,局部复发的卵巢癌患者应当考虑再次手术治疗,文献报道再次手术治疗可以获得6~12个月的无瘤生存期,而孤立的肝转移、腹腔外转移(包括肺转移、脑转移)也可以通过再次手术获益。
对于部分晚期卵巢EOC,在术前评估时考虑的手术难以切除,或难以达到满意的肿瘤细胞减灭术后,可以考虑新辅助化疗(neoadjuvant chemotherapy,NACT)。NACT指在经细胞学或组织学诊断后,对于难以完成满意的肿瘤细胞减灭术的患者应用化疗。这一过程最早在1979年应用于耶鲁大学。在Bristow等的荟萃分析中包括了6885晚期卵巢癌患者,仅42%达到了满意的肿瘤细胞减灭术,仅有少数患者达到肉眼无残留。最近的一项GOG试验也显示在Ⅲ期患者中只有23%的患者和Ⅳ期患者中只有8%的患者能达到肉眼无残留。NACT能显著提高肿瘤切除率,降低手术并发症。Kang和Nam荟萃21项研究,得出结论NACT患者更能获得满意的肿瘤细胞减灭术率,似乎增加中位生存时间,但差异并不显著。













