中文别名 :宫颈内膜腺体异型(非典型)增生和原位腺癌;宫颈腺体上皮内肿瘤
2014年,第4版WHO分类将原位腺癌(adenocarcinoma in situ,AIS)列入宫颈腺性肿瘤癌前病变,这一病变是指宫颈腺上皮呈现恶性表现,如果不进行治疗,具有进展为浸润性腺癌的风险。可以接受的同义词为高级别宫颈腺上皮内病变(High-grade cervical glandular intraepithelial neoplasia,HG-CGIN)。由于宫颈腺性病变与鳞状病变不同,具有一定比例的宫颈腺性病变与HPV感染不相关。在2020年,第5版WHO分类中,对于AIS进一步分为HPV相关性AIS和非HPV相关性AIS,后者常显示胃型分化,与HPV感染无关。
宫颈上皮内病变与HPV感染、过早开始性生活、多个性伴侣或高危性伴侣、有性传播疾病感染病史、多产、口服避孕药、吸烟等因素相关。
1.HPV感染
几乎所有的宫颈上皮内病变都与HPV感染有关。大多数HPV感染不会引起症状或疾病,并在感染后12~24个月内被清除,5%~10%HPV感染发生持续性感染,仅1%~4%最终发展为癌前病变和浸润性癌。
(1)HPV
人乳头瘤病毒(HPV)是一种嗜上皮组织的无包膜双链环状小DNA病毒,由病毒蛋白衣壳和核心单拷贝的病毒基因组DNA构成。编码的蛋白包括来自病毒基因组早期区的6个非结构蛋白(E1、E2、E4、E5、E6和E7),以及来自基因组后期区的两个结构性病毒衣壳蛋白(L1和L2)。
E1和E2基因可调控病毒基因组复制。E4基因编码的E4蛋白与病毒颗粒的组装及释放有关。E5基因与致癌潜力相关,在高危型HPV病毒中,E5蛋白干扰病毒抗原的递呈,逃避免疫监视,是HPV持续性感染的重要因素之一。而晚期区所编码的主要衣壳蛋白L1和次要衣壳蛋白L2起包装病毒DNA的作用,是HPV感染人体时首先与上皮细胞相互作用的结构。E6和E7基因是癌变过程的启动因素。高危型HPV的E6和E7蛋白在宫颈癌组织内持续性表达,是致癌的关键分子。E6和E7癌蛋白分别抑制肿瘤抑制基因p53和pRb活性,从而降低细胞染色体的稳定性并诱导细胞永生化。
到目前为止,已经发现了200多种HPV基因型。根据致癌潜力,分为高危型和低危型。低危型HPV与生殖器疣和其他良性病变有关,包括HPV 6、11、42、43和44等;高危型HPV主要与宫颈上皮内病变和宫颈癌相关,包括HPV16、18、31、33、35、39、45、51、52、56、58、59、66和68。70%左右的宫颈癌是HPV 16或18感染所致。
(2)HPV感染的流行病学
HPV在生殖器和肛门的感染主要与年龄及性行为习惯相关。性活跃的年轻妇女感染率最高,感染的高峰年龄为15~25岁。年轻女性的HPV感染及其引起的宫颈低级别病变的频率很高,并可反复感染或同时感染多种型别的HPV,但绝大多数都会在短期内自动消失。30岁以上女性中宫颈HPV感染率有所下降,但是HPV持续性感染的风险随着年龄增长而增加。因此,建议21岁以上有性生活女性定期进行宫颈癌筛查,主要目的是发现可能进展为宫颈癌前病变(HSIL和AIS),并进行有效治疗阻断其发展。
2.性生活
宫颈上皮内病变与过早开始性生活、多个性伴侣或高危性伴侣、有性传播疾病感染病史、免疫功能低下等相关。首次性生活年龄小于16岁与HPV感染,特别是高危HPV 16和18型感染有显著关系。青春期女性宫颈转化区发生柱状上皮异位,转化区未成熟的化生鳞状上皮细胞代谢活跃,与较晚开始性生活的女性相比,首次性生活年龄较小的女性更易感染HPV,且感染发生后更易持续,可能持续暴露于HPV感染的时间也更长。
研究发现,女性感染HPV的风险随着最近6个月和一生中男性性伴侣的数量增加而增加,且更易感染高危型HPV。此外,女性感染HPV的风险在很大程度上取决于其男性性伴侣的性行为。例如:男性伴有多个性伴的女性HPV阳性率是男性单性伴的1.5倍。
性传播疾病感染史,包括人类免疫缺陷病毒(HIV)、单纯疱疹病毒、淋病奈瑟菌、沙眼衣原体和阴道毛滴虫,以及免疫功能低下(如自身免疫性疾病、器官移植后或免疫缺陷疾病如HIV感染)与机体HPV清除能力下降或生殖道HPV易感性增加有关。
3.早产多产
研究显示,在持续感染HPV的妇女中,分娩次数越多,发生高级别宫颈上皮内病变的风险就越大。特别是对于高龄高胎次的妇女,HSIL更容易进展。此外,首次足月妊娠的年龄与CIN3/原位癌有关。妊娠期由于高水平雌孕激素刺激以及与分娩有关的宫颈创伤,促宫颈柱状上皮外移,暴露于HPV或其他辅助高危因素。
4.长期口服避孕药
长期口服避孕药也是危险因素之一。正在使用口服避孕药的妇女与从未使用过或过去使用过激素避孕药的妇女相比,发生高级别CIN的概率增加了约50%,且CIN2,CIN3的发生风险随着使用时间的增加而增加。服用避孕药5年或以上者患浸润性宫颈癌和CIN3/宫颈原位癌的风险增加约一倍,并在停止使用后下降。
5.吸烟
吸烟可增加宫颈上皮内病变发生风险。吸烟者患高级别CIN的风险高于不吸烟者,且随着每天吸烟量和吸烟时间的增加而增加。烟草代谢物引起的局部免疫抑制作用,不利于宿主对病毒感染产生有效免疫反应,从而增加宫颈持续感染的风险。此外,烟草所含的化学物质,如尼古丁及其代谢物可替宁,可引起鳞状上皮细胞DNA损伤,女性吸烟者的宫颈黏液中发现尼古丁及其主要代谢物可替宁的水平较血清增加4倍。
由于病变主要位于宫颈管,AIS很难通过阴道镜发现病变。多数AIS是局灶性的,但大约有13%~17%的病例为多灶性,少数病例可以呈跳跃性。因此,临床活检时,宫颈管内膜的搔刮对于排除AIS及腺性肿瘤非常重要。
几乎所有的AIS均累及宫颈表面上皮和腺体。正常腺体结构尚保存,HPV感染相关性AIS黏膜上皮或腺腔上皮被覆核大、深染且有核仁的恶性细胞,细胞核分裂活性增加,胞浆内黏液减少,病变上皮细胞与正常腺上皮细胞之间可见转化(图1 A),非HPV相关性胃型AIS,包括非典型小叶状增生,腺体呈现小叶状增生,细胞胞浆嗜酸性或淡染,细胞核有异型(图2)。免疫组化染色:HPV感染相关性AIS,p16常呈弥漫强阳性表达(图1 B)。Ki-67:呈高表达。ER和PR表达有明显丢失。而非HPV相关性AIS,p16一般呈现阴性,但同样可显示ER和PR表达丢失。
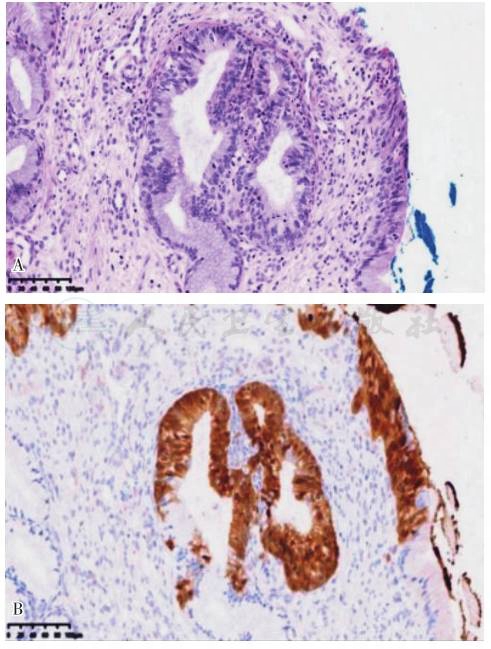
图1宫颈原位腺癌(HPV感染相关性)
A.宫颈部分黏膜腺体被具有恶性细胞学表现的上皮所替代;B.免疫组化染色显示:宫颈黏膜腺体中的异型细胞呈现p16弥漫强阳性。
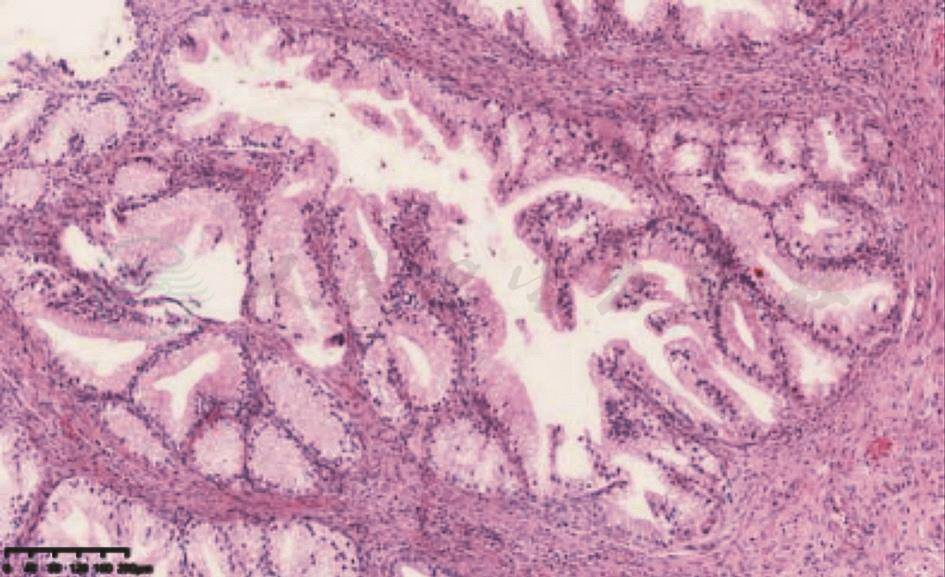
图2宫颈非HPV相关性原位腺癌
可见宫颈腺体呈现小叶状增生,腺泡排列密集,腺腔大小不等,部分腺腔内可见乳头结构,细胞胞浆透亮,呈现胃幽门腺化生,部分细胞核增大,移向腺腔面。
对于需要保留生育功能的AIS患者可以采用Leep手术或锥切手术治疗,但是对于术后标本的评估很重要,如果切缘阳性,则复发的风险明显增高。即使切缘阴性,文献报告仍有10%~15%的复发概率。因此,保守治疗后的患者,应密切行细胞学、HPV以及阴道镜随访。对于已经完成生育的妇女建议行子宫切除术。













