英文名称 :age-related macular degeneration
中文别名 :老年性黄斑变性
年龄相关性黄斑变性(age-related macular degeneration,AMD)患者多为50岁以上,双眼先后或同时发病,视力呈进行性损害。该病是60岁以上老年人群视力不可逆性损害的首要原因。其发病率随年龄增加而增高。
确切病因尚未明了。可能与遗传因素、黄斑长期慢性光损伤、代谢及营养因素等有关。
1.AMD的分期
该病的早期改变主要为黄斑区的软玻璃膜疣(drusen),玻璃膜疣存在于视网膜RPE和Bruch膜之间,呈黄或白色的细胞外物质的沉积物,正常人40岁后出现小的玻璃膜疣是正常的。但是大的和数量较密集的玻璃膜疣常常是AMD的早期改变。中等大小(63~ 125μm之间)和大的(≥125μm)玻璃膜疣(中期AMD),大约18%在5年内发展为进展型(晚期)AMD。表1显示玻璃膜疣的范围和色素异常对5年后发展为进展型AMD的影响,任何色素异常,无论色素多少伴有中等度大小的玻璃膜疣,5年内发展为进展型的可能性很低,约50%~60%进展型AMD患者发生严重视力下降。
2013年的国际黄斑病专家组对AMD分期的玻璃膜疣直径做了分析,对出现在黄斑区2个视盘直径(disc diameter,DD)内的病变推荐了下述新的分期(表2)。
表1AREDS参与人员按照玻璃膜疣大小和色素异常程度在5年中发展为进展期AMD的比例
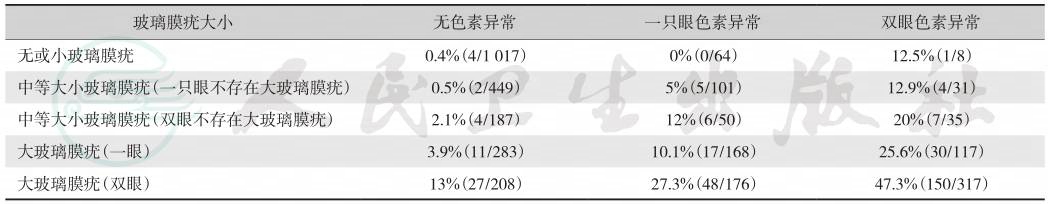
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
表22013年的国际黄斑病专家组AMD分期

注:AMD相关色素异常:任何明确的色素脱失或色素沉积,且与中等大小玻璃膜疣或大玻璃膜疣相关,而不与其他已知疾病相关
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
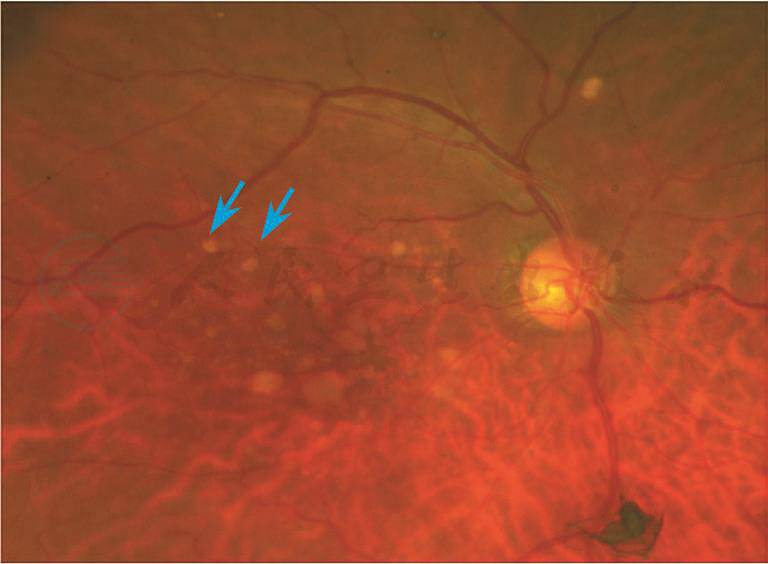
图1中期AMD,玻璃膜疣>125μm(蓝色箭头)
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
(1)无年龄性改变
无玻璃膜疣、无RPE异常。
(2)正常年龄性改变
仅有小的玻璃膜疣(≤63μm)。
(3)早期AMD
玻璃膜疣65~125μm,无RPE异常。
(4)中期AMD
任何≥125μm的玻璃膜疣,任何中心凹2个视盘直径内的 RPE 异常(图1)。
(5)晚期AMD
包括新生血管性AMD和/或任何地图样萎缩。新生血管性AMD包括各种类型的新生血管膜、渗出性或出血性神经上皮 / 色素上皮脱离,纤维血管性盘状瘢痕。
专家组在分类中提到根据较新的测量技术,视盘直径应为1800μm而不是以往的1500μm,以此为标准原来(AREDS)的早期小的玻璃膜疣63μm计算为75μm更合适,同样可以将中等度玻璃膜疣125μm调整为150μm。中国AMD的临床路径将AMD分期的路径表述如下(图2)。
上述分期指导了AMD的早期干预(见下述)。
玻璃膜疣在FFA的动静脉期比检眼镜下容易看到,Gass认为基底膜玻璃膜疣(basal laminar drusen)是RPE基底膜的增厚,不同分布、大小一致的小的圆形、稍隆起的玻璃膜疣,通常25~75μm,可见于成年人,常常数量较多,成堆,基底膜玻璃膜疣的FFA染色差。50岁后基底膜玻璃膜疣可以发展为大小不一致的、渗出性玻璃膜疣,累及中心凹部,有的可看到单眼或双眼黄斑部黄色渗出性脱离,常导致中心视力下降,脱离区玻璃膜疣消失,液体吸收后RPE地图样萎缩,有些患者发生脉络膜新生血管膜。
2.AMD的分型
非渗出性AMD与渗出性AMD、干性与湿性AMD:AMD是由黄斑区新生血管、视网膜色素上皮细胞(RPE)和神经上皮退行性变引起的不可逆性视力下降或视力丧失。以往将有玻璃膜疣、色素异常和地图样萎缩的AMD称作干性AMD(dry AMD)或非渗出性 AMD(non-exudative AMD),而将有黄斑新生血管、RPE脱离或盘状纤维化的AMD称为湿性(wet AMD)或新生血管性AMD(neovascular AMD)或渗出性AMD(exudative AMD)(图3、图4)。2014年的AMD分类经过全球专家讨论,调整了干性AMD的定义,将大于65μm的玻璃膜疣定为早期改变,干性和湿性均为进展期AMD(晚期AMD)改变,“干性”特指地图样萎缩(geographic atrophy,AG),“湿性”特指新生血管性AMD。湿性AMD包括视网膜色素上皮脱离(pigment epithelial detachment,PED)和脉络膜新生血管膜的各亚型,而新生血管性AMD常常指脉络膜新生血管膜,包括经典为主型、隐匿型、微小经典型,不包括PED。

图2我国年龄相关性黄斑变性的分期
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
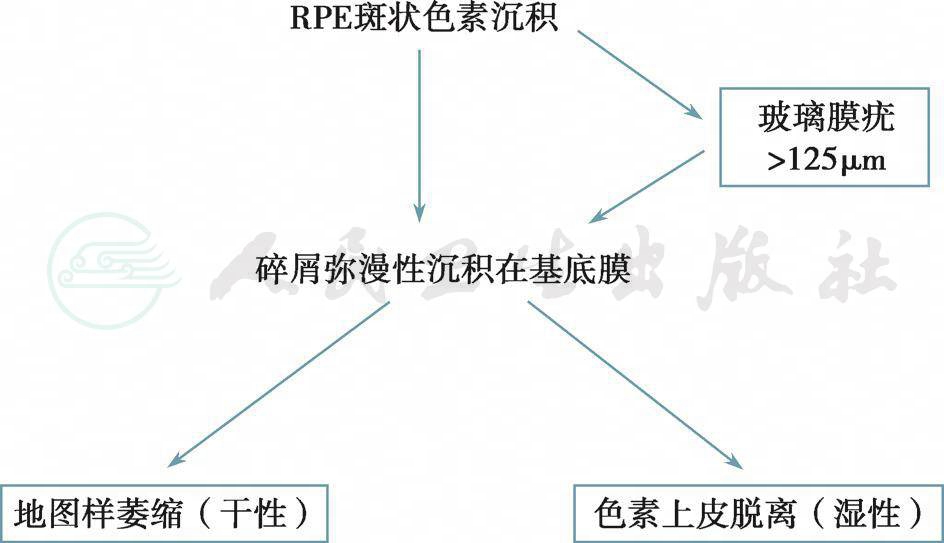
图3非渗出性AMD早期进一步发展示意图
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
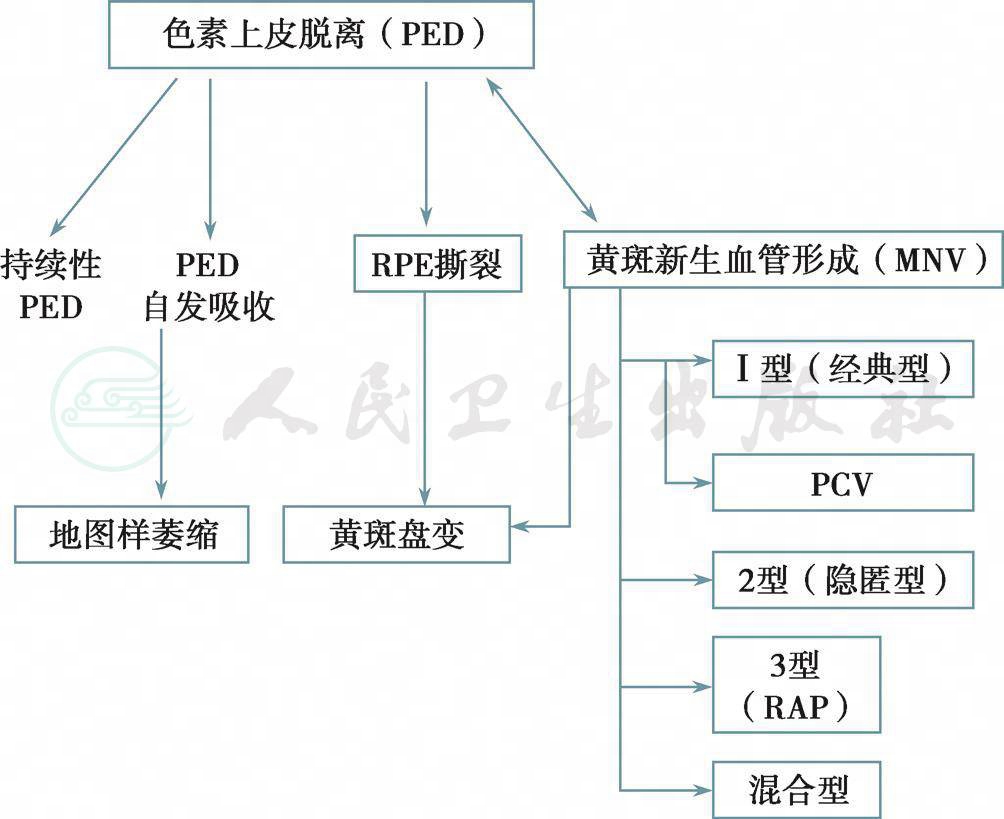
图4非渗出性和渗出性AMD(新生血管性AMD)
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
眼科基本检查应包括视力、眼压、裂隙灯和眼底检查,眼底检查可以使用裂隙灯生物显微镜联合前置镜或眼底检查镜,一般在散瞳下进行。针对新生血管型AMD的特殊检查应包括眼底荧光血管造影(FFA),吲哚菁绿血管造影(ICGA),光学相干断层扫描(OCT)。
对萎缩性病变和视力下降可行低视力矫治。软性玻璃膜疣可行激光光凝或微脉冲激光照射,可促进吸收。对湿性AMD,目前临床上最主流的治疗方法是玻璃体内注射抗VEGF药物,通过抑制VEGF发挥作用,疗效确切,目前已用于临床治疗的药物有Conbercept(康柏西普)、Ranibizumab(雷珠单抗)、Aflibercept(阿柏西普)。抑制新生血管的药物还有糖皮质激素,包括曲安奈德(triamcinolone acetonide,TA)和乙酸阿奈可他(anecortave acetate),它们主要通过抑制血管内皮细胞移行发挥作用。但这些药物仍未能解决复发问题,需要多次注射。对于中心凹200μm外的典型性CNV,可行激光光凝治疗。光动力疗法(photodynamic therapy,PDT)、810nm红外激光经瞳孔温热疗法(transpupillary therapy,TTT)可使新生血管内皮细胞产生细胞毒损伤,破坏新生血管组织,对病灶周围的视网膜影响较小,有利于保留视功能,但上述激光疗法均不能解决CNV复发问题。黄斑手术治疗包括清除视网膜下出血、去除CNV及黄斑转位术,治疗效果有待进一步评价。对PCV,PDT联合玻璃体内注射抗VEGF药物是目前最有效的疗法。对黄斑中心凹外的息肉样病灶可行激光光凝。
黄斑变性的发生可能与光的毒性蓄积作用有关,故应避免光损伤,在强光下活动应佩戴遮光眼镜。近年有应用激光治疗玻璃体疣防止进一步演变形成老年性黄斑变性的报道,尚需进一步观察疗效。













