英文名称 :tropical spastic paraparesis
中文别名 :嗜T淋巴细胞性病毒相关性脊髓病
热带痉挛性截瘫(tropical spastic paraparesis,TSP)是人类嗜T淋巴细胞病毒-Ⅰ型(human T-lymphotropic virus type-Ⅰ,HTLV-Ⅰ)感染导致慢性进行性自身免疫疾病,又称HTLV-Ⅰ相关脊髓病(HTLV-Ⅰ associated myelopathy,HAM)。神经系统HTLV-Ⅰ感染引起的炎症性疾病早年在日本称为HTLV-Ⅰ相关脊髓病,在加勒比地区称为热带痉挛性截瘫。从病原学及临床角度看,这两种疾病是同一疾病在世界不同地区的不同称谓而已。由于HAM与TSP是同一疾病,在鹿儿岛举行的WHO会议(1988年)上被统一命名为HAM/TSP。
美国学者Gallo等(1981)在T淋巴细胞肿瘤当中首次分离出HTLV-Ⅰ,它属于反转录病毒科C型病毒。Gessain等(1985)首次在TSP患者的血清和脑脊液中检出HTLV-Ⅰ抗体,认为该病可能与HTLV-Ⅰ相关。随后有学者在患者脑脊液、淋巴细胞培养中找到了HTLV-Ⅰ抗原,更有学者在患者神经组织内发现了HTLV-Ⅰ颗粒。目前,已经确认HTLV-Ⅰ是该病的病原体,HTLV-Ⅰ为正链单股RNA病毒,具有包膜,直径约100nm。病毒颗粒外覆的脂蛋白双分子层包膜来源于宿主细胞膜,其上有病毒表面蛋白及跨膜蛋白。包膜内部的二十面体衣壳保护着由病毒RNA、功能性蛋白酶、反转录酶以及整合酶组成的核糖核蛋白复合体。HTLV-Ⅰ具有嗜人类淋巴细胞和神经组织的双重特性,密切的性接触是HTLV-Ⅰ的主要传播途径,其次是母婴之间的垂直传播和输入HTLV-Ⅰ污染的血液制品。居住环境较差也是感染和传播HTLV-Ⅰ的重要条件。
近年来有关该病的报道逐年增多,至1991年文献报道病例达1 150例。HAM/TSP有一定地理分布,主要在北美洲加勒比海沿岸的哥伦比亚、牙买加等地,牙买加发病率为12/10万,年发病率为0.6/10万。日本也有发现,日本Kynshu岛发病率为5/10万,年发病率为1.0/10万。我国台湾1991年报道首例HAM,福建、汕头地区亦有报道。
本病发病机制迄今不清,曾认为可能是HTLV-Ⅰ直接侵袭神经组织,但神经元内未分离出病毒。目前认为HTLV-Ⅰ感染改变自身组织抗原性,在神经组织引起自身免疫反应,以细胞免疫为主,引起相应症状,证据为患者外周血和脑脊液抗HTLV-Ⅰ抗体效价增高、鞘内免疫球蛋白合成增加、脑脊液检出寡克隆带及皮质类固醇治疗有效等。
脊髓病变主要在胸髓,其次是腰髓,脊髓萎缩、变扁,软脊膜增厚、灰白质界限不清。镜下可见慢性软脊膜脊髓炎征象,血管周围炎性细胞浸润形成袖套样。受累最重的是侧索,尤其是皮质脊髓束,其次是前索,表现为髓鞘脱失、空泡形成、轴索崩解及再生,侧索胶质细胞增生最明显,表现空泡形成、髓鞘脱失、轴索崩解及胶质细胞增生等(Matsuura,2010)。腰段改变轻于胸段,类似华勒变性。视神经也可见髓鞘脱失及炎性细胞浸润。
免疫细胞化学染色可见脊髓血管周围及实质内弥漫性浸润的炎性细胞及T淋巴细胞,抑制性或细胞毒性T细胞CD8+占绝大部分(Martin,2011)。
1.脑脊液检查
(1)CSF细胞数增多,(10~50)×106/L,以淋巴细胞为主,蛋白轻中度增高,糖含量正常;大部分患者CSF可检出寡克隆带,可用放射免疫或ELISA检测血清和脑脊液HTLV-Ⅰ特异性抗体。
(2)CSF存在新蝶呤(neopterin)可作为本病的辅助诊断指征,新蝶呤是CSF中T淋巴细胞激活后释放。以血清学为基础的试验包括间接免疫荧光法及免疫印迹法(Romanelli,2011),目前确诊HTLV-Ⅰ感染主要通过PCR,多数PCR引物针对的是基因组最保守的部分即tax基因。实时定量PCR甚至能对前病毒定量。前病毒载量被定义为一定数量的外周血单个核细胞中HTLV-ⅠDNA的拷贝数。当前病毒载量>1拷贝/100外周血单个核细胞时,HAM/TSP发病风险随前病毒载量对数呈指数增加。HAM/TSP患者中位数HTLV-Ⅰ前病毒载量为无症状HTLV-Ⅰ携带者的10倍,快速进展的HAM/TSP患者HTLV-Ⅰ前病毒载量较缓慢进展HAM/TSP高。CSF中HTLV-Ⅰ前病毒载量与外周血HTLV-Ⅰ前病毒载量之比与临床症状进展及新近发生的HAM/TSP密切相关(Hayashi,2008)。因此,外周血HTLV-Ⅰ前病毒载量是罹患HAM/TSP风险及病情进展的重要指标。HTLV-ⅠmRNA载量是与HAM/TSP患者疾病严重程度相关的另一个指标。
2.电生理检查
(1)视觉诱发电位(VEP):
大多数病例出现异常,单侧或双侧P100潜伏期延长,伴波幅降低。
(2)体感诱发电位(SEP):
可发现髓内传导阻滞。
(3)脑干听觉诱发电位(BAEP):
波间潜伏期轻或中度延长,偶见单个波幅降低或消失。
(4)肌电图及周围神经传导速度(NCV):
多正常,伴多发性神经病患者可有轻度神经源性损害。
3.影像学检查
脑CT多无异常。MRI检查可见大脑半球深部脑室周围白质散在的大小不等斑片状异常信号灶,T1WI呈均匀低信号,T2WI为明显高信号,无明显占位效应,少数病例脑干、小脑有异常信号,受累脊髓节段变细(Morgan,2007)(图1)。脊髓MRI出现T2WI高信号,提示HAM/TSP为快速进展期,临床表现为严重的运动功能受累(Yukitake,2008)(图2),MRI检查正常并不能除外HAM/TSP。
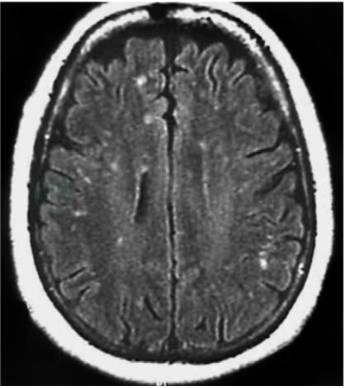
图1HAM/TSP患者脑 MRI检查,在 Flair像可见大脑局灶高信号病变
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
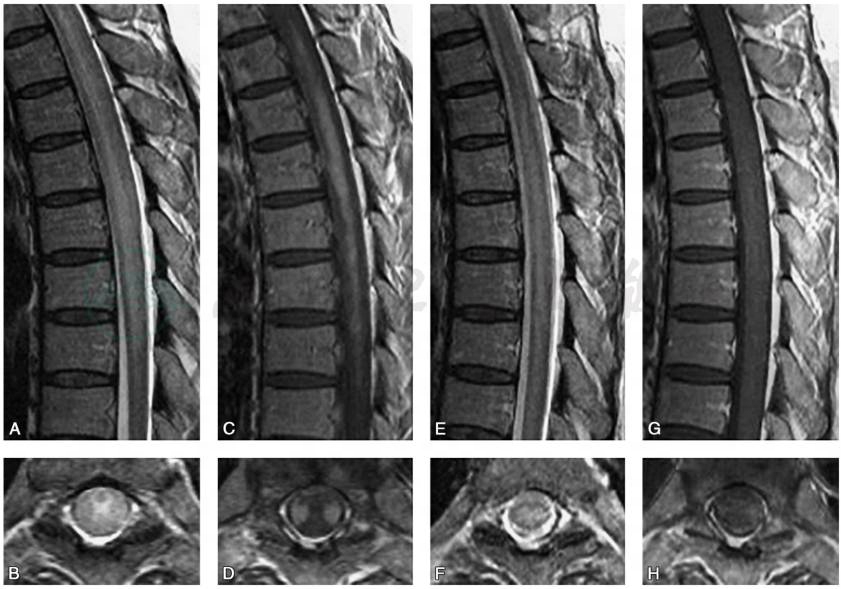
图2患者女性,58岁,发病12个月后脊髓MRI检查
A.T2WI矢状位可见脊髓中央部高信号;B.与A对应的轴位像;C.Gd-DTPA增强后矢状位的T1WI;D.与C对应的轴位像,可见T4~T9双侧皮质脊髓束增强;E、F.治疗后3周的T2WI矢状位及其对应的轴位像;G、H.Gd-DTPA增强后矢状位及其对应的轴位像,可见治疗后增强的病灶消失
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
1.目前本病尚无有效疗法,主要采用对症治疗,抗痉挛药盐酸乙哌立松、氨氟喹酮等可改善行走,α-肾上腺能阻断药盐酸哌唑嗪可使尿道压力下降,改善排尿困难。
2.免疫调节及抗炎途径主要是抑制免疫激活,特别是抑制HTLV-Ⅰ感染细胞的激活,阻止活化的HTLV-Ⅰ感染细胞迁移至脊髓,减轻脊髓中的慢性炎症反应。抗病毒途径主要通过抑制 HTLV-Ⅰ表达与复制,抑制HTLV-Ⅰ感染细胞的增殖,清除HTLV-Ⅰ感染细胞。免疫调节疗法已纳入未来HAM/TSP的治疗方案(Oh,2008),主要包括糖皮质激素、血液净化、己酮可可碱、肝素、大剂量丙种球蛋白、大剂量间断应用维生素C、磷霉素联合红霉等。抗病毒途径主要包括IFN-α及IFN-β、反转录酶抑制剂(核苷类似物如齐多夫定及拉米夫定)、人源化抗Tac抗体(daclizumab阻断 IL-2/IL-2R系统,促进HTLV-Ⅰ感染细胞凋亡)、组蛋白去乙酰酶抑制剂如丙戊酸钠、曲古菌素A、丁酸钠等。
对糖皮质激素疗效目前尚存争议。此外,减少HTLV-Ⅰ病毒抗原负荷量的疗法可能被用来降低HTLV-Ⅰ特异性细胞毒性淋巴细胞的活性(Nakamura,2009)。迄今多数针对HAM/TSP的治疗方案仅在长期患病且疾病严重程度不一的患者中作了小规模和/或非对照性研究,未来亟须针对抗炎及抗病毒药规范的对照研究。有报道,血浆交换可缓解症状,但需进一步验证。













