英文名称 :autosomal dominant polycystic kidney disease
中文别名 :成人型多囊性肾脏病
常染色体显性遗传多囊肾病(autosomal dominant polycystic kidney disease,ADPKD)曾被称为成人型多囊性肾脏病,是最常见的多囊肾病,具有遗传异质性。全球发病率为1/(1000~2500)。男女罹患机会无明显差异。主要表现为肾脏囊肿的发生、增多和增大,多系统受累。本病在严重程度、进展至终末期肾病的时间及肾外表现等方面的个体差异很大,甚至体现在同一家系中。
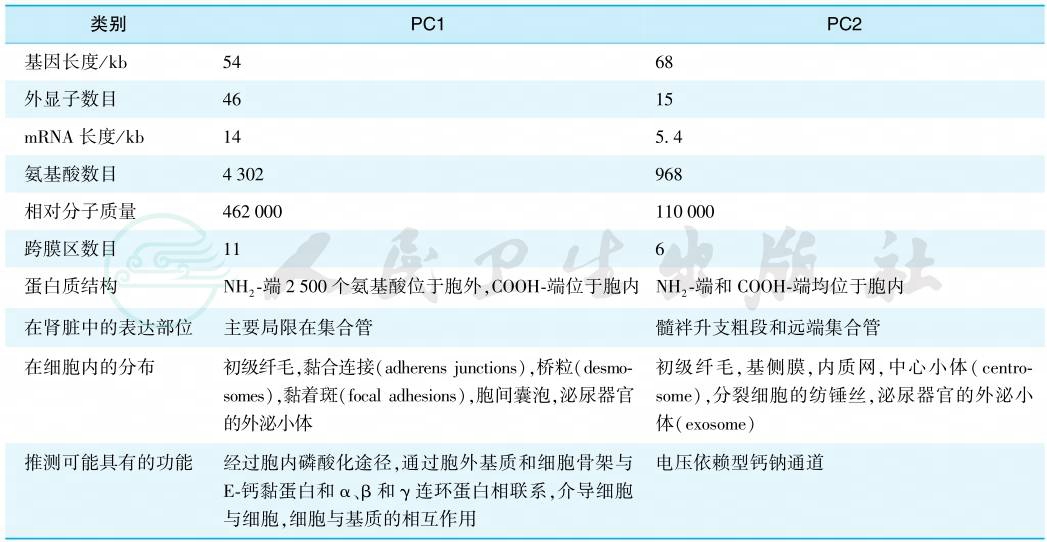
PKD1和PKD2两个基因突变可致ADPKD。PKD1基因位于16号染色体(16p13.3),编码多囊蛋白1(polycystin1,PC1),占ADPKD患者的85%。PKD2基因位于4号染色体(4q21),编码多囊蛋白2(polycystin2,PC2),约占患者中的15%。两种多囊蛋白的比较见表1。具有PKD2突变的患者肾功能损害进展稍慢。同时具有两者突变(transheterozygotes)的患者病变更加严重。还有极少数患者发现存在PKD3基因,但确切的异常位点尚未定位。目前为止,已经发现PKD1基因中有1923种截断突变,但主要发生在3’端。而5’端突变的患者病变更重,更容易伴有颅内血管瘤及血管瘤破裂出血。而在PKD2基因中,目前发现有241种类型各异的突变。
表1 两种多囊蛋白的比较
仅有1%左右的肾单位会演变成肾囊肿,以往认为患者从父母一方遗传了含有突变PKD1或PKD2的基因,从另一方遗传了野生型基因,这种先天存在的突变PKD1或PKD2基因影响到所有细胞,出生后少数细胞的正常等位基因又在感染、中毒等外界因素作用下发生体细胞突变(somatic mutation),即“二次打击模型(two-hit model)”,双重突变导致细胞正常功能丧失,后一次“打击”触发囊肿形成并决定其发生时间和部位。然而,PKD1或PKD2的单一等位基因不足会产生正常基因产物水平的随机波动,即便没有体细胞突变的“二次打击”,也会降低疾病产生的阈值(单一等位基因不足模型)。目前越来越多的证据支持单一等位基因不足模型。当然,PKD1和PKD2单倍体状态的基因不稳定性也会增加体突变二次打击的可能性,导致囊肿的形成和疾病的进展。
PC1和PC2通过细胞内的羧基端螺旋区相互连接作用,促进PC1转移到浆膜上,并稳定PC2的钙通道活性。PC1或PC2的缺乏或不足会导致细胞内钙离子浓度的下降,从而刺激环磷腺苷(cAMP)介导的囊肿上皮细胞的增生。
具有高增殖指数的肾小管的发育更容易受PC1和PC2水平减少的影响。而疾病的严重程度取决于基因灭活的时间。小鼠实验中如果PKD1和PKD2基因在尚未成熟的小管上皮细胞增生过程中灭活,就会引起巨大的囊肿及胚胎或新生儿期死亡。而如果基因灭活发生在肾脏上皮细胞已经分化成肾单位后,则病变较轻。
ADPKD患者早期肾脏大小正常,后期则增大,并出现形态异常,如肾盂肾盏的异形、肾乳头及肾锥体的完整结构受到破坏等。囊肿呈球形,大小不一。初起时肾内可仅有少数囊肿,随病程进展而渐增多,最终全肾均由囊肿所占,肾脏可达足球大小。光镜下,囊肿间尚可见到完整肾结构,从正常表现到肾小球硬化、小管萎缩、间质纤维化等程度不一,这些改变均为囊肿压迫引起肾缺血所致。电镜下显示的囊肿上皮细胞与近端或远端小管上皮细胞相似。囊液一般较清晰,当出现囊内感染或出血时则可为脓性或血性。
目前主要为对症处理,以缓解症状、预防和处理并发症。近年来随着对多囊肾病发病机制的研究,为该病的治疗提供了很多新的靶点。
(一)一般处理
剧烈运动可造成肾囊肿破裂而致肾损害,应尽量避免。避免使用咖啡因、茶碱等会增加cAMP产生的物质。而大量饮水,可以抑制抗利尿激素的产生,并减少肾结石形成的危险性。尿路感染、肾结石、梗阻需积极处理。对于明确有颅内或其他动脉瘤患者,需密切随访,较大的动脉瘤应考虑手术切除,以防止破裂出血。肾切除一般不予考虑,除非出现:不能耐受疼痛,不能控制的感染,巨大肾脏所致压迫症状严重,反复血尿、严重肾结石、恶性肿瘤可能等。
(二)降压治疗
首选药物为血管紧张素转换酶抑制剂(angiotensin converting enzyme inhibitor,ACEI)或血管紧张素Ⅱ受体拮抗剂(angiotensin receptor antagonist,ARB),效果显著。目前已经明确ACEI和ARB可以改善多囊肾患者蛋白尿和左心室肥厚,对肾功能进展的作用尚未得出阳性结论。钙通道阻滞剂降压效果也较明显,但有动物实验提示钙通道阻滞剂会加重囊肿的发展,需谨慎使用。利尿剂虽然对控制高血压有益,但利尿剂容易引起容量不足并可能会加速ADPKD囊肿的生长,应尽量避免使用。对于难治性高血压可适当加用α受体阻滞剂。
(三)实验性治疗方法
随着对ADPKD病理机制的深入了解,提出了一些新的治疗方法希望能够通过抑制囊肿上皮细胞的增生和囊液分泌延缓或终止ADPKD疾病的进展。其中,血管升压压素V2受体拮抗剂tolvaptan可以延缓肾脏体积的增大和肾功能的下降。在欧洲、日本、加拿大等国家已经被批准用以治疗ADPKD。但是tolvaptan会导致肝功能受损,25%的患者耐受性差。因此,美国FDA还没有批准用以治疗ADPKD。生长抑素类似物奥曲肽在小规模的临床实验中虽然可以阻止囊肿的扩大,但是对GFR的下降没有明显改善。荟萃分析发现,mTOR抑制剂无法延缓ADPKD患者肾功能的进展。其他药物如他汀类药物、二甲双胍、酪氨酸激酶抑制剂等目前都处于临床试验阶段。













