英文名称 :bronchial asthma
中文别名 :哮喘
支气管哮喘(bronchial asthma)简称哮喘,是由嗜酸性粒细胞、肥大细胞、T淋巴细胞、中性粒细胞、平滑肌细胞、呼吸道上皮细胞等细胞及细胞组分参与的呼吸道慢性炎症性疾病。该病表现为反复发作的喘息、气急、胸闷或咳嗽,同时伴有可变的气流受限和呼吸道高反应性,随着病程延长可导致呼吸道重塑。哮喘是一种异质性疾病,具有不同的表型和内型。全球哮喘防治倡议(Global Initiative for Asthma,GINA)和我国支气管哮喘防治指南是哮喘规范化防治和管理的重要指南。
哮喘的病因尚未完全阐明,目前认为受遗传和环境因素的双重影响。
1.遗传因素
哮喘是多基因参与的有遗传倾向的疾病。哮喘全基因组关联研究(GWAS)发现了众多哮喘候选基因,如儿童期哮喘发病与染色体17q21上血清类黏蛋白1样蛋白3(ORMDL3)基因附近的标志物之间存在可重现关联等。
2.环境因素
(1)室内外变应原
尘螨是最常见的室内变应原,另还包括家养猫、狗、蟑螂等。花粉与草粉是最常见的室外变应原。真菌(如曲霉、青霉、分枝孢子菌)也是室内外重要的变应原。职业性变应原有油漆、谷物粉、面粉、饲料、活性染料等。
(2)食物和药物
鱼、虾、蟹、牛奶、蛋类及食品添加剂(如防腐剂)等;非甾体抗炎药(如阿司匹林)、普萘洛尔等。
(3)吸烟和环境污染
哮喘患者主动吸烟会加重肺功能减退及控制不佳。被动吸烟是诱发哮喘的重要因素。母亲在妊娠期间吸烟会增加胎儿日后发生哮喘的易感性;空气中排放的各种废气、煤烟、油烟、杀虫剂等会诱发、加重哮喘。
(4)感染
呼吸道病毒感染与哮喘的发病和急性发作有关,以鼻病毒和流感病毒最为常见。新型冠状病毒疫情并未报道明显的哮喘急性加重增加。
(5)运动、精神因素
有70%~80%的哮喘患者在剧烈运动后会诱发哮喘;焦虑、紧张、抑郁、过度的躯体关注等会诱发哮喘。
(6)月经、妊娠等生理因素
月经前3~4天有哮喘加重的现象,可能与经前期黄体酮突然下降有关。妊娠也是诱发哮喘加重的因素之一。
全球哮喘患病率为1%~18%,且呈增长趋势。2010—2012年中国哮喘联盟组织的流行病学调查(CARE研究)报道中国大陆地区成人哮喘患病率为1.24%,2019年报道中国20岁以上成人哮喘患病率4.2%,显示近年我国哮喘患病率明显增高。哮喘规范化管理使死亡率在全球呈现下降趋势,我国为哮喘死亡率最高的国家之一,2016年为1.57/10万,亦较前明显降低。
(一)呼吸道炎症
现有研究表明,Th2细胞介导的过敏反应及Th17、Th22、Th9、调节性 T细胞(Treg)等 T淋巴细胞亚群、树突细胞、呼吸道上皮细胞、固有淋巴细胞等在哮喘中发挥着重要作用。
1.Th2细胞依赖、IgE介导的炎症途径
变应原在呼吸道被特定的抗原递呈细胞捕获,与细胞表面的主要组织相容性复合物Ⅱ类分子结合形成复合物。该复合物与T细胞表面受体结合,激活初始T淋巴细胞向Th2细胞分化,Th2细胞合成并分泌白介素(interleukin,IL)-4、IL-5、IL-13等进而激活 B 淋巴细胞,使之合成特异性IgE,后者结合到肥大细胞、嗜碱性粒细胞和嗜酸性粒细胞等表面的IgE受体,使机体呈致敏状态;当再次接触同种抗原时,抗原与特异性IgE交联结合,从而造成炎症介质的级联释放,导致呼吸道平滑肌收缩、黏液分泌增加及炎症细胞浸润,产生哮喘的临床表现。呼吸道局部释放的趋化因子促使炎症细胞向呼吸道募集,这些效应细胞又释放多种炎症因子,从而构成了一个与炎症细胞相互作用的复杂网络,导致呼吸道慢性炎症。
2.非Th2细胞的炎症途径
除Th1、Th2细胞外,还存在其他T淋巴细胞亚群。研究表明,Th17细胞对于激素抵抗型哮喘患者出现的以中性粒细胞为主的呼吸道炎症起促进和维持作用。Treg细胞具有免疫抑制作用。哮喘中Treg细胞减少,从而不能有效抑制促炎症细胞因子的合成及释放,进而导致或加重呼吸道炎症。近年来发现固有免疫应答亦参与了哮喘的发生。过敏原直接作用于呼吸道上皮细胞,促使其释放IL-25、IL-33、胸腺基质淋巴细胞生成素(TSLP),诱导2型固有淋巴细胞(ILC2)释放IL-5、IL-13,促进骨髓嗜酸性粒细胞动员、分化、成熟,向肺部募集,参与哮喘的呼吸道炎症反应。
(二)气道高反应性(airway hyperresponsiveness,AHR)
指呼吸道对正常不引起或仅引起轻度应答反应的刺激物出现过度的呼吸道收缩反应。呼吸道炎症是导致AHR最重要的机制,呼吸道上皮损伤与炎症介质和细胞因子的参与为主要原因。AHR是哮喘的基本特征。
(三)呼吸道重塑
指呼吸道结构发生改变,上皮损伤、基底膜增厚、呼吸道平滑肌增厚、杯状细胞化生与呼吸道血管和淋巴管增生。呼吸道重塑使哮喘患者出现不可逆气流受限及持续存在的AHR,与持续存在的呼吸道炎症反应和呼吸道上皮细胞正常修复机制受损有关。
(四)神经机制
支气管受复杂的自主神经支配,包括胆碱能神经、肾上腺能神经和非肾上腺非胆碱能(NANC)肺内感觉神经系统。哮喘与β肾上腺素能受体功能低下和迷走神经张力亢进密切有关。此外,呼吸道上皮层内的肺神经内分泌细胞(PNECs)可分泌多种肽类激素。肺内感觉神经和PNECs可能通过一些共有的化学信息分子(如神经肽)及其受体构成一个复杂的神经-内分泌网络,发挥调节气道反应性和炎症的作用。
基本病理改变为呼吸道炎症和重塑。早期为支气管黏膜肿胀、充血,分泌物增多,呼吸道内炎症细胞浸润,呼吸道平滑肌痉挛等可逆性的病理改变。随着疾病发展和反复发作,病理变化逐渐加重,可见支气管柱状上皮细胞纤毛倒伏、脱落,上皮细胞坏死,黏膜上皮层杯状细胞增多,黏液蛋白产生增多,支气管黏膜层大量炎症细胞浸润、黏液腺增生、基底膜增厚,支气管平滑肌增生,成纤维细胞增殖和活化,细胞外基质蛋白沉积,呼吸道黏膜下血管数目明显增多。
1.血液检查
血常规中嗜酸性粒细胞百分比和总数;血清总IgE反映过敏状态,在过敏性哮喘中可升高。
2.诱导痰检查
可用于区别哮喘表型及炎症状态,正常人诱导痰中嗜酸性粒细胞计数<3%,过敏性嗜酸性粒细胞型哮喘表型者诱导痰中嗜酸性粒细胞明显升高;中性粒细胞表型者细胞分类以中性粒细胞为主;混合细胞表型者可见两者均增多;寡细胞表型者细胞数很少。
3.影像学检查
一般胸部X线片或胸部CT非急性发作期无明显异常。急性发作期胸部X线片可见肺透亮度增高,膈肌低平等肺过度充气表现。哮喘严重发作者应常规行胸部X线检查,注意有无肺部感染、肺不张、气胸、纵隔气肿等并发症的存在。影像学检查还可协助发现哮喘患者并发症,如支气管扩张症、肺不张等表现。
4.肺功能检查
是哮喘诊断和评估的重要手段。
(1)常规肺通气及容量检测
哮喘发作时呈阻塞性通气改变,呼气流速指标显著下降。FEV1、FEV1/FVC%、最大呼气中期流量(maximal mid-expiratory flow,MMEF)及最大呼气流量(PEF)均下降。肺弥散功能正常。肺容量指标见残气量增高、功能残气量和肺容量增高,残气占肺总量百分比增高。
(2)支气管舒张试验
对于有气道阻塞或小气道功能障碍的患者,可行支气管舒张试验。吸入支气管扩张剂后FEV1较用药前增加≥12%,且绝对值增加≥200ml,为支气管舒张试验阳性,对诊断哮喘及评估病情有重要作用。
(3)支气管激发试验
对于有哮喘症状但肺功能正常的患者,可行支气管激发试验。吸入乙酰甲胆碱或组胺后通气功能下降、呼吸道阻力增加。在设定的激发剂量范围内,如FEV1下降≥20%,为支气管激发试验阳性,使FEV1下降20%的累积剂量(PD20-FEV1)或累积浓度(PC20-FEV1),可对呼吸道高反应性的程度作出定量判断,PD20-FEV1或PC20-FEV1越低,表示呼吸道反应性越高。支气管激发试验阳性对诊断哮喘有重要作用,如未治疗者支气管激发试验阴性,基本上可以排除哮喘。FEV1<70%预计值时,不宜行激发试验。
(4)PEF及变异率
哮喘发作时PEF下降。哮喘患者常有通气功能昼夜变化,如果1~2周内平均昼夜PEF变异率≥10%(儿童≥13%)有助于哮喘的诊断。
5.呼出气一氧化氮检测(FeNO)
是呼吸道炎症的重要生物标记物,可评估呼吸道炎症程度。正常值成人5~25ppb,儿童5~20ppb。过敏性哮喘、过敏性鼻炎、嗜酸性粒细胞性支气管炎患者FeNO升高,FeNO越高,呼吸道炎症越严重。FeNO>50ppb,预示对吸入激素治疗反应好,并对诊断哮喘有帮助。
6.变应原检测
皮肤点刺试验和血清特异性IgE检测可明确过敏状态,指导患者尽量避免接触变应原及进行特异性免疫治疗。
(一)治疗目标
治疗应该长期规范地应用抗炎药物,预防哮喘急性发作,减少并发症发生,改善肺功能,提高生活质量,以达到并维持哮喘控制。2014—2019年GINA均提出并强调,哮喘治疗目标要达到哮喘总体控制,既要达到症状控制,又要降低不良预后的危险因素。
(二)治疗药物
根据其作用机制可分为舒张支气管和抗炎两大类,某些药物兼有舒张支气管和抗炎作用。
1.舒张支气管药物
(1)β 2受体激动剂
通过选择性兴奋β2受体舒张呼吸道平滑肌、减少肥大细胞和嗜碱性粒细胞脱颗粒和介质的释放、降低微血管的通透性、增加呼吸道上皮纤毛的摆动等功能缓解哮喘症状。可分为短效(作用维持4~6小时)和长效(作用维持12小时或以上)β2受体激动剂,后者又可分为速效(数分钟起效)和缓慢起效(30分钟起效)两种(表4)。
表4 β2受体激动剂
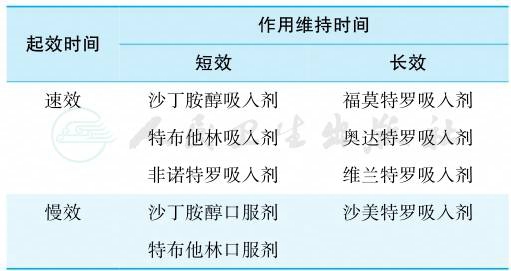
1)短效β 2受体激动剂(SABA)
常用的沙丁胺醇和特布他林可吸入、口服给药。
①吸入:通常在数分钟内起效,疗效可维持数小时,是缓解急性哮喘症状的首选药物,也可用于运动性哮喘的预防。如每次沙丁胺醇100~200μg或特布他林250~500μg,必要时每20分钟重复1次。不良反应有骨骼肌震颤、低血钾、心律失常等,一般少见。
②口服:通常在服药后15~30分钟起效,疗效维持4~6小时。心悸、骨骼肌震颤等不良反应较吸入给药明显。缓释和控释剂型作用时间可达8~12小时,适用于夜间哮喘症状的预防和治疗。SABA需间歇使用,长期、单一和过量应用可造成细胞膜β2受体下调,呼吸道炎症无法控制,应予以避免。
2)长效β 2受体激动剂(LABA)
LABA分子结构中具有较长的侧链,舒张支气管平滑肌的作用可维持12小时以上。有吸入、口服和透皮给药等途径,目前临床可用吸入型LABA有沙美特罗、福莫特罗、维兰特罗、奥达特罗和茚达特罗。沙美特罗吸入给药后30分钟起效,平喘作用维持12小时以上,推荐剂量50μg每天2次。福莫特罗吸入给药后3~5分钟起效,平喘作用维持8~12小时以上;平喘作用具有一定的剂量依赖性,推荐剂量4.5~9μg每天2次;维兰特罗吸入给药后6分钟起效,平喘作用维持24小时,推荐剂量25μg每天1次。奥达特罗和茚达特罗暂未用于哮喘治疗。临床推荐LABA联合ICS治疗哮喘,两者具有协同抗炎和平喘作用,适用于中至重度持续哮喘患者的长期治疗,福莫特罗因起效迅速,也可和ICS联合用于哮喘按需治疗。口服LABA有丙卡特罗、班布特罗,作用时间可维持12~24小时,用于中重度哮喘的控制治疗,适用于缓解夜间症状。透皮吸收剂型现有妥洛特罗贴剂,为中效β2受体激动剂,由于采用结晶储存系统来控制药物释放,药物经过皮肤吸收,疗效可维持24小时,并减轻了全身不良反应,每天1次,对预防夜间症状有较好疗效。LABA不应长期单独使用。
(2)茶碱类
可舒张支气管平滑肌,也有强心、利尿、扩张冠状动脉、兴奋呼吸中枢和呼吸肌等作用,低浓度茶碱还具有抗炎和免疫调节作用。GINA不推荐茶碱作为控制药物治疗哮喘,但由于其价格低廉,在我国仍有较广泛应用。对应用ICS或ICS/LABA仍未控制的哮喘患者,可加用缓释茶碱作为哮喘的维持治疗。静脉给药建议监测其血药浓度,避免心律失常、血压下降甚至死亡等不良反应。多索茶碱及双羟丙茶碱(喘定)不良反应较少。
(3)抗胆碱能药物
吸入型抗胆碱能药物可阻断节后迷走神经传出支,通过降低迷走神经张力而舒张支气管。溴化异丙托品为短效抗胆碱能药物。长效抗胆碱能药物包括噻托溴铵、格隆溴铵、乌美溴铵、阿地溴铵,目前噻托溴铵用于哮喘治疗,选择性抑制M1和M3受体,每天1次吸入给药。与β2受体激动剂联合应用具有协同、互补作用。
2.抗炎药物
(1)糖皮质激素
是最有效的抗变态反应性炎症的药物。
1)吸入糖皮质激素(ICS)
可有效改善哮喘症状和肺功能、控制呼吸道炎症,减少发作频率和减轻发作程度,降低病死率。局部不良反应包括声音嘶哑、咽部不适和念珠菌感染,吸药后及时漱口。全身不良反应与药物剂量、生物利用度、肝脏首过代谢及全身吸收药物的半衰期等有关。长期高剂量ICS可出现的全身不良反应包括皮肤瘀斑、肾上腺皮质功能抑制、血糖异常和骨质疏松等。ICS目前有丙酸倍氯米松、布地奈德、丙酸氟替卡松、糠酸氟替卡松和环索奈德。干粉和定量气雾剂是哮喘长期治疗的首选,雾化溶液适用于哮喘急性发作及婴幼儿。国际上推荐ICS日剂量见表5。
表5 常用ICS日剂量高低与互换关系

2)口服给药
适用于中度及以上哮喘急性发作、重症哮喘大剂量ICS治疗仍无法控制的患者,作为静脉应用激素治疗后的序贯治疗。一般使用半衰期较短的泼尼松、泼尼松龙或甲泼尼龙等。对于重症糖皮质激素依赖型哮喘,可每天或隔天清晨顿服。泼尼松维持剂量推荐≤10mg/d。长期口服可能引起骨质疏松症、高血压、糖尿病、下丘脑-垂体-肾上腺轴功能抑制、肥胖症、白内障、青光眼、皮肤菲薄导致皮纹和瘀斑、肌无力等不良反应。对于伴有结核、寄生虫感染、骨质疏松、青光眼、糖尿病、严重抑郁或消化性溃疡的哮喘患者,应慎用并密切随访。哮喘急性发作时推荐剂量泼尼松龙40~50mg/d,当症状缓解时应及时减量或停药。
3)静脉给药
用于重度急性发作治疗。
(2)白三烯调节剂(LTRA)
包括半胱氨酰白三烯受体拮抗剂和5-脂氧化酶抑制剂,前者通过拮抗细胞表面白三烯受体,抑制肥大细胞和嗜酸性粒细胞释放的半胱氨酰白三烯的致喘和致炎作用,具有较强的抗炎作用,可改善症状和肺功能、减少哮喘恶化。与ICS联用,可减少中至重度哮喘患者ICS用量。尤其适用于阿司匹林哮喘、运动性哮喘和伴有过敏性鼻炎哮喘。孟鲁司特10mg,每晚1次口服。
(3)抗组胺药物
酮替芬和新一代组胺H1受体拮抗剂氯雷他定、西替利嗪、依巴斯丁、曲尼斯特等具有抗过敏作用,可用于伴有变应性鼻炎的哮喘患者。
(4)生物靶向药物
针对高Th2表型的生物靶向治疗药物已成为哮喘新药开发的热点,对重症过敏性哮喘疗效较好。
1)抗IgE单体
是人源化重组的抗IgE单克隆抗体(omalizumab,奥马珠单抗),与血液中游离IgE结合,阻断 IgE与效应细胞(肥大细胞、嗜碱性粒细胞等)表面的FcεRⅠ受体结合,从而阻断过敏性炎症的级联反应,阻止炎症介质释放,发挥抗炎作用。多项国内外临床研究表明,中至重度过敏性哮喘患者经奥马珠单抗治疗后,可以显著改善哮喘症状,减少口服激素用量,减少哮喘急性发作和住院率。长期使用安全性良好。国内外哮喘指南均推荐奥马珠单抗用于经ICS-LABA治疗仍未控制的重度过敏性哮喘患者。根据患者治疗前IgE水平和体重确定剂量后皮下注射,每2周或4周给药,一般16周后评估疗效,如有效,建议使用12个月以上。
2)抗IL-5/IL-5R单抗
IL-5是嗜酸性粒细胞在骨髓中分化、生成及在呼吸道趋化过程中重要的细胞因子。抗IL-5单抗通过阻断IL-5与其受体结合,阻断IL-5的作用,抑制呼吸道嗜酸性粒细胞炎症。国外研究结果显示,抗IL-5单抗可以减少嗜酸性粒细胞型哮喘急性发作,减少急诊或住院率,减少口服激素剂量,改善哮喘控制及肺功能。目前美泊珠单抗(IL-5单抗)已被美国和欧盟批准上市用于>12岁中-高剂量ICS-LABA未控制的重症嗜酸性粒细胞型哮喘。正在进行Ⅲ期临床研究的还有抗IL-5单抗reslizumab和抗IL-5受体单抗benralizumab等。
3)抗IL-4R单抗
抗IL-4R单抗(dupilumab)通过特异性地与IL-4Rα亚基结合,阻断了IL-4和IL-13的生物学作用,从而抑制嗜酸性粒细胞型呼吸道炎症。国外临床研究发现,dupilumab可以明显减少嗜酸性粒细胞型哮喘患者急性发作,国内外进一步临床研究正在进行中。
(三)哮喘的长期治疗
1.控制药物
主要通过抗炎作用和长效扩张支气管作用使哮喘达到并维持临床控制,包括ICS、全身用糖皮质激素、白三烯调节剂、LABA(须与ICS联合应用)、缓释茶碱、LAMA(噻托溴铵)、抗IgE抗体、抗组胺药及其他抗炎药物。
2.缓解药物
通过迅速解除呼吸道痉挛从而缓解哮喘症状,包括SABA、全身用糖皮质激素、短效胆碱能受体阻断剂(SAMA)、茶碱及短效口服β2受体激动剂等。
3.制订初始治疗及长期治疗计划
对初诊患者要评估其病情严重度,制定初始治疗方案、长期随访行动计划,定期随访、监测、评估,以改善患者的依从性,检查吸入药物使用的正确性,并根据其病情变化及时修订治疗方案。哮喘患者长期治疗方案分为5级(表6),长期管理模式见图1。
表6 哮喘分级治疗的药物选择

注:ICS.吸入糖皮质激素;LABA.长效β2受体激动剂;SABA.速效β2受体激动剂;LTRA.白三烯受体拮抗剂;OCS.口服糖皮质激素。
控制哮喘强调抗炎治疗的重要性,对于以往未经规范治疗的初诊哮喘患者应根据病情严重度,选择相应的治疗级别,病情轻者从第1~2级治疗开始,病情严重者选择第3或4级治疗方案。
整个治疗过程中要对患者进行病情评估,调整并检查对治疗的反应。当哮喘未控制或症状加重时,应升级治疗以达哮喘控制。当哮喘控制并维持至少3个月后,应降级治疗,推荐的降级方案为:①单用中-高剂量 ICS:将 ICS剂量减少 50%。②ICS+LABA:将ICS剂量减少50%,仍继续使用LABA联合治疗。当达到低剂量ICS时,可改为每日1次联合用药,或停用LABA单用ICS。若患者使用最低剂量控制药物达到哮喘控制1年以上时,可考虑停用控制药物。要确立维持最佳控制的治疗最低级别和最小剂量,以降低费用,确保用药安全性。
4.哮喘控制不佳原因的识别及处理
部分哮喘患者即使经过ICS-LABA的联合治疗,仍无法得到控制,其中少部分是重症哮喘,而大部分是由于各种原因没有给予充分关注及处理,导致哮喘难以控制。长期暴露在过敏原、职业接触、吸烟等诱发因素、吸入药物使用不当、依从性差、合并过敏性鼻炎、鼻窦炎、肥胖、胃食管反流、阻塞性睡眠呼吸暂停综合征、焦虑/抑郁等是导致哮喘控制不佳的常见原因,需识别并积极处理。
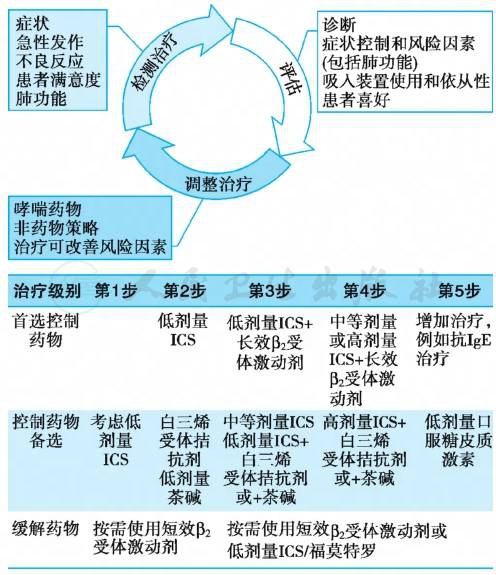
图1 哮喘长期管理模式
ICS.吸入性糖皮质激素。
(四)哮喘急性发作的处理
治疗取决于发作严重程度及对治疗的反应。目的在于尽快缓解症状、解除气流受限和低氧血症。若有相关死亡高危因素的患者,当有急性发作时应尽早到医院就诊。
高危患者:①曾有过气管插管和机械通气的重度哮喘发作病史;②过去1年因哮喘住院或看急诊;③正在使用或刚停用口服糖皮质激素;④目前未使用ICS;⑤过分依赖SABA,尤为沙丁胺醇(或等效药物)>1支/月者;⑥有心理疾病或社会心理问题,包括使用镇静剂;⑦有对哮喘治疗计划不依从的历史。
1.轻度和部分中度急性发作
在家或社区治疗。吸入SABA,第一小时2~4喷/20min。根据治疗反应,轻度可调整为2~4喷/3~4h,中度6~10喷/1~2h。亦可口服短效氨茶碱或特布他林。如果治疗反应不好,尽早口服糖皮质激素(泼尼松龙0.5~1mg/kg或等效剂量的其他激素),必要时及时到医院就诊。
2.部分中度和重度急性发作
急诊或医院就诊。氧疗以缓解低氧血症。雾化SABA,初始治疗时连续雾化给药,随后按需间断给药(每4小时一次)。可联合使用β2受体激动剂和抗胆碱能药物以取得更好的支气管舒张作用。可静脉应用茶碱,尽早使用全身糖皮质激素,推荐口服泼尼松龙30~50mg/d或等效的其他激素。重度急性发作可静脉使用甲泼尼龙80~160mg,或氢化可的松400~1 000mg分次给药。全身糖皮质激素的疗程一般为5~7天,通常不需递减撤药。哮喘急性发作患者医院内治疗流程见图2。
3.危重哮喘的处理
经上述治疗,临床症状和肺功能无改善甚至继续恶化,应及时给予机械通气治疗,机械通气的指征主要包括:神志改变、呼吸肌疲劳、动脉血气提示呼吸性酸中毒。可先采用无创机械通气,若无效、不能配合或出现呼吸骤停者,应及时气管插管机械通气。危重哮喘存在呼吸道阻力明显增高,要选择低潮气量通气,允许性高碳酸血症。气管插管早期可短期应用镇静剂、肌松剂,以减少呼吸道阻力,减少气压伤。症状改善尽早拔管,必要时可用无创通气序贯。
激素应早期、足量、短程使用,甲泼尼龙80~240mg/d。可静脉应用氨茶碱,雾化吸入SABA和SAMA。对于顽固性重度发作,硫酸镁和钙通道阻滞剂可能有效。注意纠正酸中毒并维持水、电解质平衡,加强对症、支持治疗,如合并感染,给予积极抗感染治疗。
危重哮喘要尽早入住 ICU,加强心肺功能监护,防止并发症。
应寻找并处理急性发作的诱因,制定个体化长期治疗方案及哮喘行动计划,预防再次急性发作。
(五)特异性免疫治疗(specific immunotherapy,SIT)
是在临床上确定过敏性疾病患者的变应原后,将变应原制成疫苗并配制不同浓度,经反复注射或舌下含服、口服,逐步增加剂量和浓度,以提高患者对该种变应原的耐受性,当再次接触该变应原时过敏现象减轻或不再产生。SIT是唯一可影响变应性疾病自然病程的病因治疗,并可防止变应性鼻炎发展为哮喘。SIT适用于由明确变应原所致的哮喘,通常伴有变应性鼻炎,特异性IgE抗体增高而常规治疗不满意者,或有季节性哮喘发作患者,或常规治疗虽有效但由于无法避免接触变应原而反复发作者。目前国内最常用的SIT针对尘螨过敏。SIT分为脱敏和维持治疗两个阶段,总疗程为3~5年。
(六)支气管热成形术
经纤维支气管镜射频消融呼吸道平滑肌治疗重症哮喘,减少哮喘患者支气管平滑肌数量,降低支气管收缩能力和呼吸道高反应性。多项研究证明其对重度哮喘有效,但其远期疗效及安全性、最大获益人群等仍需进一步大规模临床研究。治疗需严格掌握适应证,注意围手术期安全性,分析获益-风险比,并在有资质的注册中心进行。
(七)特殊类型哮喘及其处理
1.重症哮喘
在过去1年中,需要使用GINA建议的第4级或以上治疗才能维持控制或经上述治疗仍未控制的哮喘。重症哮喘虽仅占总哮喘5%~10%,但却是哮喘管理中的难点和重点,医疗卫生资源花费巨大。对重症哮喘的治疗和管理需全面评估:第一,要再次明确哮喘诊断;第二,评估导致哮喘难以控制的混杂因素,包括哮喘触发因素暴露史、吸入技术、用药依从性,特别要评估合并症及其处理,常见的合并症有鼻炎、鼻窦炎、胃食管反流、阻塞性睡眠呼吸障碍综合征、焦虑、抑郁等,需要积极处理;第三,评估哮喘表型,针对表型指导药物选择,给予个体化治疗。
重症哮喘根据临床特点,分为早发过敏性哮喘、晚发嗜酸性粒细胞型哮喘、频繁急性发作型哮喘、持续气流受限型哮喘、肥胖型哮喘;根据炎症类型,分为Th2型和非Th2型哮喘。生物靶向药物如抗IgE单抗、抗IL-5单抗、抗IL-4单抗主要针对Th2型重症哮喘,在常规控制药物基础上加用。但对于非Th2型重症哮喘,目前仍无有效药物,可在高剂量ICS-LABA基础上加用噻托溴铵、小剂量阿奇霉素长期口服或支气管热成形术等,根据其不同表型及特点进行选择。
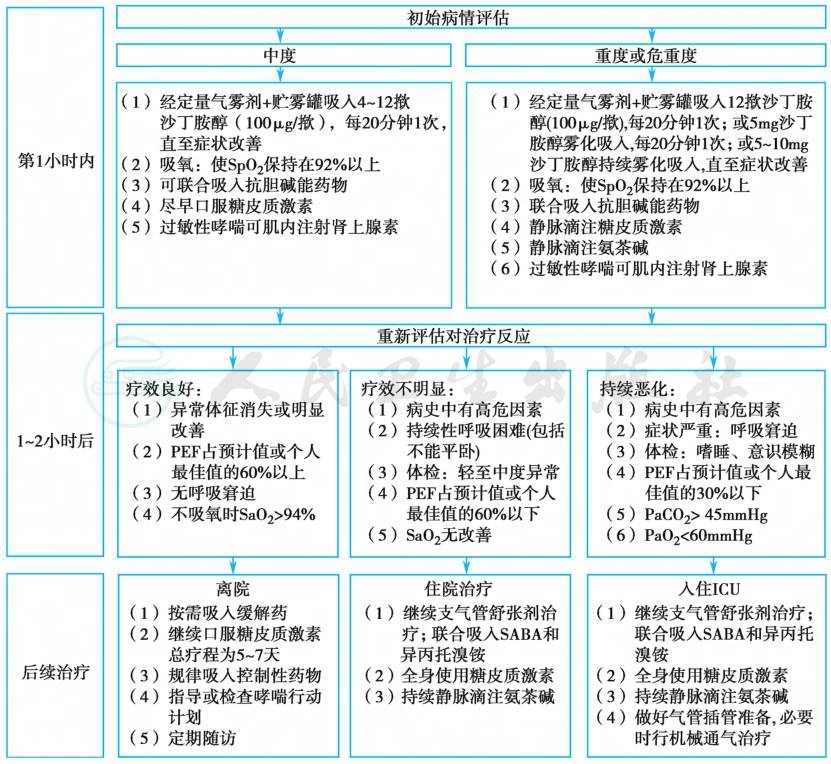
图2 哮喘急性发作医院内处理流程
2.妊娠期哮喘
哮喘发作和平喘药物均会对胎儿及分娩过程产生不良影响,但哮喘未控制远比药物不良反应危险。因此,妊娠期妇女首先应积极控制哮喘,最好在孕前得到控制,并用最少的控制药物维持。怀孕后应密切随访,在医师指导下用药。用药原则是尽可能应用吸入药,尽量避免使用对孕妇、胎儿安全性尚不确定的药物;如果病情需要,应将用药剂量尽量控制在最低水平。妊娠期推荐药物:①特布他林或沙丁胺醇吸入剂:妊娠妇女在任何阶段都可以使用。②ICS:最主要的抗炎药物,推荐中、低剂量吸入型布地奈德(为妊娠用药 B级)。③吸入LABA:低剂量ICS不能控制者,选用联合吸入LABA。④白三烯受体拮抗剂:较安全。⑤抗胆碱药物:与β2受体激动剂、ICS联合使用,可选择。⑥全身应用激素:妊娠期重症、不能控制的哮喘对母体和胎儿危险极大,应给予积极治疗,在权衡利弊下可应用全身激素治疗。口服泼尼松最常用,≤10mg/d对孕妇及胎儿不良反应少。病情严重时泼尼松30~40mg/d,连续3~7天,逐渐减量短期内停药。长期口服激素对孕妇及胎儿均有较大的不良反应,孕妇应尽量避免。切忌在怀孕后擅自停药或减药,可能导致哮喘急性加重。妊娠期哮喘患者更应密切随访,规范治疗和管理。
3.哮喘慢阻肺重叠(asthma-COPD overlap,ACO)
以持续气流受限为特征,同时伴有与哮喘和慢阻肺相关的临床特点。ACO较单独哮喘或慢阻肺病情更重,预后更差。目前ACO诊断标准尚不确切,慢阻肺患者如果存在可逆的气流受限、FeNO增高、诱导痰嗜酸性粒细胞增高、既往有哮喘或过敏性鼻炎病史,则需考虑ACO诊断;有高危因素(吸烟、有害气体暴露等)的哮喘患者经过规范治疗仍然存在持续气流受限,要考虑ACO诊断。ACO治疗要兼顾抗炎和解痉,推荐联合应用ICS与LABA 和/或 LAMA。
(八)哮喘的教育和管理
是哮喘维持控制的保障,目的是指导患者自我管理,对治疗目标达成共识,制定个体化的书面管理计划,以达到控制和避免发作。教育方式包括:①初诊教育;②定期开办哮喘学校、健康讲座,患者经验交流会;③移动网络平台。目的为与患者建立医患伙伴关系,提高患者的依从性,使患者增加理解、增强自信心、增强自我管理能力,从而减少卫生保健资源消耗。物联网医学作为一种全新的诊疗模式,弥补了传统医疗“间断化、片段化”的缺陷,在医患之间构架了一条便捷的纽带,可广泛应用于哮喘的管理中,可以做到对哮喘发作的即刻预警和及时治疗,实现更加精准医疗。













