英文名称 :long QT syndrome
长QT间期综合征(long Q-T syndrome,LQTS)是一组表现为心肌复极化时间延长的离子通道病的统称,1957年首先报道,发病率1/2 000。以心电图QT间期延长、尖端扭转型室性心动过速、晕厥、搐搦及猝死为临床特征。按病因可以分为先天性和获得性。心电图特征性为基础状态下QT间期延长(校正QT间期>480毫秒),T波异常和U波。在此基础上可以发生尖端扭转型室性心动过速(torsade de pointes,TdP),从而引起晕厥、抽搐和心脏性猝死。1966年法国学者Dessertenne首先描述TdP,是一种以QRS波群的方向和波形围绕等电位线上下扭转为典型特征的多形性室性心动过速。
先天性长QT间期综合征与基因异常遗传有关。现已发现20个基因上的950多个突变可导致先天性LQTS,包括7个编码钾通道基因、4个编码或调控钠通道的基因、1个编码钙通道的基因及1个非编码离子通道基因。对患者进行基因检测时,发现已知的20个基因突变的阳性检出率为80%~85%,而将近15%~20%的LQTS患者的致病基因仍未知。LQTS通常是一种单一突变遗传疾病,但也有少数病例可见多种突变发生在一个或多个基因上,占LQTS患者总数的5%~10%;有多种基因突变的LQTS患者可能比单一突变的患者表现出更长的QTc。
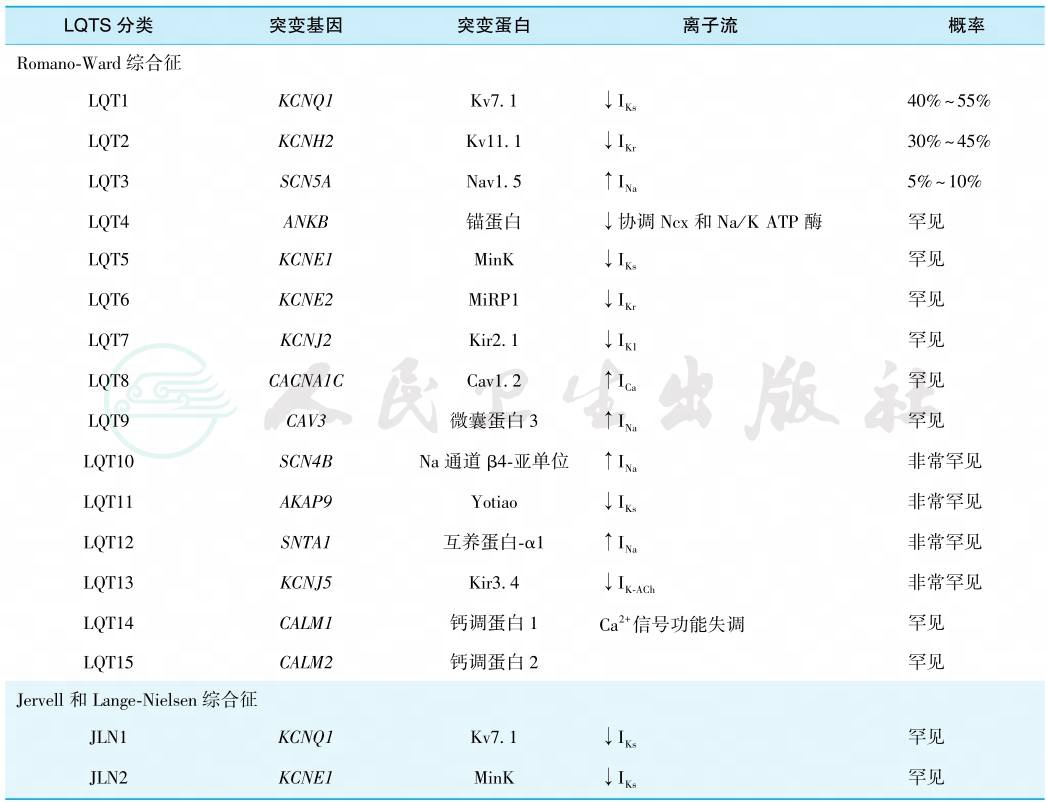
如按突变基因分型,目前至少已发现了17种LQTS的类型(表1),其中常见的是 1~3 型(LQT1,LQT2,LQT3),占所有患者的92%。其中LQT1和LQT2分别为编码钾离子通道的基因KCNQ1和KCNH2突变所致。LQT3为钠通道相关基因SCN5A突变。QT间期延长的本质是心肌细胞动作电位时程的延长。SCN5A突变携带者可以分别或同时出现多种疾病的表现,包括LQTS、Brugada综合征、传导延缓、病态窦房结综合征及房颤等,这一现象被称为SCN5A重叠综合征。与Brugada综合征相反,SCN5A基因导致的钠通道蛋白突变为功能获得性突变,导致晚钠电流等内向电流增强。KCNQ1和KCNH2为功能丧失性突变,导致钾通道IK s和IK r等外向电流减弱,这些都可导致动作电位时程的延长,在心电图上表现为长QT间期。早期后除极(early after-depolarization,EAD)是TdP发作的主要触发机制。期前收缩后长间歇增加了复极离散和EAD的幅度,容易形成折返激动,诱发TdP发生。
表1 已知的LQTS突变基因和相关的通道蛋白
获得性LQTS患者平常QT间期正常,心肌细胞离子通道潜在的功能异常是基础,在一定条件下,由药物、代谢和其他心脏疾病等继发因素诱导而表现出LQTS。致QT间期延长药物包括部分抗心律失常药(奎尼丁、普鲁卡因胺、索他洛尔、多菲利特、胺碘酮)、抗组胺药、抗抑郁药、抗感染药物(大环内酯类、喹诺酮类、吡咯类抗真菌药物)等。代谢因素主要为电解质紊乱(低血钾、低血镁、低血钙)及肝肾功能异常等。心力衰竭、心肌缺血、心动过缓,心肌炎和心肌病等也可作为获得性LQTS的病因。
诊断LQTS首先是需要正确测量QT间期,一般选择Ⅱ或V5导联测量。通常用Bazett公式来计算校正的QT间期,即测得的未校正的QT间期除以RR间期的平方根(以秒为单位)。美国心脏协会/美国心脏病学学会2010年发表的院内获得性LQTS防治建议中,推荐QTc正常值男性为470毫秒,女性为480毫秒。不论女性或男性,QTc>500毫秒都属于明显的异常。10%(LQT3)~37%(LQT1)的患者在基础状态下QTc可在正常范围。站立、运动、儿茶酚胺类药物可诱发QTc的延长。心电图上LQT1的心电图常表现为宽底T波,而LQT2的T波电压较低,伴有切迹或双向,LQT3具有长等电位线后出现窄底T波的特征(图2)。如能记录到发生临床事件时尖端扭转型室速的心电图则更有临床价值。
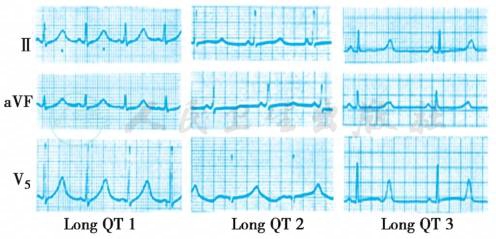
图2 LQT1~3型患者的特征性心电图表现
LQT1(左)T 波宽大,LQT2(中)T 波双相,LQT3(右)T波延迟出现。
按照HRS/EHRA/APHRS联合专家共识的建议,LQTS的治疗包括药物和非药物治疗治疗两个方面。如无室性心律失常发作的临床证据且无猝死家族史者仅需随访。对于出现临床症状的长QT间期综合征患者的治疗包括:①规避引起QT延长的因素,包括避免相关药物使用和电解质紊乱;②给予最大耐受剂量的β受体阻滞剂,可降低心脏事件的发生率;③对发生过恶性心律失常的患者,应该植入ICD;④针对β受体阻滞剂无效或拒绝ICD植入的高危患者,可行左心交感神经切除术(LCSD)。
β受体阻滞剂是一线治疗选择,可显著降低心脏事件发生率。治疗量的β受体阻滞剂对绝大多数的LQT1患者有保护作用,应将缓释的普萘洛尔或纳多洛尔作为首选药物,同时应强调β受体阻滞剂的足量使用。普萘洛尔[2~4mg/(kg•d)]和纳多洛尔[1~1.5mg/(kg•d)]在抑制心脏事件方面优于美托洛尔。如普萘洛尔的通常用量可从10mg,每日3次起始,每隔5~7日加量5mg,直至患者能耐受的最大剂量。美托洛尔和阿替洛尔由于疗效不佳通常不作为首选药物使用。β受体阻滞剂治疗在LQT1和LQT2中较LQT3的效果更加明显。
所有发生过心脏事件的患者均适合接受ICD治疗,特别是在使用β受体阻滞剂后仍发生晕厥的患者。ICD适应证为:①所有经历药物治疗后仍发生心脏骤停的患者;②未经过药物治疗发生心脏骤停,不存在可逆的因素,如低钾血症;③尽管服用了足量的β受体阻滞剂,仍发生晕厥,患者不愿意选择LCSD;④服用了β受体阻滞剂及曾行LCSD,但仍发生晕厥;⑤少数无症状患者,但QTC>550毫秒,并且有明显心电异常的信号(如T波改变)或者其他证据表明具有高危因素(如长时间的窦性停搏合并T波形态异常)。对于未发生恶性心律失常的患者,ICD适用于评估危险较高的患者。包括双位点突变和JLN综合征等。考虑到ICD植入本身的风险,对于无症状的患者,需严格进行个体化评估,包括疾病相关猝死风险,手术相关风险及患者个人意愿。对于未使用β受体阻滞剂情况下发生事件的LQT1的婴幼儿,也可以予以β受体阻滞剂+LCSD的治疗方案。
LCSD目前可以通过开放手术或胸腔镜实施,切除胸3~4交感神经节,可用于ICD频繁放电,拒绝或当前状况不能植入ICD的患者。特别适合因体格大小不适合ICD植入的高危婴幼儿患者,或存在哮喘等β受体阻滞剂使用禁忌的患者。
对于药物引起的获得性LQTS及TdP发作的患者,应静脉注射硫酸镁(Ⅱa类,证据级别B级)。无论血镁水平高低,静脉注射硫酸镁均是终止TdP的一线药物。以硫酸镁1~2g加入5%葡萄糖液稀释至10ml,5~20分钟注入,如果TdP发作仍持续,必要时可再重复静脉注射硫酸镁2g,方法同前。以后可以采用硫酸镁持续静脉滴注(2g硫酸镁加入100~250ml液体中),直至TdP消失。使用硫酸镁时一般不需监测血镁的水平。获得性LQTS致TdP往往合并低血钾。药物和低血钾协同可使TdP的发生率增加。因此积极补钾也是治疗措施之一;尽管支持的证据有限,仍建议将血钾水平保持至4.5~5.0mmol/L(Ⅱb类,证据级别C级)。抗心律失常药在获得性LQTS和TdP中的治疗价值有限。虽然有建议可以考虑使用利多卡因和美西律,但这不是治疗和预防的主要措施。
对心动过缓和明显长间歇依赖者可考虑经静脉心房或心室临时起搏,起搏频率维持80次/min左右,某些患者可能需要更快的频率,若有指征,应该进行永久起搏。
LQT1:运动及游泳是心脏事件常见的诱发因素,男性患者多在15岁前发病。因此,必须限制患者从事竞争性体育运动、游泳、潜水等。LQT2:运动中发病少见,夜间电话铃声、闹钟、警车及救护车声音是发病的常见诱因,需要避免。在就诊时,应告知患者避免使用导致QT间期延长并诱发TdP的药物,并告知其他相关的药物和潜在的药物相互作用的信息。应提供可延长QT间期作用的药物列表(www.qtdrugs.org),并在病例中记录药物获得性LQTS的病史。如果患者病史或家族史中出现过不明原因的晕厥或过早猝死,建议对所有的一级亲属进行12导联心电图检查,并应考虑进行先天性LQTS的基因检测。必要时应植入ICD预防心脏性猝死。













