英文名称 :infection of immunodeficiency patients
正常人具有物理和化学的屏障、非特异性免疫和特异性免疫功能以防御各种病原体的入侵。任何影响和损伤这些免疫功能的因素,皆可使人易于发生感染,称为免疫缺陷者感染(infection of immunodeficiency patients)。免疫缺陷有原发性(先天性)和继发性(获得性)之分,前者发病率低,其发病机制尚不能完全了解。近年来随着创伤性诊疗技术的广泛开展,尤其是实体器官移植、造血干细胞移植等新技术的开展以及免疫抑制剂在临床上的广泛应用,感染仍然是免疫缺陷者最常见的并发症及引起死亡的主要原因,也是临床诊治中的难题。本文重点介绍获得性免疫缺陷者感染,即由创伤、异物、营养不良、肿瘤和各种疾病、脾切除、药物和某些病原体等所致免疫缺陷而产生的感染。
(一)革兰阳性球菌感染增多
主要有凝固酶阴性葡萄球菌、链球菌属、金葡菌和肠球菌属等。增多的原因为:采用强化抗癌治疗、留置静脉导管的广泛应用、肿瘤患者化疗后常伴有口腔及上消化道黏膜破损、广泛采用抗生素预防等。
(二)革兰阴性杆菌感染中病原菌的变迁
大肠埃希菌、铜绿假单胞菌感染相对减少、克雷伯菌属、肠杆菌属、嗜麦芽窄食单胞菌和鲍曼不动杆菌增多。
(三)分枝杆菌属感染增多
除结核分枝杆菌外有非结核分枝杆菌如鸟分枝杆菌、龟分枝杆菌、偶然分枝杆菌、溶血分枝杆菌等。
(四)真菌(念珠菌属、曲霉、隐球菌属、镰刀霉属、耶氏肺孢子菌、毛孢子菌属等)
近年来接受非实体和实体器官移植的患者急剧增多,在器官移植受者中曲霉感染的发病率明显增高。据报道异体造血干细胞移植受者中曲霉感染发生率约5%~26%;实体器官移植,肝移植受者中为1%~8%,肺移植受者中为3%~14%,心脏移植受者中为1%~15%。
(五)其他
病毒(水痘-疱疹病毒、巨细胞病毒、肝炎病毒等)、寄生虫(弓形虫、粪类圆线虫等)等感染有所增多。据报道在异基因骨髓移植受者中弓形虫感染的发病率约占0.3%~7.6%,在肾移植受者中约占1.1%。在实体器官移植受者中奴卡菌感染的发病率约为0.6%。
(六)耐药菌增多
甲氧西林耐药金葡菌(MRSA)、耐青霉素肺炎链球菌、耐万古霉素肠球菌属、多重耐药肺炎克雷伯菌、肠杆菌属、假单胞菌属,并出现耐碳青霉烯类的假单胞菌属及不动杆菌属的病原菌,多重耐药结核分枝杆菌(尤其是艾滋病患者中)、耐阿昔洛韦疱疹病毒株等。
(一)皮肤黏膜的完整性受损
创伤、烧伤、各种导管放置、心瓣膜置换术等皆可引起局部防御屏障损害,导致其邻近部位寄殖病原微生物(如寄殖于皮肤的葡萄球菌属)或医院内耐药菌(如铜绿假单胞菌、大肠埃希菌、肠杆菌属、肠球菌属和不动杆菌属等)入侵形成感染。
(二)吞噬作用受损
由中性粒细胞缺乏或减少及巨噬细胞功能障碍(包括趋化性障碍、吞噬作用减弱和杀菌活性减低)所致。中性粒细胞减少症见于再生障碍性贫血、血液系统恶性疾病和肿瘤化疗后等;中性粒细胞功能不良见于蛋白缺乏所致的营养不良、系统性红斑狼疮、糖尿病、肝硬化和接受皮质激素治疗者。吞噬作用受损患者易发生条件致病菌如铜绿假单胞菌、大肠埃希菌、肺炎克雷伯菌、金葡菌、表皮葡萄球菌和有荚膜的细菌以及念珠菌、曲霉属等真菌的感染。
(三)细胞免疫缺陷
原发性细胞免疫缺陷者常在成年之前死于条件致病菌感染。临床所见多为继发性,如淋巴瘤患者、肿瘤患者接受放疗或化疗者、器官移植及应用免疫抑制剂者等,亦包括结核病、获得性免疫缺陷综合征(AIDS)等患者。细胞免疫缺陷者易发生细胞内细菌、真菌、病毒和原虫等感染。
1.细菌
李斯德菌属、布鲁菌属、军团菌属、结核分枝杆菌、鸟型分枝杆菌、麻风杆菌和星形奴卡菌等。
2.真菌
念珠菌属最常见;近年来曲霉感染也在增加,以烟曲霉为主;隐球菌属、肺孢子菌属也是淋巴瘤、AIDS等患者的重要致病菌。
3.病毒
单纯疱疹病毒、水痘-带状疱疹病毒、巨细胞病毒和乙型、丙型肝炎病毒等。
4.寄生虫
弓形虫长期以来被认为是免疫缺陷者感染的常见病原体,亦可发生于AIDS患者。播散型粪类圆线虫自身感染可并发于恶性肿瘤、麻风、结核等疾病或接受免疫抑制药物者。此外,尚有表现为腹泻的隐孢子虫病,以及贾第虫、溶组织内阿米巴原虫等原虫感染,皆可见于AIDS患者。
(四)体液免疫缺陷
主要为免疫球蛋白和补体缺乏,后者多为先天性。体液免疫缺陷者对有荚膜的细菌抵抗力减弱,缺乏产生炎症的调理素作用,或IgM形成减少,因而易发生肺炎链球菌、流感嗜血杆菌、脑膜炎奈瑟菌等感染以及某些病毒感染。
(五)肿瘤引致空腔器官阻塞
例如淋巴瘤患者可有腹腔淋巴结肿大引起胆管梗阻和胆管感染,支气管肺癌引起支气管腔阻塞和肺炎,前列腺癌可引起尿路阻塞和尿路感染。
各种不同类型免疫缺陷患者发生感染时的常见病原微生物见表1。
表1 不同类型免疫缺陷者感染的常见病原微生物
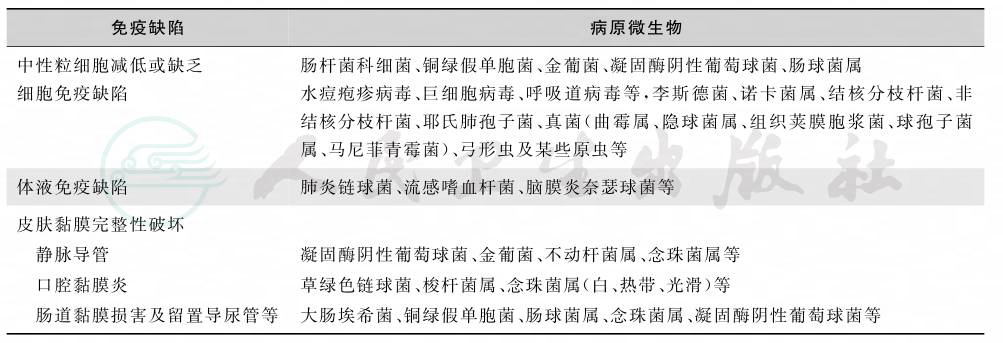
临床实际情况往往更为复杂,在同一免疫缺陷患者身上往往存在多种因素,例如人工器官移植使细胞免疫功能减低,但同时应用的大量免疫抑制药往往引起粒细胞减低,因而患者对感染更加易感。
(一)免疫缺陷者感染的治疗原则
1.尽早开始经验治疗免疫缺陷者出现发热,应首先考虑感染的可能。根据病史、体检和初步资料,采取相应的标本做病原检查;另一方面应争取时间尽早开始抗感染经验治疗。
2.根据检出的病原微生物和药敏试验结果调整用药。
3.选用的抗菌药物应具备的条件杀菌剂,对病原体有高度活性,在感染部位可达到有效浓度,毒性低,不易导致耐药菌出现。
4.抗菌药物宜静脉给药、足量近期的临床研究结果,对于低危的粒细胞减低发热患者(粒细胞减低持续时间在10天以内者),可以换用口服抗菌药。
5.在抗感染治疗期间若导管相关感染已成为感染源者,应尽早拔除导管。
6.尽可能纠正同时存在的免疫缺陷。
(二)肿瘤化疗后粒细胞减低患者的抗菌药物治疗
近年来由于肿瘤化疗趋向于强化治疗,以及骨髓移植术的广泛应用,患者经历的粒细胞减低期以及多种免疫功能缺陷的时间更加延长,使发生严重感染者增多。肿瘤或血液病患者经化疗后发生粒细胞减低和发热最为常见,而临床上有明显感染灶或病原检查呈阳性者仅占少数。临床实践证实此种患者在送验各种标本后,不失时机地开始抗菌药物经验治疗可使感染的发病率和病死率大幅度下降。
随着近年来许多具有广谱和强大抗菌活性的抗菌药物在临床上普遍使用,经验治疗方案趋向于:①某些病例可以单药治疗;②对低危患者可适当采用口服剂;③非细菌感染渐见增多,抗病毒药、抗真菌药及抗原虫药的应用增多。
1.首先评估患者发生严重感染的危险程度。通常分为:①高危患者:预期中性粒细胞减低持续7天以上,化疗后粒细胞数≤0.1×109/L,及(或)同时并发低血压、肺炎、腹痛或神经改变等症状。此类患者应收住入院并接受经验治疗。②低危患者:预期中性粒细胞减低持续时间少于7天,无活动性并发症,病情稳定,肝、肾功能良好。此类患者可采用口服抗菌药经验治疗。
2.高危患者应采用具有抗假单胞菌活性的β内酰胺类单药静脉给药,如头孢吡肟、一种碳青霉烯类(美罗培南或亚胺培南)或哌拉西林/他唑巴坦。有并发症时可根据情况加用氨基糖苷类、氟喹诺酮类及或万古霉素。
3.不推荐常规采用万古霉素或其他抗需氧革兰阳性球菌的药物,但可用于疑有导管相关感染、皮肤及软组织感染、肺炎或血流动力学不稳定等患者。
4.对于可能为下列耐药菌感染的患者,可加用:①MRSA感染加万古霉素或利奈唑胺或达托霉素。②VRE感染加用利奈唑胺或达托霉素。③产ESBLs革兰阴性菌感染尽早采用碳青霉烯类。产KPC等产碳青霉烯酶革兰阴性菌感染应及早采用多黏菌素或黏菌素或替加环素。
5.对青霉素有速发过敏反应史的患者应避免采用β内酰胺类药物,可考虑用环丙沙星联合克林霉素,或氨曲南联合万古霉素。
6.低危患者可采用住院口服或静脉用药经验治疗。临床情况许可时可转为门诊治疗。口服经验治疗可选用环丙沙星联合阿莫西林/克拉维酸,或环丙沙星联合克林霉素。
7.高危患者经广谱抗菌药治疗4~7天后仍持续发热而原因不明并粒细胞减低持续10天以上者可考虑加用抗真菌药,如两性霉素B或两性霉素B含脂类制剂。在一些曲霉和非白念珠菌感染较少的单位亦可用氟康唑。近期的研究显示伊曲康唑或卡泊芬净亦可用于经验治疗。
8.有明确感染的患者经验治疗的疗程依据感染部位和病原菌种类而定,疗程至少用至中性粒细胞数≥0.5×109/L或更长。发热病原不明者经验治疗应持续至有骨髓恢复迹象(中性粒细胞数>0.5×109/L)。经验治疗后明确的感染症状和体征已消散,但中性粒细胞减低仍持续者可给予预防性应用口服氟喹诺酮类(左氧氟沙星或环丙沙星),直至骨髓恢复。低危患者通常不需预防用抗菌药。
(三)造血干细胞移植和器官移植后感染的抗菌药物治疗
器官移植受者发生的感染是该类患者最常见的危及生命的并发症,发生感染主要取决于两种因素:①患者的免疫状态:免疫抑制剂的应用、皮肤黏膜完整受损、移植手术的创伤、坏死组织残留及积液等,同时存在的中性粒细胞减低、尿毒症、营养不良、糖尿病及可影响机体免疫功能的病毒感染等(如CMV、EBV、乙型及丙型肝病毒,HIV病毒等)均可影响患者的免疫状态;②医院及社区环境中潜在致病原的暴露程度:如各种呼吸道病毒、真菌、结核分枝杆菌、各种革兰阳性及阴性细菌等。
1.器官移植和造血干细胞移植后发生感染的时间规律
各种实体器官移植中采用的免疫抑制剂给药方案大致相似,主要为环孢素和他克莫司。因此各种移植术后发生感染的类型及时间规律基本一致。掌握这一时间规律有助于器官移植术后感染的鉴别诊断,判断患者周围环境中潜在致病原的存在,并采取积极有效的预防措施。
(1)术后1个月内发生的感染:在移植手术前应消除一切可能的感染,以减少移植后感染的危险性。在移植手术时应对移植物进行培养作为今后治疗的参考。术后1个月内发生的感染其中90%以上与免疫功能正常的患者外科手术后发生的感染相同,主要为医院获得的细菌或念珠菌感染。感染发生率与手术操作技术和术后护理有关,静脉导管和引流管的放置时间长,留置移植片固定膜,坏死组织及异物等都是引起感染的危险因素。但耶氏肺孢子菌、星形奴卡菌等机会致病原感染的可能性很小。
(2)术后1~6个月内发生的感染:曾接受肺孢子菌及抗病毒(CMV、HBV)预防用药者可发生多瘤病毒感染、艰难梭菌结肠炎、丙型肝炎病毒、腺病毒、流感病毒、新型隐球菌、结核分枝杆菌等感染。未接受过预防性抗菌药物者可发生肺孢子菌、疱疹病毒、CMV、EBV、乙型肝炎病毒及李斯特菌、奴卡菌、弓形虫、粪类圆线虫、利什曼原虫等感染。
(3)术后6个月以上发生的感染:社区获得性肺炎、曲霉、毛霉、奴卡菌、红球菌属、CMV、HBV、HCV、疱疹病毒、SARS等感染。
(4)感染类型的改变:近年来由于新的免疫抑制剂的应用以及抗菌药的预防性应用(TMP/SMZ预防肺孢子菌病、阿昔洛韦预防疱疹病毒感染等)使器官移植受者的免疫抑制状态有所改变,移植后发生的感染也有某些改变。移植后1个月内发生机会感染者少见,感染主要来自供者或与移植手术有关。病原菌以细菌和念珠菌为主,治疗应依据药敏试验的结果。移植后1~6个月发生的感染中肺孢子菌肺炎、李斯特菌、弓形虫、奴卡菌等感染和疱疹病毒感染减少,但可发生地方性真菌、曲霉、隐球菌、多瘤病毒、腺病毒、复发性丙型肝炎等。移植后6个月以上感染的危险性减少,但在肝移植受者中可发生丙型肝炎,肺移植后可发生细支气管阻塞、心脏移植受者可发生CMV病毒感染导致血管疾病或移植后淋巴增殖失调或皮肤癌等。
2.器官移植和造血干细胞移植后感染的抗微生物病原治疗
(1)原则:对确诊感染患者进行治疗,对器官移植受者普遍进行药物预防某种感染,对高危患者给予先发制治疗,重点在于后两者。
(2)预防用药:移植术后的头4~12个月内,每日口服SMZ-TMP 1片,主要对术后肺孢子菌病有预防作用,并可减少李斯特菌、星形奴卡菌和弓形虫感染,减少肾移植术后尿路感染。心脏移植术受者弓形虫血清试验呈阴性而供者为阳性时,也应给予抗菌药物预防。
(3)预先或先发治疗:CMV血清试验阳性的患者,因排斥反应而接受抗淋巴细胞抗体治疗时,可予以低剂量更昔洛韦治疗可能发生的CMV感染。
定期用微生物法或血清试验等监测患者呼吸道内曲霉定植及CMV病毒血症等存在,此时虽无临床症状,可预先给予相应治疗。
(4)不同微生物病原感染的治疗:见表2~表4。
表2 细菌感染的治疗
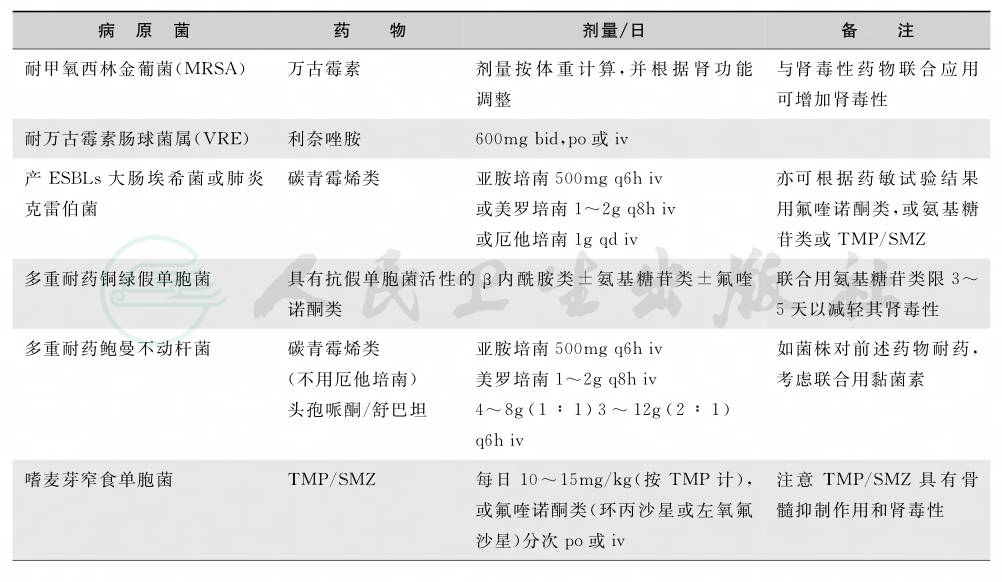
续表
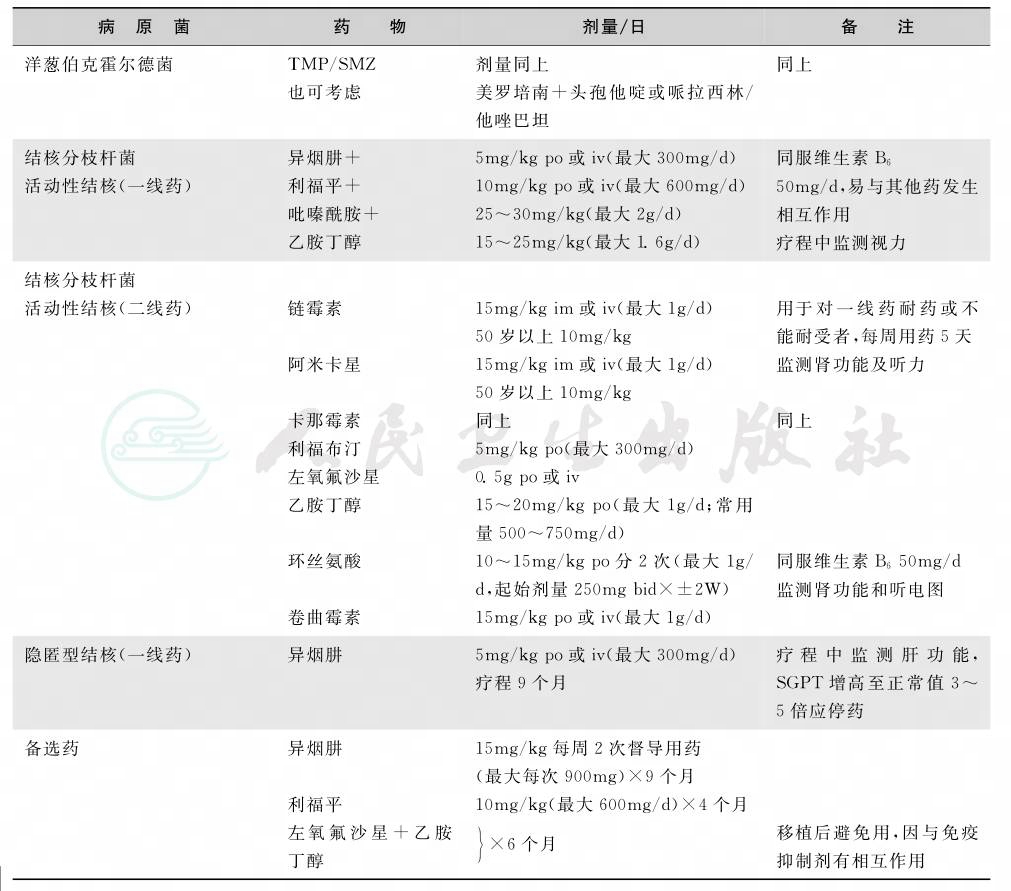
注:①活动性结核一线药用起始治疗2个月后,肺结核用异烟肼+利福平×4个月;播散性结核继续用7个月,中枢神经系统结核继续用7~10个月,应督导给药
②耐异烟肼TB用利福平(或利福布汀)+乙胺丁醇+吡嗪酰胺+氟喹诺酮×6个月
③耐利福平或利福布汀TB用INH+乙胺丁醇+氟喹诺酮+吡嗪酰胺×12~18个月,在起始治疗的头2个月加用一种氨基糖苷类,可缩短疗程至12个月
表3 病毒感染的治疗
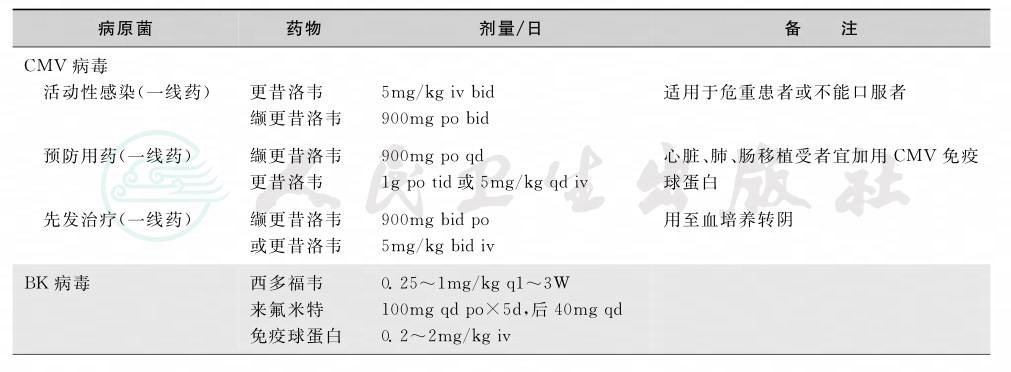
续表
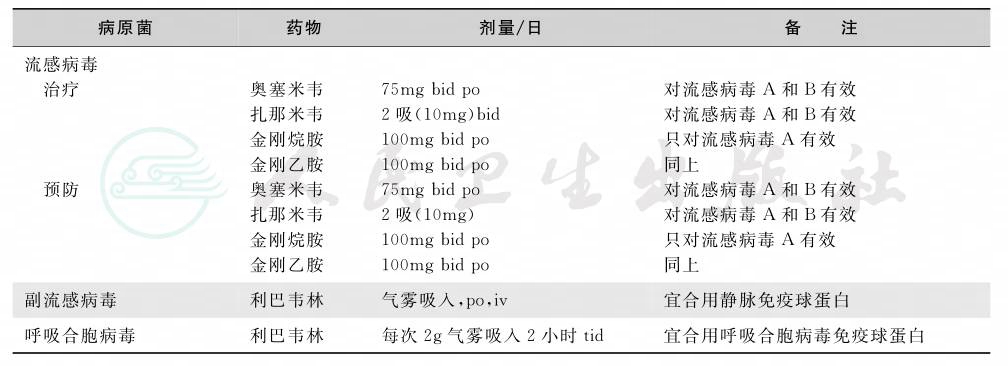
表4 真菌感染的治疗
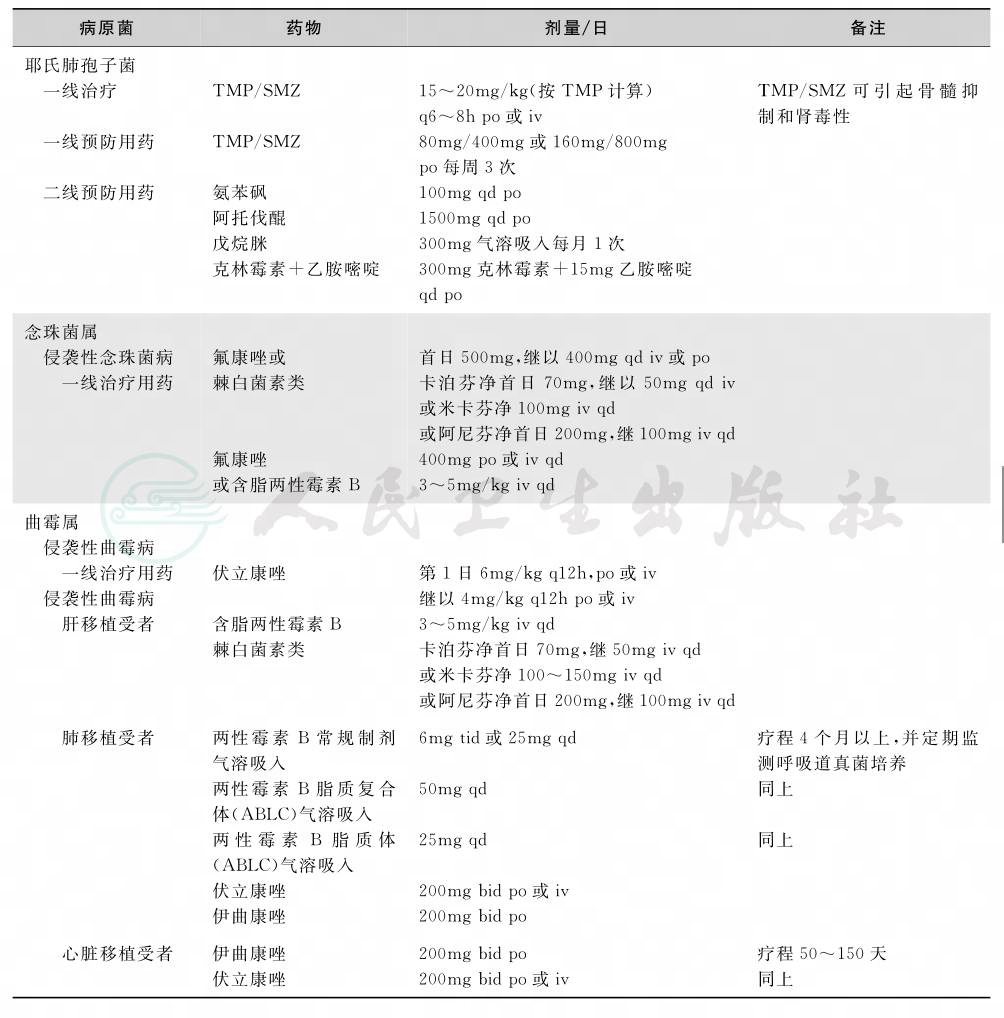
(5)造血生长因子的应用:造血生长因子如G-CSF,GM-CSF曾被用于粒细胞减低伴发热患者作为辅助治疗,对照研究结果显示用后可使患者粒细胞减低的时间缩短,但不能缩短发热和住院的时间和减少抗菌药物的应用,减低医疗费用或降低病死率等,因此不推荐常规应用于粒细胞减低伴发热患者的治疗。但估计骨髓造血功能短期内不能恢复,因而病情可能恶化的患者中可考虑应用。例如肺炎患者,出现低血压,严重鼻窦炎或蜂窝织炎的患者,系统性真菌感染及脓毒症引起多脏器功能衰竭等患者。目前不推荐常规应用中性粒细胞输入。
免疫缺陷者一旦发生感染治疗较困难,病死率高,故预防感染的发生极为重要,预防措施有下列几方面。
(一)严格掌握所有可能损伤防御功能的侵袭性诊治措施
各种导管(尤其是导尿管)应尽量少用,如应用应经常调换。可能导致菌血症或促使感染在局部播散的某些操作对免疫缺陷者更具有危险性;因此,各种内镜检查、血管造影、逆行胆管造影、膀胱镜检查和牙科操作等只能在有绝对指征时才使用,并必须做好严密消毒,在操作开始前0.5~1小时和操作后1~2天内给予适当抗菌药物。有关医务人员应严格执行消毒隔离制度。
(二)患者周围环境的消毒隔离
免疫缺陷者尤其是中性粒细胞严重减少者(低于1×109/L)应采取隔离措施,所有患者用水、饮食、医疗器械等皆须经过消毒。空气层流也可采用,但总的效果不明显。
(三)改善机体防御功能
应用免疫球蛋白、转移因子等,输入中性粒细胞、注射疫苗等。但中性粒细胞输入应有明确指征。许多免疫缺陷患者注射疫苗后并不能产生充分的免疫反应。
(四)抗菌药物的预防性应用
采用口服抗菌药物以消除患者自身的细菌、真菌等病原微生物,可用药物有新霉素、巴龙霉素、复方磺胺甲噁唑、氟喹诺酮类、甲硝唑以及制霉菌素等。但是预防用药后胃肠道反应多见,患者常难以完成疗程,过早停药后感染发生率反而升高,并易引起细菌产生耐药性,目前认为不是一种经济有效的措施。经临床验证对于免疫缺陷患者以及造血干细胞移植及实体器官移植患者机会菌感染有一定预防作用的方案有:
1.单纯疱疹病毒的预防
阿昔洛韦250mg,每12小时1次;或200mg,每日3次口服,疗程自准备期至移植物植入,或黏膜炎症消失。
2.移植器官巨细胞病毒检测阳性而器官移植受者阴性的患者预防移植后巨细胞病毒感染
更昔洛韦5mg/kg,每12小时1次,共7天,然后每日1次,每次5mg/kg,每周用药5~6天,均静脉滴注,疗程从移植物植入至移植后100天。
3.预防念珠菌属感染
氟康唑400mg,每日1次,口服或静滴;也可选择米卡芬净50mg,每日1次静脉滴注。
4.预防耶氏肺孢子菌感染
每日1次口服SMZ-TMP 1片(含SMZ 400mg,TMP 80mg),或每周口服3~7天,剂量同上。
5.预防弓形虫感染
心脏移植受者弓形虫血清试验呈阴性而供体为阳性时,应给予受者口服乙胺嘧啶,第一日,每次50~100mg,一日2次;继以每日25mg;联合磺胺嘧啶每日4次,每次1~1.5g,同时每日口服亚叶酸10mg,连续6个月。













