英文名称 :primary open angle glaucoma
中文别名 :慢性开角型青光眼;慢性单纯性青光眼
原发性开角型青光眼(primary open angle glaucoma,POAG)病因尚不完全明了,可能与遗传有关,其特点是眼压虽然升高房角始终是开放的,即房水外流受阻于小梁网-Schlemm管系统。组织学检查提示小梁网胶原纤维和弹性纤维变性,内皮细胞脱落或增生,小梁网增厚,网眼变窄或闭塞,小梁网内及Schlemm管内壁下有细胞外基质沉着,Schlemm管壁内皮细胞的空泡减少等病理改变。
青光眼治疗的目的是保存视功能。治疗方法包括:①降低眼压,由于眼压是相对容易控制的危险因素,目前对青光眼的治疗主要是通过药物或手术,将眼压控制在视神经损害不进一步发展的水平,即所谓目标眼压。目标眼压值因人因眼而异,视神经损害程度越重,其残余神经纤维对眼压的耐受性越差,因此其目标眼压值也相对较低。对晚期病例,要求眼压比一般水平更低,以防止病情进一步恶化。目标眼压还与视神经损害出现时的眼压水平、青光眼病情进展速度、患者的年龄及可能的寿命有关。除了眼压峰值外,昼夜眼压波动大也是导致病情恶化的危险因素,因此24小时眼压测量对于观察眼压控制情况也十分重要。由于眼压不是青光眼发病的唯一危险因素,部分患者在眼压得到控制后,视神经萎缩和视野缺损仍然进行性发展,因此目标眼压仅是一个相对安全眼压水平。②视神经保护性治疗,即通过改善视神经血液供应和控制节细胞凋亡来保护视神经。
(一)常用降眼压药
药物降低眼压主要通过3种途径:①增加房水流出;②抑制房水生成;③减少眼内容积。其中,通过增加房水流出降低眼压最符合正常房水生理功能的维持。
1.拟副交感神经药(缩瞳剂)
最常用为1%~4%毛果芸香碱(pilocarpine)滴眼液,每日3~4次,或4%毛果芸香碱凝胶,每晚1次滴眼。毛果芸香碱直接兴奋瞳孔括约肌,缩小瞳孔和增加虹膜张力,解除周边虹膜对小梁网的堵塞,使房角重新开放,为治疗闭角型青光眼的一线用药。对开角型青光眼,毛果芸香碱的降压机制为刺激睫状肌收缩,牵引巩膜突和小梁网,减小房水外流阻力,增加房水外流。但该药可引起眉弓疼痛、视物发暗、近视加深等副作用,若用高浓度制剂频繁滴眼,还可能产生胃肠道反应、头痛、出汗等全身中毒症状。
2.β-肾上腺能受体阻滞剂
常用0.25%~0.5%噻吗洛尔(timolol)、0.25%~0.5%盐酸左旋布诺洛尔(levobunolol)和0.25%~0.5%倍他洛尔(betaxolol)等滴眼液,每日1~2次滴眼。β-受体阻滞剂通过抑制房水生成降低眼压,不影响瞳孔大小和调节功能,但其降压幅度有限,长期应用后期降压效果减弱。噻吗洛尔和盐酸左旋布诺洛尔为非选择性β1、β2受体阻滞剂,对有房室传导阻滞、窦房结病变、支气管哮喘者忌用。倍他洛尔为选择性β1受体阻滞剂,呼吸道方面的副作用较轻。
3.肾上腺能受体激动剂
α2受体激动剂有0.2%酒石酸溴莫尼定(brimonidine),其选择性兴奋α2受体,可同时减少房水生成和促进房水经葡萄膜巩膜外流通道排出。酒石酸溴莫尼定对α1受体作用甚微,不引起瞳孔扩大,对心肺功能无明显影响。
4.前列腺素衍生物
目前已投入临床应用的制剂有0.005%拉坦前列素(latanoprost)、0.004%曲伏前列素和0.03%贝美前列素,其降眼压机制为增加房水经葡萄膜巩膜外流通道排出,但不减少房水生成。每日傍晚1次滴眼,可使眼压降低20%~40%。本药不影响心肺功能,副作用主要为滴药后局部短暂性烧灼、刺痛、痒感和结膜充血,长期用药可使虹膜色素增加、睫毛增长、眼周皮肤色素沉着。毛果芸香碱可减少葡萄膜巩膜通道房水外流,理论上与前列腺素制剂有拮抗作用,一般认为两者不宜联合用药。
5.碳酸酐酶抑制剂
以乙酰唑胺(diamox)为代表,每片0.25g,其通过减少房水生成降低眼压,多作为局部用药的补充。剂量不宜过大,可给0.125g,2次/天,或0.0625g,3次/天。久服可引起口唇、面部及指(趾)麻木、全身不适、肾绞痛、血尿等副作用,故不宜长期服用。目前已研制出碳酸酐酶抑制剂局部用药制剂,如1%布林佐胺(azopt),其降眼压效果略小于全身用药,但全身副作用也很少。
6.高渗剂
常用50%甘油(glycerin)和20%甘露醇(mannitol)。前者供口服使用,2~3ml/kg体重;后者静脉快速滴注,1~2g/kg体重。这类药物可在短期内提高血浆渗透压,使眼组织,特别是玻璃体中的水分进入血液,从而减少眼内容量,迅速降低眼压,但降压作用在2~3小时后即消失。高渗剂主要用于治疗闭角型青光眼急性发作和某些有急性眼压增高的继发性青光眼。使用高渗剂后因颅内压降低,部分患者可出现头痛、恶心等症状,宜平卧休息。甘油参与体内糖代谢,糖尿病患者慎用。
(二)常用抗青光眼手术
1.解除瞳孔阻滞的手术
如周边虹膜切除术(peripheral iridectomy)、激光虹膜切开术(laser iridotomy)。本手术的基本原理是通过切除或切开周边虹膜,使前后房沟通,瞳孔阻滞得到解除。术后前后房压力达到平衡,常常能有效地防止闭角型青光眼的再次发作。周边虹膜切除术、激光虹膜切开术主要适用于发病机制为瞳孔阻滞,房角尚无广泛粘连的早期原发性闭角型青光眼和继发性闭角型青光眼。
2.解除小梁网阻力的手术
如房角切开术(goniotomy)、小梁切开术(trabeculotomy)、选择性激光小梁成形术(selective laser trabeculoplasty,SLT)。房角切开术或小梁切开术分别从内面和外部切开发育不良或通透性不够的小梁网,房水能经正常途径引流至静脉系统,本类手术对于原发性婴幼儿型青光眼常常可达到治愈的效果。SLT应用激光激活小梁网内细胞,产生基质金属蛋白酶,降低细胞间机制,增加房水外流易度,达到降低眼压的目的,主要用于治疗早期POAG,或作为一种补充治疗用于药物治疗眼压控制不满意的POAG。SLT的远期降眼压效果不佳,但治疗可重复进行。
3.建立房水外引流通道的手术(滤过性手术)
如小梁切除术(trabeculectomy)、非穿透性小梁手术(nonpenetrating trabecular surgery)、激光巩膜造瘘术(laser sclerostomy)、房水引流装置植入术(implantation drainage device)。滤过性手术基本原理是切除一部分角巩膜小梁组织,形成一瘘管,房水经此瘘管引流到球结膜下间隙,然后再由结膜组织的毛细血管和淋巴管吸收,达到降低眼压的目的。
本类手术主要适用于POAG和有广泛房角粘连的闭角型青光眼。
4.减少房水生成的手术
如睫状体冷凝术(cyclocryotherapy)、睫状体透热术(cyclodiathermy)和睫状体光凝术(cyclophotocoagulation)。本类手术通过冷凝、透热、激光破坏睫状体及其血管,减少房水生成,以达到降低眼压、控制症状的目的。睫状体破坏手术主要用于疼痛症状较为显著的绝对期青光眼。
5.青光眼白内障联合手术
晶状体膨胀、位置前移是引起闭角型青光眼患者瞳孔阻滞的主要因素,去除晶状体因素可从发病机制上有效阻止闭角型青光眼的发生。
青光眼白内障联合手术适用于具有进行性的中等到严重青光眼视神经损害的青光眼患者,经两种以上抗青光眼药物治疗眼压控制在正常或临界水平的患者,对青光眼药物治疗依从性和随访条件较差的患者(不能应用和耐受),不具备行两期手术条件又迫切要求改善视力的患者,或者以前建立的滤过泡功能不良、眼压不能控制的患者。联合手术可减少与单纯白内障摘除有关的术后一过性眼压升高可能导致视功能不可逆性损害发生的危险。
(三)PACG的治疗
PACG眼压增高的原因是周边虹膜堵塞了房水外流通道,通过解除瞳孔阻滞或周边虹膜成型,加宽房角,避免周边虹膜与房水外流通道接触和粘连是主要治疗目的。
急性闭角型青光眼的基本治疗原则是通过药物、激光或手术的方式重新开放房角或建立新的引流通道。术前应积极采用综合药物治疗以缩小瞳孔,使房角开放,迅速控制眼压,减少组织损害。在眼压降低、炎性反应控制后手术效果较好。
1.缩小瞳孔
先兆期小发作时,用1%毛果芸香碱每半小时滴眼一次,2~3次后一般即可达到缩小瞳孔、降低眼压的目的。急性大发作时,每隔5分钟滴眼一次,共滴3次,然后每隔30分钟一次,共4次,以后改为每小时一次,如瞳孔括约肌未受损害,一般用药后3~4小时瞳孔就能明显缩小,可减量至一日4次。如眼压过高,瞳孔括约肌受损麻痹,或虹膜发生缺血坏死,则缩瞳剂难以奏效。通常在全身使用降眼压药后再滴缩瞳剂,缩瞳效果较好。如频繁用高浓度缩瞳剂滴眼,每次滴药后应用棉球压迫泪囊部数分钟,以免药物通过鼻黏膜吸收而引起全身中毒症状。
2.联合用药
急性发作期,除局部滴用缩瞳剂外,常需联合用药,如全身应用高渗剂、碳酸酐酶抑制剂,局部滴用β-受体阻滞剂以迅速降低眼压。
3.辅助治疗
全身症状严重者,可给予止吐、镇静、安眠药物。局部滴用糖皮质激素有利于减轻充血及虹膜炎症反应。
4.手术治疗
急性闭角青光眼缓解后,眼压可以保持较低水平数周,原因是睫状体缺血,房水分泌功能减退,因此这时眼压不是房角功能的好指标。应该向患者强调指出,经药物治疗眼压下降后,治疗尚未结束,必须进一步行手术治疗。术前应仔细检查前房角,并在仅用毛果芸香碱的情况下,多次测量眼压。如房角仍然开放或粘连范围<1/3周,眼压稳定在21mmHg以下,可做周边虹膜切除术或激光虹膜切开术,目的在于沟通前后房,解除瞳孔阻滞,平衡前后房压力,减轻虹膜膨隆并加宽房角,防止虹膜周边部再与小梁网接触(图3)。如房角已有广泛粘连,应用毛果芸香碱眼压仍超过21mmHg,表示小梁功能已遭永久性损害,应做滤过性手术。
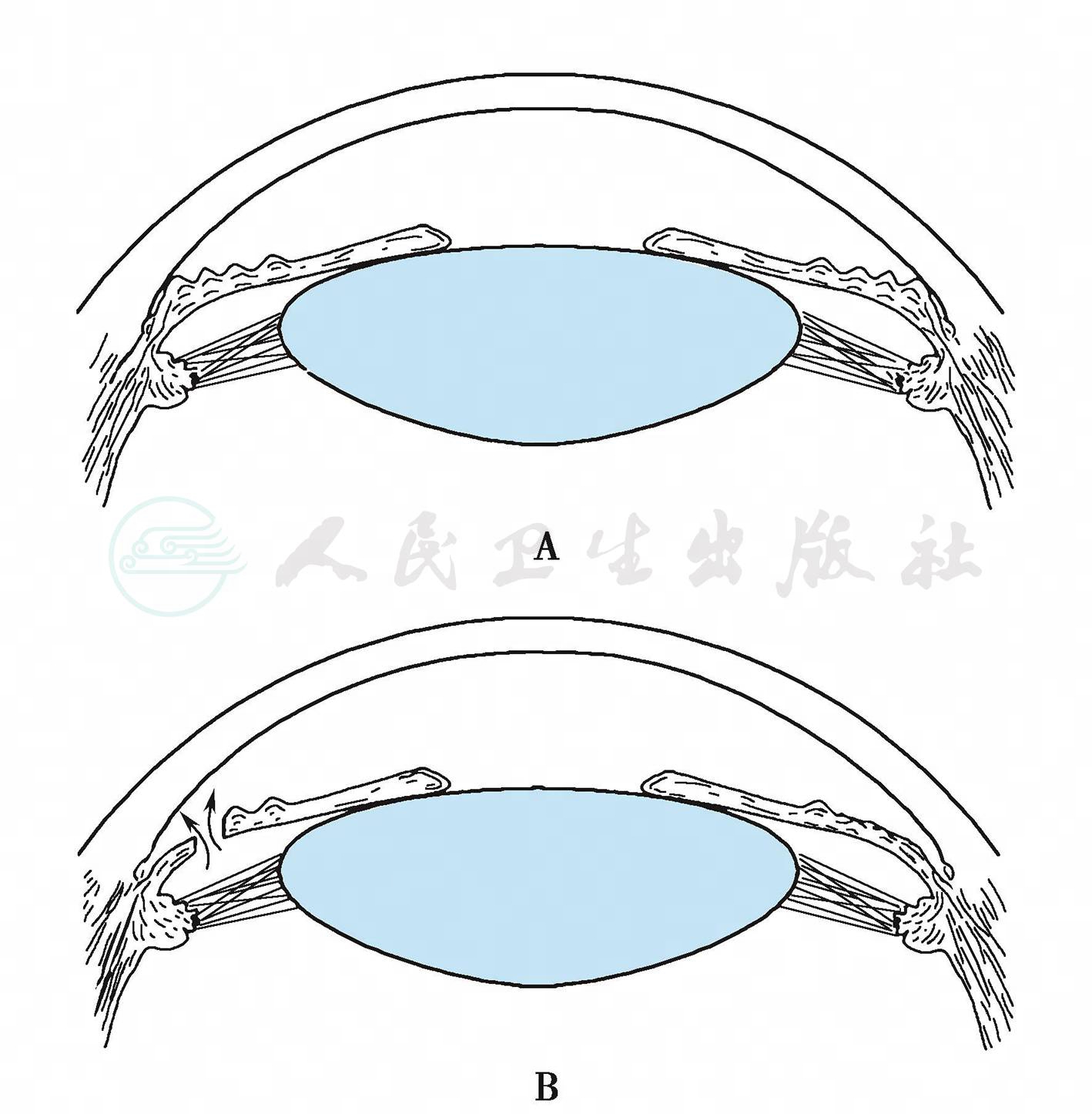
图3 急性闭角型青光眼周边虹膜切除术原理示意图
A:急性闭角型青光眼周边虹膜切除术前,虹膜膨隆堵塞小梁网,房角关闭;B:周边虹膜切除术后,膨隆消除,房角增宽。
临床上极少数病例虽然联合用药,但眼压仍居高不下,可在药物减轻角膜水肿的情况下,考虑激光周边虹膜成形术和激光虹膜切开术以迅速解除瞳孔阻滞。如果激光虹膜切开术不能实施,也可试行前房穿刺术,防止持续性过高眼压对视神经产生严重损害。
临床前期如不予治疗,其中40%~80%在5~10年内可能急性发作。长期使用毛果芸香碱不一定能有效地预防急性发作,因此对于具有虹膜膨隆、浅前房、窄房角的临床前期患者,应早期做预防性周边虹膜切除术或激光虹膜切开术。
慢性闭角型青光眼的治疗原则也是通过药物、激光或手术的方式控制眼压,达到保护视神经的目的。由于慢性闭角型青光眼瞳孔阻滞因素不明显,周边虹膜切除术不如在急性闭角型青光眼那样有针对性。但周边虹膜切除术后,对防止长期滴用毛果芸香碱可能引起的瞳孔阻滞有帮助,在一定程度上也可防止或减慢房角的进一步粘连。因此周边虹膜切除术可用于存在瞳孔阻滞,房角粘连范围不大,单用缩瞳剂即能控制眼压的早期病例。对于非瞳孔阻滞机制性慢性闭角型青光眼,单用周边虹膜切除术往往不能阻止房角进行性关闭,应采用氩激光周边虹膜成形术,以加宽房角。对大部分房角已有广泛粘连,单用缩瞳剂眼压不能控制,或已有明显视神经损害的慢性闭角型青光眼患者,需行滤过性手术。
(四)POAG的治疗
1.药物治疗
POAG眼压升高的主要原因是小梁网通透性降低。增加小梁网房水外流的药物如缩瞳剂,可针对病因进行治疗,但缩瞳剂的副作用限制了其在POAG的应用。尽管通过减少房水生成来降低眼压并非病因治疗,但由于房水生成抑制剂副作用较少,故在临床上应用更广泛。前列腺素衍生物增加房水经葡萄膜巩膜通道排出,也是目前治疗POAG的重要药物。若局部滴用1~2种药物即可使眼压控制在安全水平,患者能配合治疗并定期复查,则可先试用药物治疗。如无禁忌证,目前国际和国内的青光眼指南均推荐前列腺素类药物为一线用药。一种药物不能控制眼压,可换用另一种药物。如滴用单一药物眼压仍未控制在安全水平,可联合用药,两种药物滴眼应间隔10分钟以上。滴药后压迫泪囊区或闭合眼睑1~2分钟有助于维持局部药物浓度并减少全身吸收。
2.激光治疗
如药物治疗不理想,可试用选择性激光小梁成形术(SLT)。
3.滤过性手术
小梁切除术是最常用的术式。一般认为手术适应证是药物治疗无效或无法耐受长期用药,或没有条件进行药物治疗的病例。近来有人主张一旦诊断明确,且已有明显视盘、视野改变时,滤过性手术可作为首选的治疗手段,并认为早期手术比长期药物治疗失败后再做手术效果更好。
(五)难治性青光眼的治疗
难治性青光眼(refractory glaucoma)一般指那些药物难以控制眼压,而做常规手术预后不好的青光眼,如既往滤过性手术失败的青光眼、青少年型青光眼、无晶状体性青光眼、有较长期用药历史的青光眼、新生血管性青光眼以及某些继发性青光眼。难治性青光眼常规滤过性手术之所以难以控制,是因为存在以下复杂因素:①多次手术失败的青光眼患者可能属于对创伤有超强愈合反应的个体;②青少年多具有肥厚的眼球筋膜和活跃的创伤愈合反应;③无晶状体性眼的玻璃体可释放成纤维细胞刺激素,促使瘢痕形成;④新生血管性青光眼术后滤过道常有新生血管及血管性结缔组织膜生长,使其阻塞;⑤炎症尚未完全平静的葡萄膜炎继发性青光眼,术后组织反应强烈,血-房水屏障破坏,纤维连接蛋白和生长因子释放,可激活成纤维细胞增生,使滤过道瘢痕化。
为了提高难治性青光眼的手术成功率,可在术中或术后应用抗代谢药(如丝裂霉素-C、5-氟尿嘧啶)以抑制成纤维细胞的增殖,也可采用房水引流装置,如Molteno装置、Ahmed青光眼阀门,由一硅胶管将房水引流至安置于眼球后方的盘片下,形成一个“房水蓄积池”,最后房水扩散至眼球后部组织并被毛细血管和淋巴管吸收。
(六)视神经保护性治疗
青光眼以视神经节细胞进行性死亡为特征,研究表明节细胞死亡机制为凋亡。眼压升高或视神经缺血是青光眼发病的始动因素,而自由基、神经营养因子的剥夺、眼内兴奋性毒素——谷氨酸增多,可能是节细胞凋亡的激发因子。因此除了降眼压外,合理的青光眼治疗应包括视神经保护性治疗。目前正在从中和凋亡激发因素,开发外源性和内源性神经营养因子,基因治疗和神经再生或移植诸方面进行研究,以控制节细胞凋亡,达到保护视神经的目的。
钙离子通道阻滞剂、谷氨酸拮抗剂、神经营养因子、抗氧化剂(维生素C、维生素E)以及某些祖国医药可从不同环节起到一定的视神经保护作用。β1受体阻滞剂倍他洛尔,除降低眼压外,尚可增加视神经血流量,α2受体激动剂酒石酸溴莫尼定也有一定神经保护作用。













