英文名称 :renal parenchymal hypertension
肾实质性高血压(renal parenchymal hypertension)是由各种肾实质病变引起的高血压。2018年欧洲高血压协会/欧洲心脏病协会(ESH/ESC)数据显示:肾实质疾病占高血压病因的2%~10%,在40岁以下继发性高血压中居首位,且合并慢性肾脏病(CKD)的高血压患者其难治性高血压、隐匿性高血压和夜间血压升高更常见,更易合并相关靶器官损害。2012年我国CKD流行病学调查资料显示:肾小球滤过率(GFR)<60ml/(min·1.73m2)的患者60.5%伴有高血压,有白蛋白尿的患者61.2%具有高血压。
肾实质性高血压易引起严重心、脑血管并发症。文献报道,CKD合并高血压患者的心血管不良事件发生率为40.6%,而正常血压的CKD患者心血管不良事件发生率仅为13.3%。Keith等长期随访研究也显示CKD患者死亡事件主要与心血管并发症相关,仅少部分进展至终末期肾病(ESRD),故高血压在CKD患者心血管并发症中无疑扮演着重要角色。另外,肾实质性高血压也能促进CKD进展,导致ESRD。所以,肾实质性高血压应早期实施干预,将血压控制达标,保护心脑肾靶器官。
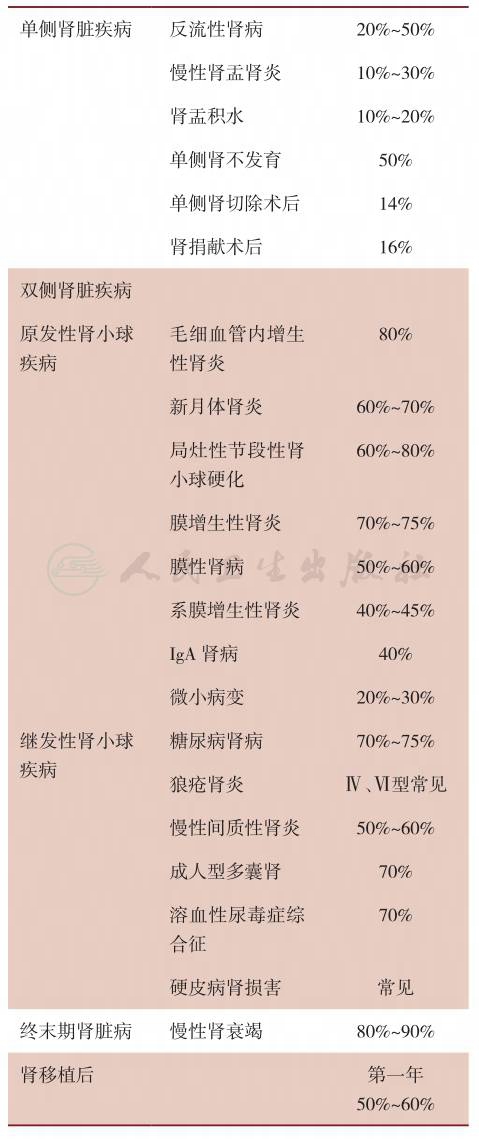
肾实质性高血压在不同CKD中发病率有所不同。一般来说,肾小球疾病及多囊肾高血压发病率高于慢性间质性肾炎;而在肾小球疾病中,病理呈增殖性和/或硬化性病变者高血压发病率较高,临床上肾功能损害重者高血压发病率较高(表1)。
表1常见引起肾实质性高血压的疾病
(一)细胞外液过多
透析前患者因GFR下降,存在显著的水钠潴留,细胞外液增加,从而引起高血压。多项研究发现,在大多数接受维持性血液透析患者中,细胞外液增多是引起高血压的重要原因。调整透析超滤量来控制细胞外液容量以及限制膳食中钠摄入量可以控制血压。容量超负荷常见于腹膜透析治疗,系残余肾功能丧失,腹膜超滤失败,及患者依从性差而造成,当这些患者从腹膜透析改为血液透析时,随着多余容量的清除,体重和血压在3个月内会显著下降。
(二)肾素-血管紧张素-醛固酮系统活化
肾实质病变时缺血可激活肾素-血管紧张素-醛固酮系统(RAAS)系统,造成循环RAAS活化,肾脏局部RAAS以及醛固酮活化。血管紧张素Ⅱ(AngⅡ)不仅与血管壁上AT1受体(AT1R)结合发挥缩血管作用,还能与近端、远端肾小管及集合管上AT1R结合,增加钠离子(Na+)重吸收,从而增加血容量,加重高血压。
(三)交感神经系统活化
交感神经系统活化在肾实质性高血压发病中起着重要作用。肾实质病变时,肾交感神经活化。激活的交感神经系统释放去甲肾上腺素等介质,刺激血管收缩,增加血管阻力;并可直接增加肾小管对钠重吸收,增加血容量,加重高血压。
(四)内皮素合成增加
内皮素是1988年分离得到的一个血管活性肽,它能通过自分泌、旁分泌或内分泌作用参与肾实质性高血压形成。肾实质疾病时,内皮素水平可升高,进而与血管平滑肌上A型受体(ETAR)结合,导致肾及外周血管收缩,增加血管阻力,造成肾实质性高血压。
(五)内源性类洋地黄物质
1980年Curber等报道盐负荷狗血浆提取物能抑制钠泵,并能与地高辛抗体发生交叉反应,因此该因子被称之为内源性类洋地黄物质,实际上就是内源性哇巴因。肾实质疾病导致水钠潴留,细胞外容量膨胀时,能反馈刺激下丘脑组织释放哇巴因。循环中增多的哇巴因抑制血管平滑肌细胞钠泵,使细胞内外Na+/K+交换减少,细胞内Na+浓度增高,Na+依赖性钙离子(Ca2+)流出减弱,细胞内Ca2+浓度增高,刺激血管平滑肌收缩,增加血管阻力,诱发高血压。
(六)一氧化氮生成减少
内皮细胞中的氧化亚氮合成酶(NOS)能催化L-精氨酸生成一氧化氮(NO)。NO可拮抗血管收缩因子,舒张血管平滑肌,减少外周血管阻力;NO还参与肾脏压力-排钠(pressurenatriuresis)效应,减少肾小管Na+、水重吸收,降低血容量。而肾实质性病变导致血管内皮受损,NOS活性降低,NO产生减少,引起血管收缩及水钠潴留,发生高血压。
(七)花生四烯酸代谢紊乱
前列腺素控制血压主要部位在阻力性小动脉和肾脏。前列腺素E2(PGE2)和前列环素(PGI2)能舒张小动脉,降低周围血管阻力,从而降低血压;PGE2能与髓袢升支粗段上的受体EP3结合,抑制Na+重吸收,PGI2也具有类似作用,故能减少水钠潴留,降低血压。肾实质性疾病时花生四烯酸代谢紊乱,PGE2及PEI2生成减少,从而引起高血压。
积极治疗肾实质性高血压对于减少心脑血管并发症、延缓肾功能损害进展以及降低死亡率具有重要意义。一体化的治疗不仅包括生活方式的干预,更要注重降压药物的选择、联用,以期达到血压靶目标。
一、降压目标值——变迁及思考
(一)CKD高血压的降压目标值
肾实质性高血压的降压目的在于降低尿蛋白排泄、延缓肾功能损害进展及预防心血管事件发生,最终降低全因死亡率,这就必须降压达标。不同指南对CKD高血压降压目标值的推荐并不一样,而且在不断调整。最初的降压目标值主要来自于1997年美国“肾脏病膳食改良研究”(MDRD研究)获得的结果,该研究显示:尿蛋白>1g/d的CKD患者,宜将血压控制在16.63/9.98kPa(125/75mmHg)以下;而尿蛋白<1g/d的患者,宜将血压控制在17.29/10.64kPa(130/80mmHg)以下。这一目标值已被写入世界卫生组织及国际高血压联盟(WHO/ISH)1999年制定的高血压指南。
但是,2003年美国高血压国家联合委员会公布的第7次报告(JNC7)并没有根据患者尿蛋白量进行分层,而将高血压的降压目标统一定为17.29/10.64kPa(130/80mmHg)以下;2004年美国肾脏基金会(NKF)所属“肾脏病预后质量倡议”组织(K/DOQI)发布的CKD高血压指南,也推荐糖尿病及非糖尿病的CKD高血压患者应将血压降到17.29/10.64kPa(130/80mmHg)以下;2007年ESH/ESC高血压指南也推荐,伴有脑卒中、心肌梗死、糖尿病、肾功能不全或蛋白尿的高危/极高危高血压患者应将血压降至17.29/10.64kPa(130/80mmHg)以下。这些指南都没有再推荐把血压降至16.63/9.98kPa(125/75mmHg)以下。
2012年国际“改善全球肾脏病预后”组织(KDIGO)制定的CKD高血压指南建议,对于糖尿病及非糖尿病的CKD患者,尿白蛋白排泄率<30mg/d时,降压目标值为18.62/11.97kPa(140/90mmHg)以下;而尿白蛋白排泄率≥30mg/d时,降压目标值为17.29/10.64kPa(130/80mmHg)以下。2013年的ESH/ESC高血压指南推荐,CKD、糖尿病、心脑血管疾病患者的降压目标值均为18.62/11.97kPa(140/90mmHg)以下,不过当CKD患者出现明显蛋白尿时仍宜将收缩压降至17.29kPa(130mmHg)以下。2014年美国的JNC8认为没有证据显示将CKD高血压降到17.29kPa(130mmHg)以下会比降到18.62/11.97kPa(140/90mmHg)以下更加获益,因此该指南就只推荐将CKD高血压降至18.62/11.97kPa(140/90mmHg)以下。2017年AHA高血压指南建议CKD高血压应降至17.29/10.64kPa(130/80mmHg)以下。2018年中国高血压防治指南建议,合并CKD的高血压患者无白蛋白尿时血压可控制至18.62/11.97kPa(140/90mmHg)以下,有白蛋白尿者需将血压控制至17.29/10.64kPa(130/80mmHg)以下。2018年ESH/ESC高血压指南推荐在所有CKD患者中首先将血压降至18.62/11.97kPa(140/90mmHg)以下,若治疗可耐受则在大多数患者中血压需降至17.29/10.64kPa(130/80mmHg)以下。
上述各家指南的建议都可供我们临床实践参考,但是2012年KDIGO在CKD高血压指南中提出的降压目标值可能对我们临床实践的参考意义更大。
(二)CKD高血压老年患者的降压目标值
针对老年高血压患者血压波动大,“晨峰”现象多,易出现直立性低血压,并常伴发冠心病、心力衰竭和脑血管疾病等特点,指南均强调老年人的降压目标值不能与年轻人相同。但是目前并没有针对CKD高血压老年患者降压目标值的循证研究,所以只能从一般老年高血压患者降压目标值的研究获得启示。
2008年日本进行的一项关于老年患者血压控制靶目标值的随机对照试验(JATOS研究)发现:降压目标值控制在18.09~18.22kPa(136~137mmHg)之间的患者与控制于18.89~19.29kPa(142~145mmHg)的患者比较并无更多收益。2009年ESH/ESC指南再评价指出,将老年高血压患者的降压目标值定为收缩压降至18.62kPa(140mmHg)以下,并没有循证医学依据。2008年国际多中心HYVET研究显示,年龄≥80岁的老年高血压患者将血压控制达19.95/10.64kPa(150/80mmHg)水平就能获益。2010年中国高血压指南建议,65岁以上的老年患者宜将收缩压控制至19.95kPa(150mmHg)以下,若能耐受还可以进一步降低,达18.62kPa(140mmHg)以下,但是大于80岁的患者将血压降达18.62kPa(140mmHg)以下能否更多获益尚不清楚。2013年ESH/ESC高血压指南内容与我国指南推荐收缩压≥21.28kPa(160mmHg)的老年患者应予治疗,并将收缩压降到18.62~19.95kPa(140~150mmHg)水平,而年龄小于80岁且能很好耐受的患者还可考虑将血压降至18.62kPa(140mmHg)以下。2014年美国JNC8指南推荐≥60岁的一般高血压患者应将血压降至19.95/11.97kPa(150/90mmHg)以下。2017年AHA指南推荐对于≥65岁并伴有多种合并症且预期寿命有限者,降压目标可根据临床情况、患者意愿和基于团队的方法进行风险/获益评估后做出决定。2018年ESH/ESC高血压指南建议对于老年(>65岁)高血压患者收缩压降至17.29~18.62kPa(130~140mmHg),舒张压降到10.64kPa(80mmHg)以下。2018中国高血压防治指南建议对于老年患者需根据合并症的严重程度,对治疗耐受性及坚持治疗的可能因素进行评估,综合决定患者降压目标。对于老年高血压患者,所有指南都强调个体化制定治疗方案及降压目标非常重要,降压不宜过快,尽量避免将血压降得过低或诱发直立性低血压,以免诱发严重心,脑血管事件。
2018年《中国高血压防治指南》及2018年ESH/ESC高血压指南建议的降压目标值可能对于临床更有参考价值。
(三)过度降压与J形曲线现象
1987年Cruickshank等提出高血压患者在降压治疗中可能出现J形曲线现象,即随着血压下降患者心血管疾病死亡率也下降,但是血压降到一定程度后若继续降低,则心血管疾病死亡率反而会上升。J形曲线的观点在理论上应能成立,但是多年来在积极倡导和鼓励降压治疗的背景下并未被充分重视。ESH/ESC指南对J形曲线阐述最多,但是在他们不同时期的指南所表明的观点仍有所差异。2007年ESH/ESC指南阐述:某些事后分析(post-hoc analysis)怀疑血压下降程度与患者死亡率之间存在J形曲线,此J形曲线现象仅发生在血压下降至远低于目标值时。2009年ESH/ESC指南再评述对此作了更清楚的阐述:基于某些临床试验及事后分析,过度积极降压似乎已有所收敛,目前尽管证据尚弱,但已有试验提示当血压降达15.96~16.63/9.31~9.98kPa(120~125/70~75mmHg)以下时,已很难进一步获得器官保护效益,却可能诱发J形曲线现象。可是2013与2018年ESH/ESC公布的指南在阐述J形曲线现象上,观点似乎没有2009年那么明朗。两份指南均认为,从病理生理角度J形曲线现象可能存在,但是欲用临床试验去提供证据却相当困难。迄今的临床试验有的支持,有的否定J形曲线现象,而且各试验获得的曲线“低谷值”(血压低于此值危险即开始增加)更是差别甚大。因此,指南提出在J形曲线现象上,是否可能患者的基础危险因素比过度降压更重要?今后需要设计更为合理的试验去进行进一步研究。
不同的高危患者对降压的耐受性确实可能不同。已有临床试验显示,冠心病患者若将血压降达9.31~7.98kPa(70~60mmHg)以下有可能增加心肌梗死及全因死亡的风险;而慢性脑卒中患者并无证据显示将收缩压降达17.29~15.96kPa(130~120mmHg)以下能更多获益。在临床治疗CKD合并心、脑血管病变的高血压患者时,上述资料可供参考。
二、降血压药物合理选择——应关注的几个问题
(一)第一线降压药物
1999年以前的高血压治疗指南均推荐ACEI、ARB、钙通道阻滞剂(CCB)、β受体拮抗剂、α受体拮抗剂及利尿剂等6种药物作为降压治疗的第一线用药。2003年后,ESH/ESC高血压治疗指南及美国JINC7只推荐ACEI、ARB、CCB、β受体拮抗剂及利尿剂等5种药物作为第一线用药;而2006年英国国家卫生与临床优化研究院(NICE)制定的高血压指南及2014年美国的JNC8却只推荐ACEI、ARB、CCB及利尿剂4种药物作为第一线用药。
美国JNC8不再推荐α受体拮抗剂作为第一线降压药物的主要原因是,ALHHAT研究显示与利尿剂相比,α受体拮抗剂治疗组患者发生脑卒中及复合心血管疾病的风险显著增加;不再推荐β受体拮抗剂作为第一线降压药物的主要原因是,LIFE研究显示与ARB相比,β受体拮抗剂治疗组患者达到心血管病死亡、脑卒中及心肌梗死原发复合终点的比例显著增高。
但是,要强调的是未被推荐作为第一线降压药的药物,临床仍然可使用,在第一线药物联合治疗效果不佳时,可配合第一线降压药应用。
(二)降压药物的联合应用
由于肾实质性高血压降压达标比较困难,因此联合用药相较于单一用药显然更受推崇。Corrao等的调查表明,与单一用药相比,联合用药血压控制好,心血管事件发生率低、不良反应少,并且患者的失随访率也显著下降。因此,2007年ESH/ESC高血压指南推荐,对于较重(≥2级)的高血压患者或合并心脑血管疾病、肾脏病或糖尿病的高危和极高危患者,从治疗开始即采用药物联合治疗。2014年美国JNC8虽然没有推荐在治疗之初联合用药,但是对药物联合治疗的重要性仍十分强调。
那么应该如何进行药物联合治疗呢?两药或多药联用时,作用机制应具有互补性,降压效应能叠加,而且不良反应能抵消或减轻。近年国内、外高血压指南在治疗CKD高血压时,都一致推荐ACEI或ARB作为联合用药的基石药物,这与它们有显著的器官保护效应相关。指南还推荐ACEI或ARB应首先与利尿剂和/或CCB联合治疗,疗效不佳时再加用其他降压药物。ACEI或ARB与噻嗪类利尿剂联用时,后者激活RAAS的不良效应能被ACEI或ARB抵消,而利尿剂排钠又能增强ACEI或ARB的降压疗效;ACEI或ARB与双氢吡啶类CCB联用时,前者通过拮抗血管紧张素Ⅰ作用扩张血管,后者通过阻滞血管平滑肌细胞的钙离子流入使血管扩张,两药协同能显著增强降压疗效。
但是,利尿剂与β受体拮抗剂联合应用有增加新发糖尿病可能,必须警惕。另外,2013年ESH/ESC高血压指南及2014年美国JNC8都已明确提出不主张ACEI与ARB联合应用,如此联用虽可能增强降低尿蛋白效果,但会引起急性肾损伤等严重副作用。
(三)肾功能不全对降压药物药代动力学的影响
凡是经肾脏排泄为主的降压药物均需参考肾功能状态调整用药,包括减少每次剂量或延长给药时间。具体应用时可以查阅药物学或肾脏病学的相关书籍或手册,这里拟对这4种第一线降压药的用药调整作一简述:
(1)ACEI类:
仅福辛普利是经肝肾双通道排泄,而且肾功能损害时,肝脏排泄会代偿性增多,所以只有GFR≤10ml/min时才需适当减量,而其他所有ACEI都是以肾脏排泄为主,它们都需要在肾功能损害的较早时期减量。
(2)ARB类:
都是经肝肾双通道排泄,且以肝脏排泄为主,故肾功能损害时无需调节用药。
(3)CCB类:
均以肾外清除为主,肾功能损害时无需调节用药。
(4)利尿剂:
当血清肌酐(SCr)≥159μmol/L(1.8mg/dl)时,噻嗪类利尿剂即失去利尿作用,其利尿作用减弱;但噻嗪类利尿剂直接参与肾脏、内皮、血管反应,减少外周血管抵抗从而扩张小血管;间接通过对心排量快速下降的慢反馈减少外周血管抵抗,可降低高血压患者的心因死亡率,同时增加其他降压药物的效用;故噻嗪类利尿剂随着GFR下降其利尿之外的血管内皮保护作用愈发显著。而氯噻酮是以肾脏排泄为主,肾损害早期即应延长给药时间,GFR≤50ml/min时即应停用。
不能应用上述利尿剂时可改用小剂量袢利尿剂。
(四)血液净化对于降压药物药代动力学的影响
肾脏病进行血液净化治疗时许多药物的药代动力学也会发生改变,因此用药需要调整,尤其是能被血液净化清除的药物,需要在血液净化结束后补充给药,否则会显著降低药物疗效。
一般而言,药物能否被血液净化清除取决于如下因素:
(1)药物蛋白结合率:
药物的分子量较小(一般小于500Da,很少大于1 500Da),故游离状态很容易被血液净化清除,但是当它们与分子量较大的血浆蛋白结合后,则很难被清除,因此药物的蛋白结合率是决定其能否被血液净化清除的最重要因素。
(2)药物的表观分布容积(Vd):
代表药物在体内组织分布的广泛程度。不同个体间Vd存在差异,Vd≤1L/kg时药物易被清除,而≥2L/kg时则清除困难。蛋白结合率低的高Vd药物,仍能被血液透析清除,使透析后血药浓度明显下降;但是在两次透析间期,组织中的高浓度药物又会迅速进入血液,致使血药浓度迅速回升。
(3)血液净化治疗方式:
高通量膜及延长透析时间会增强药物清除;连续性肾脏替代治疗(CRRT)对高Vd药物的清除效力远较一般透析高。
这里拟对血液净化治疗清除几种常用降压药的情况作一简述:
(1)ACEI类:仅贝那普利及福辛普利的蛋白结合率高(均达95%)不被血液透析清除,无需透析后追加给药,而其他ACEI均能被透析清除,需要透析后追加给药。
(2)ARB类:蛋白结合率均高(厄贝沙坦90%,缬沙坦94%~97%,氯沙坦、替米沙坦、奥美沙坦及坎地沙坦均高达99%),不能被血液透析清除,无需透析后追加给药。
(3)CCB类:蛋白结合率也均很高(氨氯地平95%,硝苯地平97%,贝尼地平>98%,非洛地平99%),不能被血液透析清除,无需透析后追加给药。
三、维持性血液透析患者的降压治疗——问题与思考
高血压在维持性透析患者中发生率高达80%~90%,而且是脑血管疾病、冠心病及充血性心力衰竭的重要危险因素,与疾病不良结局密切相关,因此需要予以治疗。但是,近年一些大样本的临床研究结果却显示,不是血压较高,而是血压较低,与血液透析患者的不良结局相关,为此已有学者提出血透高血压患者进行降压治疗到底是有利还是有害的质疑,这说明血液透析患者的高血压治疗,与非透析患者不同,有其特殊性,需要深入研究。
目前至少有如下问题值得考虑:①血液透析患者的血压判断应以OBP还是应以ABPM为准?血液透析患者透析前后的血压波动常较大,若测量OBP,那又应以透析前还是透析后血压为准?到目前为止,仅某些临床研究是用ABPM来观察透析患者的血压变化,而临床上仍在用OBP测量血压,既然透析前后血压波动较大,那么透析前后的血压都应关注。②有临床观察显示,血液透析患者透析前低收缩压及透析后高舒张压能显著增加死亡率,如果这观察正确,那么血液透析患者透析前应避免过度降压(部分患者需在透析前暂停降压药),而透析后应努力避免高舒张压发生(掌握好脱水程度,透后追加降压药物等)。③血液透析患者透析前后的血压应控制到什么程度?这很重要,过高或过低都对靶器官不利,这目标值尚待确定。目前某些研究推荐透析前血压宜降至<18.62/11.97kPa(140/90mmHg),透析后血压宜降至<17.29/10.64kPa(130/80mmHg),可供参考。④控制透析患者的高血压同样需要综合治疗,包括改变生活方式、实施透析及服用降压药等。但是需要强调的是,透析干体重达标是有效降压的基础,超滤脱水达到干体重能使85%~90%患者的高血压得到控制。不过某些透析患者的降压效果会延迟出现,在脱水至干体重后不能及时见效,需要数周至数月高血压才能被有效控制。⑤应注意透析对降压药物的清除(详见前述),能被清除的降压药一定要在透析后追加给药,否则也可导致透析后血压增高。
2012年KDIGO发布的CKD高血压指南,仍没有对血液透析患者的高血压治疗提出建议。指南解释这是因为许多问题目前尚未明确,例如血透患者的血压应如何测量、血压高低与不良结局到底存在什么联系、相互牵连的影响血压的各种复杂因素又在如何起作用等。所以KDIGO工作组认为目前对血透患者的高血压治疗提出指南性意见尚为时过早。由此看来,对维持性血透患者进行合理的降压治疗,还有许多问题需探索。
四、肾脏去神经支配术——现状与前景
经导管去肾脏交感神经术(catheter-based renal denervation)可作为顽固性高血压治疗的一种备选治疗策略,适用于在生活方式调整和药物治疗后未达到降压目标的耐药性高血压患者。2013年欧洲心血管学会(ESC)制定的经导管去肾神经支配术专家共识认为满足如下标准的患者适宜接受此治疗:①诊室血压≥21.28kPa(160mmHg)[糖尿病患者标准为≥19.95kPa(150mmHg)];②调整生活方式及足量使用3种或更多抗高血压药物(包括利尿剂)治疗无效;③已排除继发性高血压;④通过动态血压检测已排除假性顽固性高血压;⑤GFR ≥45ml/(min·1.73m2);⑥无肾极动脉(指不经肾门而入肾实质的动脉,又称副动脉),无肾动脉狭窄,无肾动脉重建史。肾脏去神经支配术可能通过降低外周阻力、减少肾素释放以及改善水钠潴留而达到降压目的,在治疗顽固性高血压方面有良好应用前景。
CKD可引起交感神经活化,而交感神经活化又在CKD进展中具有重要作用,因此肾脏去神经支配术对CKD高血压治疗可能具有一定益处。尽管目前已有应用此治疗的初步研究,但是其确切疗效及安全性仍需更大样本临床试验验证。目前,2018年ESC指南不推荐将肾脏去神经支配术用于高血压患者的常规治疗中。













