英文名称 :Invasive breast cancer
中文别名 :浸润性乳腺癌
所谓浸润性癌是指乳腺癌细胞穿破基底膜侵入至间质内生长,临床检查乳腺内可扪及边界不清、质地较硬的肿块。切面常为灰白色、放射状侵入间质,并可发生淋巴道转移。多数浸润性乳腺癌(invasive breast carcinoma)表现为可触及的肿物和/或乳腺X线摄影、超声检查的异常。有些肿瘤可表现为隐匿性,临床仅为淋巴结肿大和/或出现远处转移为首发症状。
常见的浸润性乳腺癌组织学类型
(一)浸润性导管癌,非特殊型
浸润性导管癌,非特殊型(invasive ductal carcinoma,no special type,IDC-NST)是乳腺癌中最常见的亚型,占浸润性乳腺癌的40%~75%。这是一组异质性肿瘤,它们在形态学、临床表现及预后方面均有不同。IDC-NST常因临床扪及肿物和X线摄影或超声检查被发现。
【诊断要点】
①肿瘤大小差异显著,病变呈不规则星芒状或结节状;边界不清,无包膜;通常实性质硬,刀切有砂粒感,切面灰白伴黄色条纹。②浸润性导管癌虽然缺乏可以用于分类的特殊组织形态学,但在生长方式、细胞学形态、增殖活性及伴发原位癌级别及范围等方面不尽相同。其生长方式可为丛状、小梁状、条索状。异质性在同一肿瘤内也很显著。③在浸润性癌成分确定困难时,可行免疫组化染色辅助标记肌上皮,如p63、calponin、平滑肌肌球蛋白重链、CD10、S-100证实肌上皮细胞消失。因不同的肌上皮标记具有不同的敏感性和特异性,建议联合应用。鉴于p63核阳性的稳定表达和管腔周的线性排列,SMMHC平滑肌肌球蛋白重链标记与乳腺间质成纤维细胞的交叉反应小,可优先选择上述两种肌上皮标记。
ESBR分级系统是判断预后的重要分级系统(图1)。
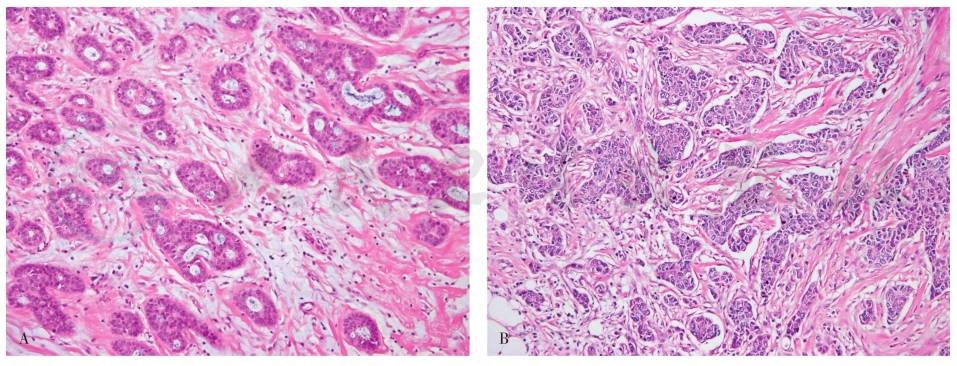
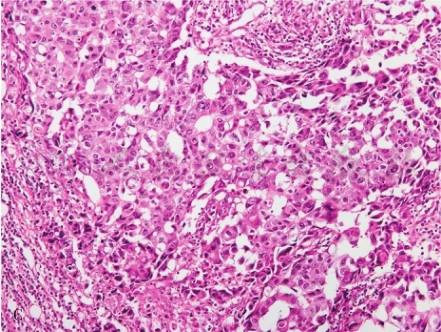
图1浸润性导管癌
A.ESBR分级1级;B.ESBR分级2级;C.ESBR分级3级。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
(二)特殊组织学类型
1.浸润性小叶癌(invasive lobular carcinoma,ILC)
是浸润性乳腺癌中第二常见的类型,占所有浸润性癌的5%~15%。常表现为同侧多灶性或双侧发生的病变。ILC患者临床可触及团块,但更多的时候也是在乳房X线摄影或超声检查时发现。ILC与IDC-NST的临床特征具有差异:前者较少发生实质脏器(肺、肝和脑)转移,更易转移至卵巢、腹膜、胃肠道及骨等,部分转移癌在腋窝淋巴结转移中常见孤立肿瘤细胞模式(不同于肿瘤细胞簇状侵及被膜下淋巴窦)。故发生在卵巢的以印戒细胞形态为主的转移性癌,除考虑胃肠来源的印戒细胞癌外,还需鉴别诊断乳腺来源ILC。
【诊断要点】
ILC肿物形态大体上可与IDC相似。部分病例也可仅表现为坚韧、难以推动的乳腺包块。有时病变乳腺未见显著的大体改变,只能通过镜下观察发现肿瘤。
ILC有独特的形态学及间质浸润方式:单个细胞散在分布或呈单列线状列兵样排列的肿瘤细胞,也可围绕正常导管呈同心圆/靶样生长。肿瘤细胞的浸润未见显著促纤维组织增生的间质反应。经典型ILC由均匀一致、失黏附性、体积小的肿瘤细胞构成,核小而均一,位于细胞的一侧,有时可见胞质内腔,核分裂象少见。ILC的特殊亚型与经典型在结构或细胞形态上存在差别:印戒细胞亚型由大量核偏位印戒样形态的细胞组成;实性和腺泡型的肿瘤细胞聚集呈球状生长,被纤维间质分割;多形性亚型的肿瘤细胞异型性大、具有显著多形性,且核分裂象更多见。
IHC染色显示80%~95%的ILC表达ER,60%~70%表达PR,HER2扩增或HER2过表达很少见。
ILC转移病灶形态类似原发性小叶癌,需要结合临床相关病史及IHC辅助诊断(图2)。经典型ILC预后好于多形性ILC及IDC-NST。
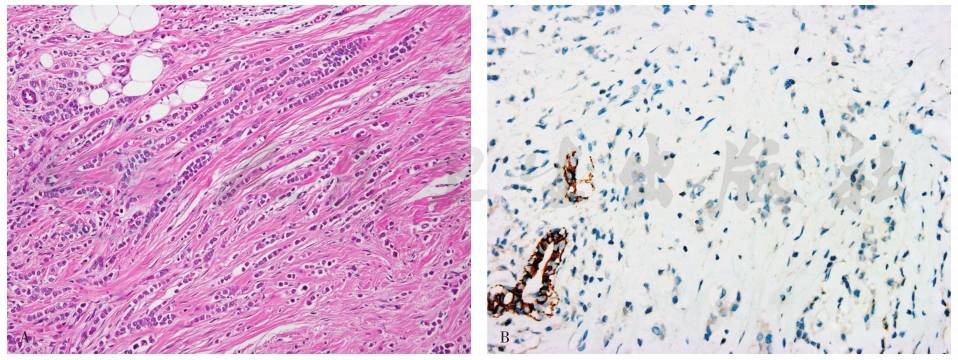
图2浸润性小叶癌
A.浸润性小叶癌(经典型);B.免疫组化示浸润性小叶癌E-cadherin(-),周围乳腺导管E-cadherin(+)。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
【鉴别诊断】
①具有ILC形态的浸润性导管癌(表1);②反应性增生的组织细胞/炎细胞;③淋巴造血系统肿瘤。
表1浸润性小叶癌与浸润性导管癌免疫组化鉴别诊断

引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
2.小管癌(tubular carcinoma)
占浸润性癌的2%,常因乳腺X线摄影筛查发现,局部复发及远处转移率少,具有相对较好的预后。
【诊断要点】
①大体表现为边界欠清的质硬包块。②成角的腺管无序排列,腺管由单层上皮细胞围绕形成,尖端呈角,管腔开放,可见细胞的顶浆突起(图3),胞核呈椭圆形伴轻至中度的异型性。癌组织具有富于细胞的促纤维增生性间质。③免疫组化显示小管癌缺少肌上皮细胞,可将此肿瘤与良性硬化性乳腺病变(硬化性腺病、放射状瘢痕、复杂性硬化性病变)相区别。肿瘤几乎总是表达ER及PR,HER2常阴性。④腋窝淋巴结转移少见,体积大的肿瘤可出现少数Ⅰ/Ⅱ级腋窝淋巴结转移。
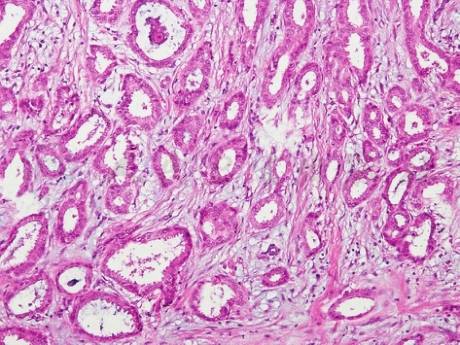
图3小管癌
腺体成角浸润,管腔开放,细胞嗜酸性或嗜双色性,可见顶浆突起。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
【鉴别诊断】
①硬化性腺病:具有小叶结构轮廓,腺体受压变形,硬化性腺病存在肌上皮细胞,免疫组化染色可证实。②放射状瘢痕:病变可见纤维化和弹力纤维变性,肌上皮标记有助于与小管癌的鉴别诊断。③微腺性腺病:腺管小而圆,弥漫浸润性生长,腔内含有胶样分泌物是其特征形态;微腺性腺病缺乏成角的形态,缺乏顶浆突起有提示作用。免疫组化示微腺性腺病S-100阳性、p63阴性、EMA阴性及AE1/AE3阳性。
3.黏液癌(mucinous carcinoma)
单纯性黏液癌是低度恶性的乳腺癌,是指肿瘤≥90%区域具有细胞外黏液成分,且细胞外黏液占据肿瘤1/3。该亚型占所有浸润性癌的1%~6%,淋巴结转移率低,预后较好。黏液癌可与浸润性导管癌混合存在,预后取决于浸润性导管癌成分。
【诊断要点】
①肿物呈局限性生长,推挤状,质软,切面呈凝胶样,伴光泽感。②肿瘤细胞呈巢状,并被纤细的富含毛细血管的纤维分隔,漂浮于细胞外的黏液湖中(图4)。多数病例细胞核级低。③老年女性患者,粗针穿刺组织乳腺间质中出现黏液湖,需要警惕黏液癌的可能性,建议手术切除肿物。④IHC:p63染色显示肌上皮消失,可以与黏液囊肿样病变鉴别。多于90%的肿瘤ER、PR表达阳性,少见HER2过表达。部分黏液癌可有神经内分泌分化。⑤特殊染色:黏液湖AB染色(+)。
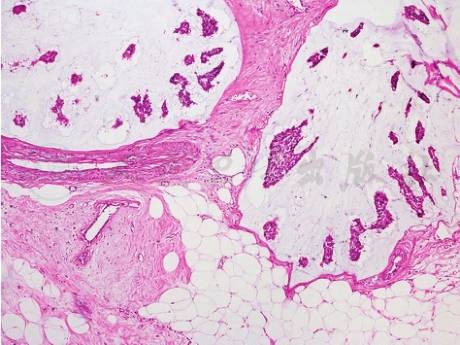
图4黏液癌
肿瘤细胞团漂浮于黏液湖中。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
【鉴别诊断】
①黏液囊肿样病变;②隆乳异物反应。
4.伴有髓样特征的癌
经典髓样癌(medulllary cacinoma)不足所有浸润性癌的1%。好发于年轻女性,临床表现为可触及的肿物。在乳腺X线摄影中为边界清楚的肿物。髓样癌和伴有髓样特征的癌有相关性,常具有BRCA1 DNA修复基因的家族性突变。
【诊断要点】
①肿瘤表现为边界清楚,质软,棕褐色或灰红色的结节。切面呈膨胀性生长方式。肿瘤可伴有出血坏死,部分病例可出现囊性变。②显微镜下(图5)合体细胞结构在肿瘤组织中的比例大于75%;有弥漫的淋巴细胞、浆细胞间质浸润;有推挤性边缘;有高级别多形性泡状核(核级2或3);无腺管分化。③通常ER阴性、PR阴性及HER2无蛋白过表达和基因扩增(三阴性肿瘤)。④与同级别的非特殊类型的浸润性乳腺癌相比单纯性髓样癌预后良好。
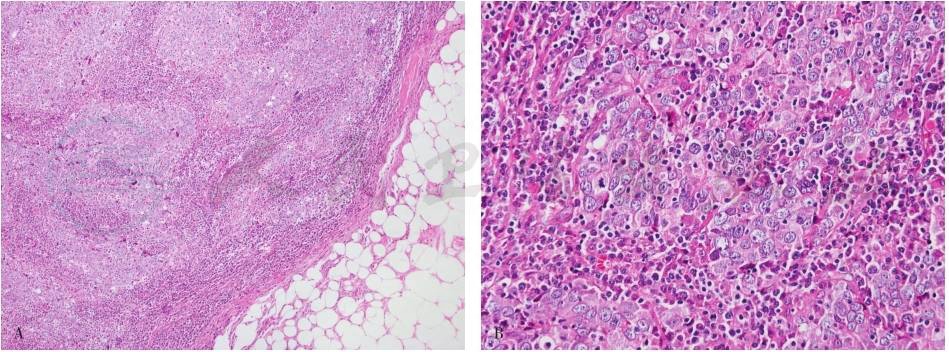
图5伴有髓样特征的癌
A.肿瘤具有推挤性边缘;B.肿瘤细胞由合体样细胞组成。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
【鉴别诊断】
①缺乏上述所有组织学标准的浸润性癌现被认为是非典型髓样癌/伴有髓样特征的癌,在日常外检这些特殊形态的癌常被过诊为髓样癌,导致患者缺乏合理的治疗,而发生早期复发和转移;②淋巴造血系统肿瘤。
5.浸润性微乳头状癌(invasive micropapillary carcinoma)
单纯型浸润性微乳头状癌指>75%的肿瘤成分表现为微乳头状结构。该亚型占浸润性癌的0.9%~2%。浸润性微乳头状癌可与浸润性导管癌和黏液癌混合存在。
【诊断要点】
①簇状、腺样或微乳头状肿瘤细胞团位于纤维间质组成的腔隙内(图6A),腔隙内不见黏液性物质。②微乳头状结构缺乏典型的纤维血管轴心。③EMA显示微乳头外侧缘阳性(图6B),证实肿瘤极向翻转。④肿瘤ER、PR阳性表达率不一。需要注意在评价HER2蛋白表达时肿瘤细胞膜虽然未呈闭环状完整着色,存在一定程度的不连续性和间断性,但强而厚的细胞膜棕褐色染色应等同于完整的细胞膜染色。⑤认识这种癌的重要性在于此型淋巴管血管侵犯、腋窝淋巴结转移率和复发性均较其他亚型显著增高。多数研究者提出不论浸润性微乳头状癌的比例,只要该种成分出现,就应体现在病理报告中。
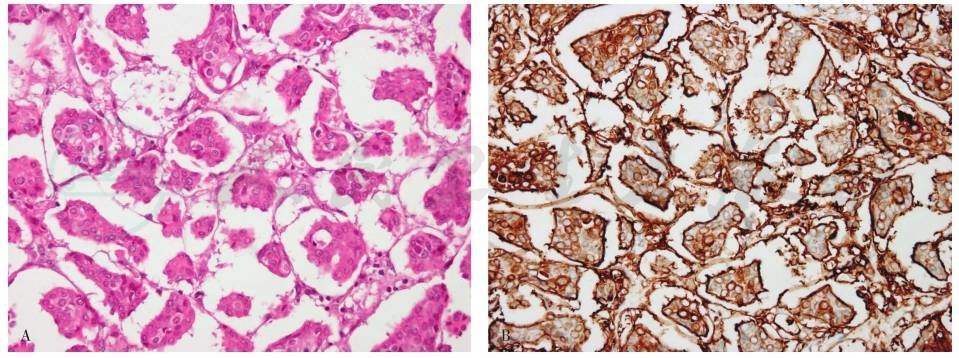
图6浸润性微乳头状癌
A.微乳头状肿瘤细胞团位于纤维间质组成的腔隙内;B.免疫组化示肿瘤乳头外侧缘EMA(+)。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
【鉴别诊断】
①非特指浸润性导管癌伴有间质收缩裂隙;②微乳头状结构的黏液癌;③伴有微乳头状结构的转移性卵巢癌、肺及尿路上皮癌。
6.化生性癌(metaplastic carcinoma)
少见,占乳腺浸润性癌的0.2%~5%。这是异质性成分很高的一组肿瘤,肿瘤内可见上皮-间质相互移行转化:非腺性上皮(鳞状细胞、梭形细胞)或间叶细胞(软骨细胞、骨细胞、横纹肌细胞)类型。
【诊断要点】
除肿瘤体积较大,其余大体表现与非特殊型浸润性导管癌相似。鳞状细胞癌可表现为囊性肿物。
低级别腺鳞癌由成角的轻度异型腺体和灶状鳞状分化细胞团组成,排列无序伴浸润性生长,腺体内可见充满角化物的微囊。
化生性梭形细胞癌(图7)由转化的梭形细胞组成,其组织学可仅表现为轻度细胞异型,如纤维瘤病样梭形细胞癌。当肿瘤内合并腺管结构明显时,诊断相对容易;但当腺管样结构缺乏时,诊断需要辅助IHC染色多种细胞角蛋白(如MNF116和高分子量/基底细胞型角蛋白抗体CK34βE12)及肌上皮标记p63,肿瘤旁导管原位癌区域也对诊断具有提示作用。
间叶分化的混合性化生性癌最常见的是灶状区域向软骨样/软骨黏液样基质或骨样基质分化;其他类型的间叶细胞分化如纤维肉瘤、横纹肌肉瘤也可见到。
因为单纯的肌上皮癌在组织学形态和免疫表型方面与梭形细胞化生性癌无显著区别,已将其归入化生性癌的其中一种亚型。
>90%的化生性癌成分ER、PR及HER2表达为阴性,但是腺管结构生物学标记的表达不一。
预后较好的化生性癌亚型见于纤维瘤病样化生性癌、低级别腺鳞癌;梭形细胞癌具有相对较低的淋巴结转移率,但是易出现淋巴血管侵犯,总体预后差。
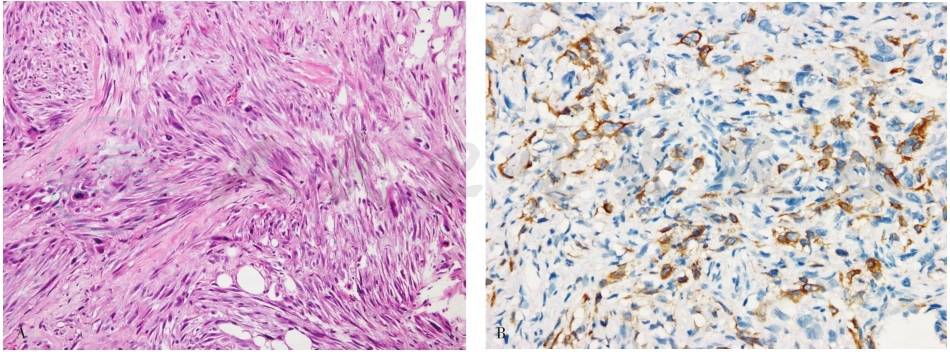
图7梭形细胞癌
A.肿瘤细胞呈梭形组织学形态;B.免疫组化示肿瘤细胞MNF116(+)。
引自:临床病理学(第2版)(国家卫生健康委员会住院医师规范化培训规划教材).第2版.ISBN:978-7-117-31663-7.主编:
【鉴别诊断】
①皮肤来源鳞状细胞癌。②原发性或转移肉瘤:乳腺原发肉瘤极其罕见,以梭形细胞形态为主的乳腺恶性肿瘤,在诊断前应排除化生性癌。多种上皮性标记及p63在化生性癌中阳性表达。③恶性叶状肿瘤。
7.炎症性乳腺癌(inflammatory carcinoma)
是一种临床-病理结合性的诊断性病变类型,临床表现为弥漫性红疹、硬化及乳房皮肤压痛,超过1/3的乳腺皮肤出现水肿,且与非凹陷性水肿(橘皮征)相关。
【诊断要点】
①特定的临床表现和/或伴有肿物。②炎症性乳腺癌的临床表现与皮肤淋巴管血管内的肿瘤栓子形成,阻塞脉管相关。不伴有皮肤改变的真皮内淋巴管癌栓的发现不能用于诊断炎症性乳腺癌。③炎症性乳腺癌的诊断不是病理学诊断,是与临床表现密切相关的肿瘤名称。在乳腺癌分期中,炎症性乳腺癌归为T4d期,是预后极差的肿瘤。
8.其他少见类型的乳腺癌
腺样囊性癌、筛状癌、肌上皮癌、皮脂腺癌、富于脂质癌、富于糖原透明细胞癌、腺泡细胞癌及浸润性大汗腺癌。













