英文名称 :primary central nervous system lymphoma
原发性中枢神经系统淋巴瘤(primary CNS lymphoma, PCNSL)是相对少见的颅内肿瘤,占颅内原发肿瘤的0.8%~1.5%,WHO Ⅲ~Ⅳ级。命名之初,较为复杂,包括网状细胞肉瘤、软脑膜肉瘤,淋巴肉瘤、组织细胞性淋巴瘤、血管外皮肉瘤、混合性肉瘤、小胶质细胞瘤、混合性血管肉瘤等。脑内原发性淋巴瘤均为非霍奇金淋巴瘤,是少见肿瘤,但是近年来由于艾滋病(又名获得性免疫缺陷综合征,acquired immunodef i ciency syndrome, AIDS)及器官移植术后服用大量的免疫抑制剂患者的增多,淋巴瘤的发生率逐年增加。原发性中枢神经系统淋巴瘤的发病在无免疫系统缺陷的人群时,好发于40~70岁,平均发病年龄为40岁左右,而具有机体免疫抑制和艾滋病患者的发病年龄高峰在30~40岁,发病率男性高于女性。
脑部原发性淋巴瘤起源于脑内何种细胞尚不十分清楚,有学说认为起源于多能干细胞,常离心性播散,从血管周围浸润进入相邻的脑实质,肿瘤也可侵透血管壁进入管腔内,从而造成血-脑屏障的破坏。CT和MRI增强检查时的造影剂外渗,形成病灶的显著强化,而未被完全破坏的血-脑屏障的破坏。CT和MRI增强检查时的造影剂外渗,形成病灶的显著强化,而未被完全破坏的血-脑屏障部分则强化较轻,这一影像表现支持上述的学说。
典型的原发性中枢神经系统淋巴瘤是小病灶性淋巴细胞聚集于血管周围,大多数为B细胞型淋巴瘤,T细胞型淋巴瘤极少发生。
PCNSL由Bailey于1929年以“血管周围肉瘤”首次报告,目前已认识到其细胞来源是恶性淋巴细胞。过去通常认为先天性或获得性免疫缺陷是患PCNSL的危险因素,如HIV感染者面临更大危险,其发病率是健康人群的3600倍。但近年来发现免疫正常人群的发病率也明显增加,其原因不详。一些研究发现 PCNSL与 EB病毒(EBV)感染有关,但Tandon等采用原位杂交技术检测了19例免疫正常的PCNSL患者的标本,结果EBV全部阴性,该研究提示EBV并不是普通人群PCNSL发病的主要病因。
淋巴结或淋巴组织遍布全身各脏器或组织,但在CNS内并无淋巴组织,也无淋巴循环,PCNSL是通过怎样一种机制发病,目前仍不清楚。相关的主要有以下几种学说:①CNS内的原位淋巴细胞恶性克隆增生。②肿瘤细胞来源于全身系统中的淋巴细胞,此种淋巴细胞有嗜中枢性而在CNS异常增生。③血-脑屏障“庇护所”效应可能为恶性淋巴瘤细胞的浸润提供了一个“庇护所”。④与先天性或获得性免疫缺陷有关,PCNSL易发于三类免疫缺陷患者:艾滋病 (AIDS)、接受器官移植及免疫抑制治疗者、有遗传性免疫缺陷及其他获得性免疫缺陷者。在免疫系统功能缺陷患者中,以病毒感染学说较受重视,主要由EB病毒感染引起,疱疹病毒等亦可能促发淋巴瘤。⑤在CNS炎症发生后,淋巴细胞易被CNS捕获,然后经某致病原刺激后发生了恶性转化。这些学说均需进一步研究证实。
近几年学者们在PCNSL的遗传学方面的研究中,为其发病机制提供了科学依据。有学者发现,在PCNSL中原癌基因c-MYC和PIM-1的表达比结内淋巴瘤明显上调,能在PCNSL发病机制中起到重要的作用。国外学者通过研究发现在PCNSL中p14 ARF(56%)和pl6 INK4a(61%)的纯合子缺失或启动因子超甲基化是最常见的异常。抑癌基因的失活和原癌基因的突变对PCNSL的发生有一定作用。
PCNSL可以发生于任何年龄,发病高峰为45~70岁,10岁以下很少见;好发于男性,男女比例 (2~3)∶1。本病占非霍奇金淋巴瘤的1%~2%,占中枢神经系统 (central nervous system,CNS)原发肿瘤的3%~10%。先天性、后天获得性 (如AIDS)或医源性 (如器官移植)免疫系统缺陷患者是原发性中枢神经系统淋巴瘤的好发人群。原发性中枢神经系统淋巴瘤占先天性免疫抑制患者肿瘤约4%,占艾滋病患者的3%。近年文献资料表明,所有淋巴结外淋巴瘤呈不均衡的上升趋势,以脑部和眼部淋巴瘤最为突出。美国国立癌症研究机构的资料数据库显示:在正常免疫力的人群当中,1982-1984年与1973-1975年比较,PCNSL发病率上升了3倍,而1992年与1973年比较,发病率上升了10倍,而眼淋巴瘤发病率亦上升了1.5倍。发病率升高可能与人免疫缺陷病毒 (human immunodeficiency virus,HIV)感染增加和接受器官移植及免疫抑制治疗增加有关。
大体上PCNSL可见于中枢神经系统各个部位,如软脑膜、脑实质或室管膜下等,可单发也可多发,边界相对清楚或不规则。脑实质内PCNSL质地柔软,呈黄褐色,瘤内可有出血或坏死。
镜下观可见脑肿瘤弥散性浸润脑实质,其范围远远超过大体所见肿瘤边界。淋巴瘤细胞集聚在血管周围并浸润血管壁。此种血管周围套装浸润现象在肿瘤边界处最多见。瘤组织还会侵犯软脑膜下层和蛛网膜下层。瘤周可见明显星形细胞反应。典型的T淋巴细胞常见于肿瘤边界,在瘤内较少见。大部分PCNSL为单克隆B淋巴细胞瘤,中枢T淋巴细胞瘤极少见。
1.CT检查
是PCNSL最常用的检查方式。CT平扫表现为高或等密度病灶,增强扫描病变为中或高度强化,周围有明显水肿带,但是CT阴性并不能完全排除对PCNSL诊断的可能性。
2.MRI检查
是PCNSL最主要的检查方式。T1像表现为等或低信号,T2为低信号、等信号、混杂信号或均匀性高信号,但是信号强度通常低于脑灰质。增强MRI可表现为均匀一致的增强占位,由于病灶边界不清,因此呈现为弥漫性增强,被称为云彩样表现(图1)。若病灶发生出血或坏死,可表现为环形增强,沿瘤周的线性增强常强烈提示系PCNSL。病灶周围多有水肿带。有时位于脑表面的病灶影像学表现类似于脑膜瘤。眶内淋巴瘤MRI薄层扫描可表现为黄斑部位的增强团块或葡萄膜的增厚,然而MRI对检出眶内淋巴瘤的敏感性常较低,因此阴性结果也不能完全排除此病存在的可能性。由于PCNSL富含肿瘤细胞,限制了水分子的弥散,因而在DWI上表现为高信号,表观弥散系数(apparent diffusion coefficient,ADC)为低信号。采用弥散张量成像可发现脑白质的改变情况,多数肿瘤组织的FA值降低,表现为低信号。PCNSL的质子MRS特点是脂质峰增高,Cho/Cr比值亦高。

图1 左额叶深部病灶,边缘模糊
3.PET和SPECT检查
PCNSL在FDG-PET和蛋氨酸(MET)-PET上表现为高代谢以及摄取增多。使用激素治疗后,PCNSL的FDG-PET高代谢活性可能有降低,放疗后蛋氨酸PET的面积和摄取程度均减低,因此PET能用于评估PCNSL的临床疗效以及行肿瘤切除术后是否有残余。PCNSL的SPECT检查表现为病灶对碘-123-IMP、铊-201等有较高的摄取率,因为SPECT和PET能区分AIDS患者中PCNSL和其他常见感染,因而有研究者建议,如果AIDS患者的EBV PCR为阳性,同时又有PET或SPECT的支持,即可确诊为PCNSL而不必行活检手术。
4.立体定向活检
是明确诊断的主要方法。施行此术不仅能明确病变的诊断,而且有助于制订治疗方案。立体定向活检术的出血率约为4%,病理学检测的阴性率为8%~9%。
5.脑脊液细胞学检查
PCNSL有沿脑脊液(CSF)播散的倾向,其中10%~20%的病例表现为明显的脑膜淋巴瘤,几乎所有患者CSF中的蛋白含量均见明显增高,细胞计数也有增高,而糖含量则常降低。CSF细胞学检查曾被认为是术前确诊的主要方法,约15%~31%的患者能通过CSF的检查而获得诊断。
6.EBV PCR
在AIDS患者中,PCNSL和EBV感染有着密切的关系,因此EBV PCR对PCNSL有较高的阳性率,可用于预测其诊断。
7.其他检查
PCNSL患者外周血液中的淋巴细胞多有增高,可作为诊断此病的重要参考。对于疑有发生眶内转移的PCNSL病变,可行裂隙灯检查或做玻璃体活检。
1.一般治疗
应用激素和脱水药物治疗,能在短期内改善临床症状,主要用于缓解危重患者的临床状况,以挽救生命,并为后续治疗创造条件。但是激素的作用时间比较短暂,而且长期使用会有一些副作用,且疗效有所降低,因此使用激素时应尽量减少剂量和缩短使用时间。
2. 药物治疗
PCNSL对某些化疗药物具有高度的敏感性,以往的化疗方法多借鉴全身淋巴瘤的治疗方案。近几年发现,单一化疗药物也能取得良好疗效,其中大剂量甲氨蝶呤(HD-MTX)是目前治疗PCNSL的常用药物。对于肾功能正常的患者,MTX的推荐剂量为3g/m2,需输液3小时以上。对于应用低剂量MTX治疗后有CSF播散者,应给予MTX鞘内注射治疗,也可以通过Ommaya囊施行脑室内给药。此外,基于HD-MTX的联合化疗方案,对PCNSL也有良好疗效,例如:联合使用HDMTX、替莫唑胺和美罗华(MTR),然后使用阿糖胞苷(Ara-C)和依托泊苷。Abrey等采用的治疗方案包括连续使用2天的MTX(3.5g/m2)和Ara-C (3g/m2),然后酌情给予卡莫司汀、依托泊苷、Ara-C和美法仑。Cheng等也使用了以HD-MTX为基础的方案作为诱导治疗,然后使用塞替派、白消安和环磷酰胺,7例受试者中有6名获得了完全缓解。另一种治疗方案包括全身给予HD-MTX、鞘内注射甲氨蝶呤,异环磷酰胺、环磷酰胺、Ara-C、泼尼松和长春花生物碱,总反应率为71%,完全反应率为61%。Ara-C是仅次于MTX的有效药物,易于穿透血-脑脊液屏障,其剂量达3g/m2以上时,可在CSF中达到有效治疗浓度。容易穿透血-脑脊液屏障的其他药物如替尼泊苷、塞替派、丙卡巴肼、卡莫司、拓扑替康等,亦被常用于PCNSL的一线或二线治疗方案之中。
对于应用HD-MTX治疗失败的患者,还可以采用多种补救治疗方案。Soussain等使用的方案包括2个周期的大剂量Ara-C和依托泊苷;对于有效的患者,可酌情给予塞替派、白消安和环磷酰胺,然后进行自体干细胞移植。在接受完整治疗的27例患者中,26例出现完全缓解,所有患者和接受完整治疗者的总生存期的中位数分别为:18.3个月和58.6个月。但是此方案对于60岁以上患者疗效不甚明显。单独使用替莫唑胺作为挽救治疗也有效果,总反应率为31%,1年生存率亦为31%,无进展生存期的中位数和总生存期分别为21个月和50个月。
3.放射治疗
PCNSL对放疗十分敏感,可有效地减轻临床症状。由于PCNSL具有浸润和多灶性生长的特性,因此临床推荐进行全脑放疗(whole brain radiation therapy,WBRT)。一般认为,理想的放疗剂量是40~50Gy,不需要额外增加剂量。PCNSL对单纯WBRT的总体反应率为90%,完全反应率约为60%。接受单纯外放疗的PCNSL患者的中位生存期是12~18个月。WBRT的主要副作用系神经毒性,容易引起神经认知功能障碍,约有2/3接受WBRT的患者会出现迟发性神经毒反应,包括小脑功能障碍、进展性痴呆和尿失禁等。
目前对于WBRT在PCNSL中的治疗作用尚存争议,较为明确的是对于60岁以上患者不主张进行WBRT,研究认为该治疗对患者的预后没有明显的改善作用,而且会增加神经毒性的发生率。目前正在尝试降低WBRT剂量,提高化疗比例,增加干细胞治疗等的临床研究。一般不推荐对脊髓进行预防性放射治疗,因为接受放疗的区域仍会出现复发,因而对预后帮助不大。但如果MRI检测到有一个或多个脊髓病灶,则必须进行全脊髓放疗。对于直径小于3cm的单个或多个病灶,也可采用X刀或γ刀进行治疗,据观察其效果明显优于普通放疗。此外,还可采用立体定向后装内放疗。
4.联合放、化疗
虽然PCNSL对化疗有高度敏感性,但是复发率仍然较高。对于复发的患者,需要对其病情进行重新评估,对那些化疗效果欠佳的患者可以考虑加用放疗。采用先化疗再行放射治疗的联合放、化疗方案,能延长PCNSL患者的生存期。例如美国肿瘤放射治疗协会(RTOG)推荐使用5个周期的HD-MTX(2.5g/m2)、长春新碱、丙卡巴肼和鞘内注射甲氨蝶呤(12mg),然后进行总剂量为45Gy的WBRT。化疗后的完全反应率为36%,总体完全反应率为94%,无进展中位生存期为24个月,总生存期为36.9个月,其中60岁以下患者的总生存期明显长于60岁以上患者。但是采用联合放、化疗方案也有明显的毒副作用,MTX联合WBRT后的认知功能障碍发生率高达63%。为了进一步减少WBRT引起的毒副作用,专家们倾向于增加化疗药物在联合放、化疗方案中的比重,减少放射治疗的剂量。
5.手术治疗
手术治疗在PCNSL中的诊断和治疗中主要具有4个方面的作用:①明确诊断,在立体定向技术广泛应用之前,开颅手术切除病灶是获得组织标本,明确诊断的重要方式。随着立体定向手术技术的成熟与普及,在PCNSL的诊断中逐渐替代了开颅手术。立体定向活检术可以提供足够组织明确病理诊断,其损伤较小,术后反应轻。②肿瘤切除,由于PCNSL具有弥漫浸润性生长的特点,因此多数临床研究认为开颅手术切除病灶对PCNSL患者的临床预后没有明显的改善作用,但是仍有部分研究认为开颅手术在PCNSL的治疗中仍具有重要作用。首先,如果病灶引起明显的颅内高压、并出现脑疝等威胁患者生命的情况,进行紧急手术治疗能挽救患者生命;其次,部分学者主张对于较大的孤立性瘤体首先施行切除,继之应用放、化疗方案,能取得较好疗效(图2);此外,若肿瘤组织对激素、化疗和放疗不敏感者,手术切除肿瘤宜作为首选。③进行间质内放、化疗,通过手术的方式在瘤腔中放置籽粒进行间质内放疗,也可以进行Ommaya囊的放置,进行间质内化疗,从而提高PCNSL患者的临床疗效。④治疗并发症,肿瘤压迫、软脑膜受累以及炎症反应等因素都可能引起脑积水的发生,可以通过脑室-腹腔分流等方法治疗脑积水,缓解患者的临床症状。此外,部分患者放化疗后引起的神经毒性症状能在脑室-腹腔分流术后得到暂时性改善。但是,脑室-腹腔分流术也使得肿瘤细胞向腹腔播散的风险增加,因此手术之前要结合患者的病情来权衡利弊。
6.其他治疗
(1)免疫治疗:利妥昔单抗(rituximab,商品名美罗华)系抗CD20单克隆抗体,使用美罗华能提高全身性B细胞淋巴瘤的完全反应率。美罗华[750mg/(m2·w)]联合替莫唑胺(100~200mg/m2,用1周,停1周),患者的反应率为53%。鞘内注射美罗华联合脂质体Ara-C治疗复发淋巴瘤性脑膜炎,结果发现,此疗法不会增加药物的毒性。
(2)干细胞移植:对于复发性和高危全身性PCNSL的患者,自体干细胞移植亦有一定效果。
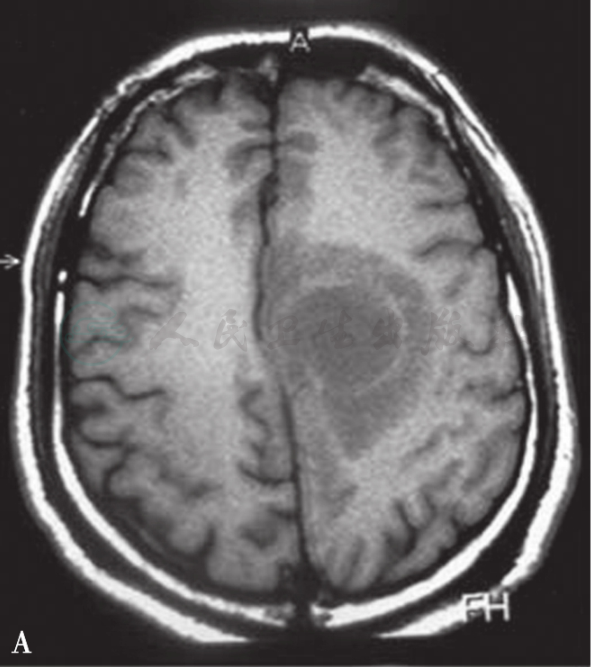
图2A 开颅手术病灶切除治疗的病例
术前
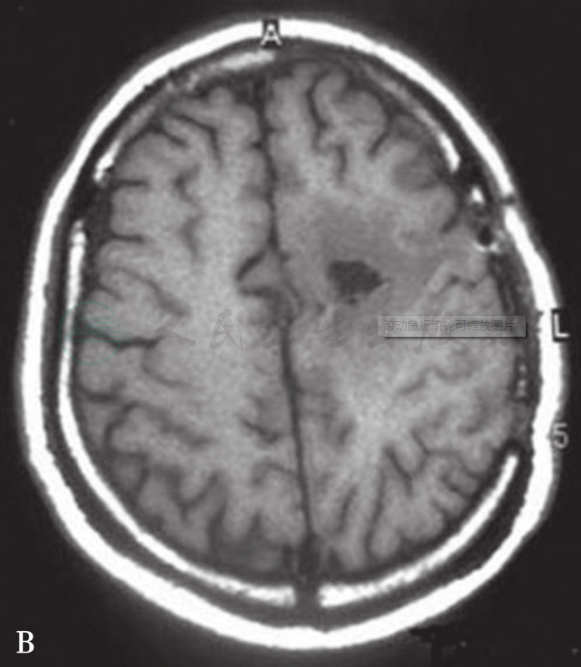
图2B 开颅手术病灶切除治疗的病例
术后3天
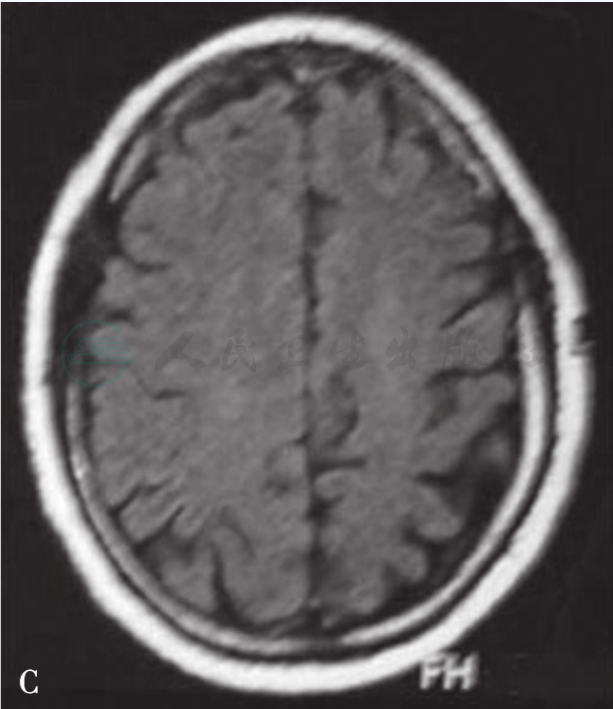
图2C 开颅手术病灶切除治疗的病例
术后8年,肿瘤未见复发













