英文名称 :upper gastrointestinal hemorrhage
上消化道出血(upper gastrointestinal hemorrhage)常表现为急性大出血,是临床常见急症。在高龄、有严重伴随病、复发性出血患者中病死率高达25%~30%,应予高度重视。
临床上最常见的出血病因是消化性溃疡、食管胃底静脉曲张破裂、急性胃黏膜病变和胃癌,占上消化道出血的80%~90%。
1.食管疾病
食管炎、食管溃疡、食管肿瘤、食管贲门黏膜撕裂、Cameron糜烂、理化和放射性损伤。
2.胃、十二指肠疾病
消化性溃疡、急性胃黏膜病变、胃血管异常(胃毛细血管扩张、Dieulafoy病等)、恶性肿瘤和其他良性肿瘤、息肉、急性胃扩张、胃黏膜脱垂或套叠、十二指肠炎和憩室炎、膈疝、胃扭转、钩虫病、胃肠吻合术后的空肠溃疡和吻合口溃疡、佐林格-埃利森(Zollinger-Ellison)综合征等。
3.门静脉高压
食管胃底静脉曲张破裂出血、门静脉高压性胃病、十二指肠异位静脉曲张破裂出血。
4.上消化道邻近器官或组织的疾病
①胆胰管出血:胆胰管结石、胆管肿瘤等;②胰腺疾病累及十二指肠:壶腹周围肿瘤、胰腺肿瘤等;③胸或腹主动脉瘤破入消化道;④纵隔肿瘤或脓肿破入食管。
5.全身性疾病
如感染、肝肾功能障碍、凝血机制障碍、结缔组织病等也可引起上消化道出血。①血液病:白血病、再生障碍性贫血、血友病等;②血管性疾病;③结缔组织病:血管炎;④急性感染性疾病:流行性出血热、钩端螺旋体病等;⑤尿毒症。
1.内镜检查
内镜检查是消化道出血定位、定性诊断的首选方法,可解决90%消化道出血的病因诊断(图1)。内镜检查见到病灶后,应取活体组织检查或细胞刷检,以提高病灶性质诊断的正确性,并根据病变特征判别是否继续出血或再出血的危险性,并行内镜下止血治疗。一般主张在出血后24~48小时内进行检查,并备好止血药物和器械。急诊胃镜最好在生命体征平稳后进行,尽可能先纠正休克、补足血容量,改善贫血。胃镜检查可在直视下观察食管、胃、十二指肠球部直至降部,从而判断出血的病因、部位。结肠镜是诊断结肠及回肠末端病变的首选检查方法。重复内镜检查可能有助于发现最初内镜检查遗漏的出血病变。超声内镜、色素放大内镜等均有助于明确诊断,提高对肿瘤、癌前期病变等的诊断准确率。胶囊内镜具有安全、创伤小的优点,主要用于小肠疾病的诊断,对怀疑小肠出血的检出率在38%~83%。小肠镜是目前小肠疾病的主要检查手段。应用最广泛的是各种器械辅助式小肠镜包括双气囊小肠镜、单气囊小肠镜、螺旋管式小肠镜,还可以进行术中小肠镜检查。如操作人员技术熟练,理论上能检查整个肠道,可用于怀疑小肠出血的患者,诊断率在60%~80%。对于胶囊内镜检查阳性的患者,再行小肠镜检查,将提高检出率至60%~90%。但若对胶囊内镜检查阴性的消化道出血患者,再次进行小肠镜检查,病变检出率仅为16.7%~37.8%。
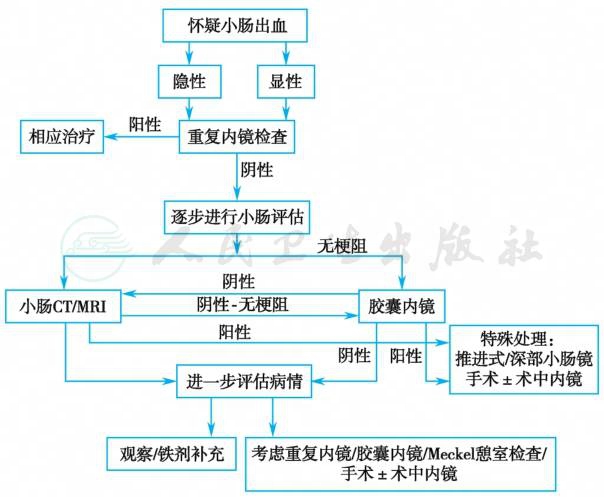
图1 小肠出血诊治流程
引自:实用内科学.第16版.ISBN:978-7-117-32482-3
2.X线钡餐检查
仅适用于出血已停止和病情稳定的患者,对急性消化道出血病因诊断的阳性率不高,多为内镜检查所代替。钡餐检查对于怀疑小肠出血的诊断率仅有3%~17%,仅对小肠憩室和粘连性病变的诊断有一定价值,目前并不推荐用于小肠出血的诊断。
3.放射性核素显像
对活动性出血出血速率≥0.1ml/min时有诊断价值,诊断率约为50%,尤其适用于间歇性和延迟性小肠出血,不适用于消化道大出血者。
4.血管造影
选择性血管造影对活动性大消化道出血(尤其是血流动力学不稳者)或者血管性病变的诊断及治疗具有重要作用,诊断率约50%。根据脏器的不同可选择腹腔动脉、肠系膜动脉造影,出血速率≥0.5ml/min时,可发现造影剂在出血部位外溢,定位价值较大。对确定下消化道出血的部位(特别是小肠出血)及病因更有帮助,也是发现血管畸形、血管瘤出血的可靠方法。但该检查是有创性操作,且有可能发生造影剂过敏、急性肾衰竭、血栓栓塞、感染和穿刺部位出血等并发症。
5.CT相关检查
CT小肠成像(CT enterography,CTE)将小肠腔充盈后使用多排CT扫描,可发现血管病变和肠道炎症改变,并提高小肠肿块尤其是黏膜来源病变的检出率,可与胶囊内镜互补,对于胶囊内镜禁忌证者具有优势。CT血管成像(CT angiography,CTA)可准确检出并定位肠道血管性疾病,可检出出血速率≥0.3ml/min的病变。
6.手术探查和术中内镜检查
各种检查均不能明确原因时应手术探查和术中内镜检查。术中内镜对小肠出血诊断率为58%~88%。另外,可在术中行选择性血管造影或注射亚甲蓝(美蓝),以帮助明确诊断。
上消化道出血病情危急,特别是大量出血者,可危及患者生命,抗休克、迅速补充血容量治疗应放在一切医疗措施首位。
1.一般处理
活动性出血期间禁食,停止出血后24小时可给予冷流质饮;卧床、注意防跌倒;保持呼吸道通畅;监测生命体征;尽快建立静脉输液通道。
2.积极补充血容量
(1)病情紧急时,输液、输血同时进行,先输注平衡液或葡萄糖盐水甚至胶体扩充血容量。
(2)输注红细胞悬液指征:①收缩压低于90mmHg,或较基础收缩压下降超过30mmHg;②血红蛋白低于70g/L,血细胞比容低于25%;③心率>120次/分。
(3)肝硬化患者可补充新鲜冰冻血浆。
(4)对高龄、伴心肺肾疾病患者,应防止输液量过多诱发急性肺水肿。
(5)血容量充足的指征:收缩压90~120mmHg;脉搏<100次/分;尿量>40ml/h、血Na+<140mmol/L;神志清楚或好转,无明显脱水貌。
3.止血措施
不论是急性非曲张静脉出血或静脉曲张破裂出血,均可以采取以下措施止血,包括药物、内镜、介入和手术等。
(1)药物止血
1)抑酸药:质子泵抑制剂(PPI)是目前最强效的抑酸药,常用于上消化道出血的治疗(表1)。小量出血,可门诊口服PPI和H2受体拮抗剂(H2RA)。大出血者,初期宜使用大剂量PPI,可迅速提高胃内pH至6以上,巩固胃镜止血疗效,减少手术和住院费用。如埃索美拉唑80mg静脉推注后,以8mg/h输注持续72小时。
表1 不同种类PPI规格及用法
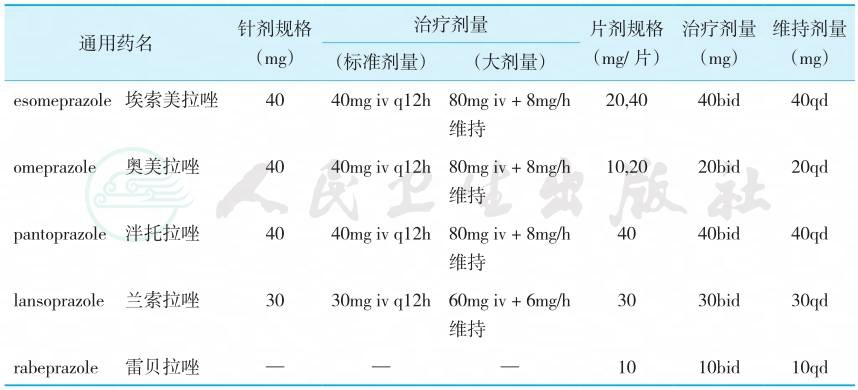
2)减少内脏血流量药物:通过减少门脉血流量及降低门静脉压力,用于食管胃底静脉曲张出血。包括生长抑素及类似物奥曲肽、特利加压素等,垂体后叶素副作用较大,在没有上述药物时可作为备选药物。生长抑素用法为首剂250μg静脉缓注,继以250μg/h持续静脉滴注。本品半衰期极短,滴注过程中不能中断,若中断超过5分钟,应重新注射首剂。奥曲肽是8肽的生长抑素拟似物,半衰期较长,首剂100μg静脉缓注,继以25~50μg/h持续静脉滴注。特利加压素起始剂量为2mg/4h,出血停止后可改为1mg/次,每日2次,维持5天。垂体加压素剂量为0.2U/min静脉持续滴注,可逐渐增加剂量至0.4U/min。该药可致腹痛、血压升高、心律失常、心绞痛等副作用,严重者甚至可诱发心肌梗死。故对老年患者应同时使用硝酸甘油,以减少该药的不良反应。
3)止血药物:插入胃管可灌注冰冻去甲肾上腺素溶液(去甲肾上腺素8mg,加入冰生理盐水100~200ml)及凝血酶等局部止血。应慎用止血药物,尤其是老年人、门静脉高压患者,避免高凝状态诱发心脑血管意外及门静脉血栓。
(2)内镜治疗
消化性溃疡出血约80%可通过药物治疗止血,对于Rockall评分高危患者应予以内镜治疗,包括注射药物、电凝及使用止血夹等。对于静脉曲张性出血,当出血量为中等以下,应紧急采用内镜下食管曲张静脉套扎术、硬化剂注射等,止血成功率与视野是否清楚与操作医生的技术水平有关。
(3)三腔二囊管压迫止血
食管胃底静脉曲张出血的暂时止血措施,用于内镜介入手术止血前的过渡性治疗;由于其食管黏膜糜烂坏死等并发症多,三腔二囊管压迫止血后,短期内不宜进行内镜治疗;该治疗常使患者不适,顺应性较差,需要患者配合。为防黏膜糜烂,一般持续压迫时间不应超过24小时,放气解除压迫一段时间后,必要时可重复应用。
(4)介入治疗
1)非静脉曲张性出血:药物及内镜治疗不成功时,可通过选择性胃左动脉、胃十二指肠动脉介入治疗,栓塞供应病灶的小动脉。上消化道各供血动脉之间侧支循环丰富,一般不存在组织坏死的危险。
2)静脉曲张性出血:经颈静脉肝内门体分流术(TIPS)对急性大出血的止血率达到95%,新近的国际共识意见认为,对于大出血和估计内镜治疗成功率低的患者应在72小时内行TIPS。择期TIPS通常对患者肝功要求在Child-Pugh评分B级,食管胃底静脉曲张急性大出血时,TIPS对肝功的要求可放宽至Child-Pugh评分C级,这与该血管介入微创治疗具有创伤小、恢复快、并发症少和疗效确切等特点有关。
(5)手术治疗
对非静脉曲张性出血,药物、内镜及介入治疗仍不能止血、持续出血将危及患者生命时,须不失时机地进行手术;静脉曲张性出血者,手术并发症多,死亡率高,目前多不采用。













