英文名称 :secondary glaucoma
继发性青光眼(secondary glaucoma)是由其他眼病所引起的,占全部青光眼的20%~40%,多为单眼。由于原发眼病的不同,临床表现亦各异。应针对原发病进行治疗,同时用药物控制眼压,必要时进行手术治疗。
一、继发于角膜病
角膜溃疡或角膜炎有时并发急性虹膜睫状体炎而继发青光眼。角膜粘连性白斑、虹膜周边前粘连及瞳孔后粘连等都能影响房水的排出而引起继发性青光眼。
二、继发于虹膜睫状体炎
1.急性虹膜睫状体炎
2.虹膜异色性睫状体炎(heterochromic cyclitis)
青光眼常在色素少的眼发生,有并发白内障时更易发生。其病理改变为小梁硬化及小梁间隙阻塞。临床过程则与单纯性青光眼相似。皮质激素治疗本病无效,可用药物控制眼压,必要时行滤过手术。并发白内障时,摘除晶状体可能控制眼压。
3.青光眼睫状体炎综合征(glaucomatocyclitic crises)
又名Posner-Schlossmann综合征为常见的继发性青光眼。
三、继发于晶状体改变
1.晶状体脱位(displacement of the lens)
晶状体半脱位压迫房角或刺激睫状体而使眼压升高。本病常伴有房角关闭,眼压升高可能与此有关。一般可用药物治疗,必要时可摘出晶状体。晶状体完全脱入前房可使眼压骤升,应立即将其摘出。晶状体脱入玻璃状体很少引起青光眼,可暂不处理,但有可能引起晶状体溶解或过敏性葡萄膜炎。
2.晶状体肿胀(intumescent lens)
白内障的肿胀期,晶状体肿胀、变厚可引起瞳孔阻滞而继发青光眼,尤其是易发生于小眼球浅前房的患者。摘除晶状体可解除瞳孔阻滞治愈青光眼。如果已有周边前粘连,则应做白内障和抗青光眼联合手术。
3.晶状体溶解性青光眼(phacolytic glaucoma)
发生于过熟期白内障,由于晶状体囊皮变薄或自发破裂,液化的晶状体皮质漏到前房,被噬细胞吞噬,这些细胞和晶状体皮质堵塞小梁间隙而引起急性或亚急性青光眼。其特征为前房深,房角开放,在角膜后壁、房水、房角、虹膜及晶状体表面有多量灰白色具有彩色反光的碎片,系含有蛋白颗粒的肿胀的噬细胞及晶状体皮质。最有效的疗法是用药物控制眼压后立即做晶状体摘除术。术后眼压一般可恢复正常,甚至术前光功能不确者,术后也可获得较好视力。
4.晶状体颗粒性青光眼(lens particle glaucoma)
又称晶状体皮质残留性青光眼。见于白内障囊外摘出或偶尔见于白内障肿胀期囊膜自发破裂后。前房内有松软或颗粒样晶状体皮质。常伴有不同程度虹膜炎症,故常有相应的虹膜后粘连或前粘连,房角开放有较多晶状体皮质或有周边前粘连。可用皮质激素和抗青光眼药物,不用缩瞳剂;如眼压不能控制,可做手术冲洗前房内晶状体皮质。
5.晶状体过敏性眼内膜炎继发青光眼(glaucoma in endophthalmitis phacoanaphylactica)
这是由于对晶状体物质过敏而引起的眼内膜炎,可发生于晶状体囊皮完整或自发破裂以及囊外摘出后有晶状体皮质残留者。前房炎性反应明显,有多量白细胞渗出,角膜后壁有成团的沉着物。在急性反应时眼压多偏低,当小梁和房角发生损害后则产生青光眼其治疗措施是摘除晶状体或取出残留皮质。
四、外伤性青光眼
1.钝挫伤(contusion)
钝挫伤引起前房积血或房角后退时可导致继发性青光眼。前房少量积血,一般在数天内即可吸收;当出血量多,尤其是反复继发出血时,常引起继发性青光眼,可并发角膜血染。房角后退继发青光眼(图1)早期发生者多在伤后数周内发病,由于小梁受损伤,使房水流出受阻,但伤后同时伴有房水分泌减少,所以眼压可不升高。当房水分泌正常后眼压即升高,常可持续数月至数年,但多在1年内外流管道修复,眼压亦恢复正常。晚期发生者可发生在伤后10年或更晚,是由于外伤后角膜内皮细胞形成玻璃样膜覆盖了房角,或继发了虹膜周边前粘连。这种晚期青光眼是顽固的。
房角后退或称前房角劈裂(图2)是睫状体表面的外伤性撕裂。为睫状体的环行肌和纵行肌之间发生撕裂和分离,因环行肌与虹膜相连,环行肌挛缩将引起虹膜根部后移,而纵行肌仍附着在原位的巩膜突,因而房角变深。Howard(1969)将房角后退分为浅、中、深三度:①浅层撕裂:为葡萄膜网部的破裂,睫状体带及巩膜突暴露,睫状体带较健眼明显加宽,巩膜突色较白,有时可有色素沉着。睫状体表面没有真正的外伤裂隙。②中层撕裂:睫状肌纤维间出现肯定裂隙,虹膜根部与睫状体前面后移,较健眼房角加宽而深,睫状体带的宽度可为正常眼的数倍,后退的范围常超过180°。③深层撕裂:睫状体有深层裂隙,而裂隙的尖端前房角镜检查看不见,有时可有广泛的睫状体截离。(睫状体截离是睫状体与巩膜突分离,使前房与睫状体上腔相通,眼压为降低。)
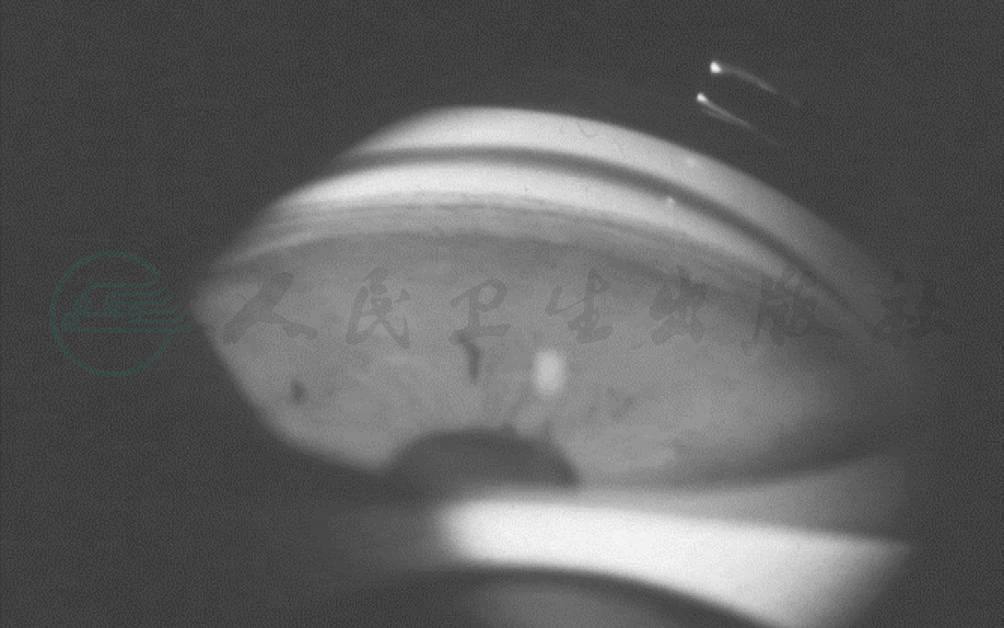
图1房角后退性青光眼
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
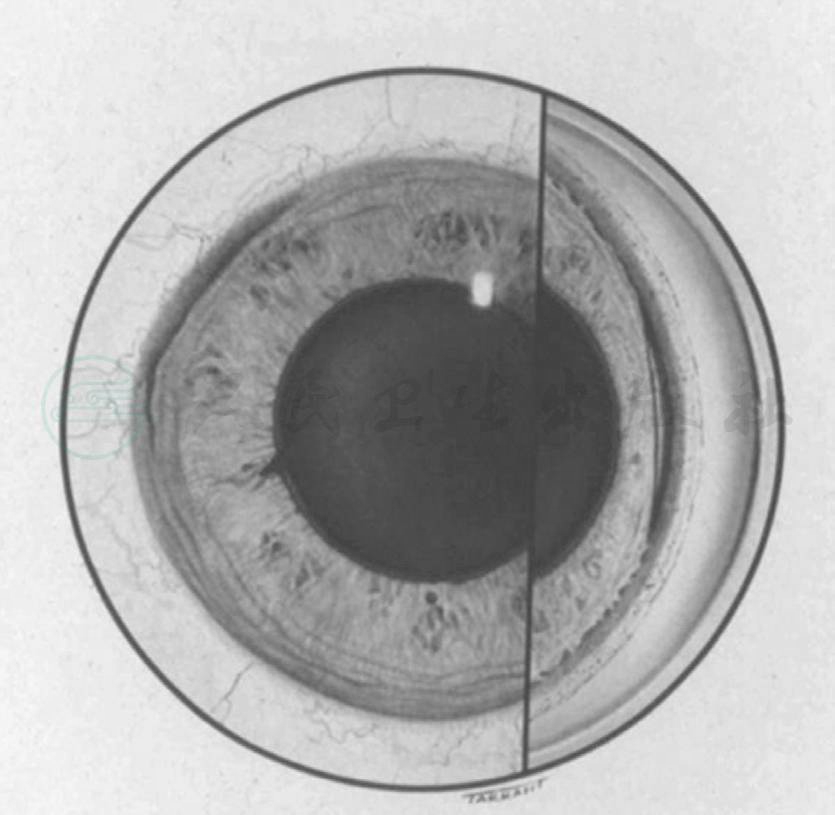
图2房角劈裂
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
房角后退的患者对于局部激素试验多呈高度反应,说明具有青光眼遗传基因的人,在外伤后更容易发生继发性青光眼。治疗与开角型青光眼相同。
2.穿通伤
穿通伤后由于眼内组织嵌入伤口,或由于晶状体囊膜破裂,皮质肿胀而引起。如眼内有异物存留,可由于炎症、铁锈或铜锈沉着使小梁发生改变而致眼压升高。
对眼球穿通伤,应妥善做好初步处理,使伤口内不嵌顿眼内组织。白内障所致的青光眼应摘出晶状体。总之应根据引起青光眼的病因酌情处理。
五、继发于血液异常、眼内出血和血管疾患
1.血液异常继发性青光眼
巨球蛋白血症(macroglobulinemia)、高蛋白血症(hyperproteinemia)和红细胞增多症(polycythemia)等由于血清中有大分子量的球蛋白或增多的红细胞而使血液黏稠度增加、血流缓慢,容易形成血栓。视网膜中央静脉血栓形成患者中,约有 10%~20%可发生继发性青光眼。有时Schlemm管内也可有血栓形成而引起急性青光眼。房角是开放的,可用药物治疗,但效果差。
患急性白血病(acute leucemia)时,葡萄膜有白细胞浸润,常并发眼压升高。虹膜明显充血,纹理消失,表面有新生血管,常伴有前房积脓或积血。眼局部对放射治疗敏感。
2.前房积血(hyphema)
眼压升高与出血量有关,出血超过前房1/2者易引起继发性青光眼。并发症为角膜血染和视神经损害,其发生与眼压升高有关,角膜血染是在前房积血持续时间较长,前房积血量大,眼压升高及直接附着在角膜内皮上的血液毒素,使角膜内皮功能失代偿,角膜内皮的渗透性发生改变,红细胞渗入角膜实质,引起角膜血染(图3)。早期血染在后部角膜基质中,表现为黄色颗粒状改变,或呈半透明红色,角膜透明度下降,此过程可迅速发展,有时在24h内整个角膜被血细胞浸润,随着血小板的降解作用,角膜逐渐显得发亮,呈不透明的绿色,可持续数年。角膜血染的消退过程是从角膜周边部开始逐渐向中央部变透明。在角膜内皮有损害时,眼压正常情况下也可致角膜血染。
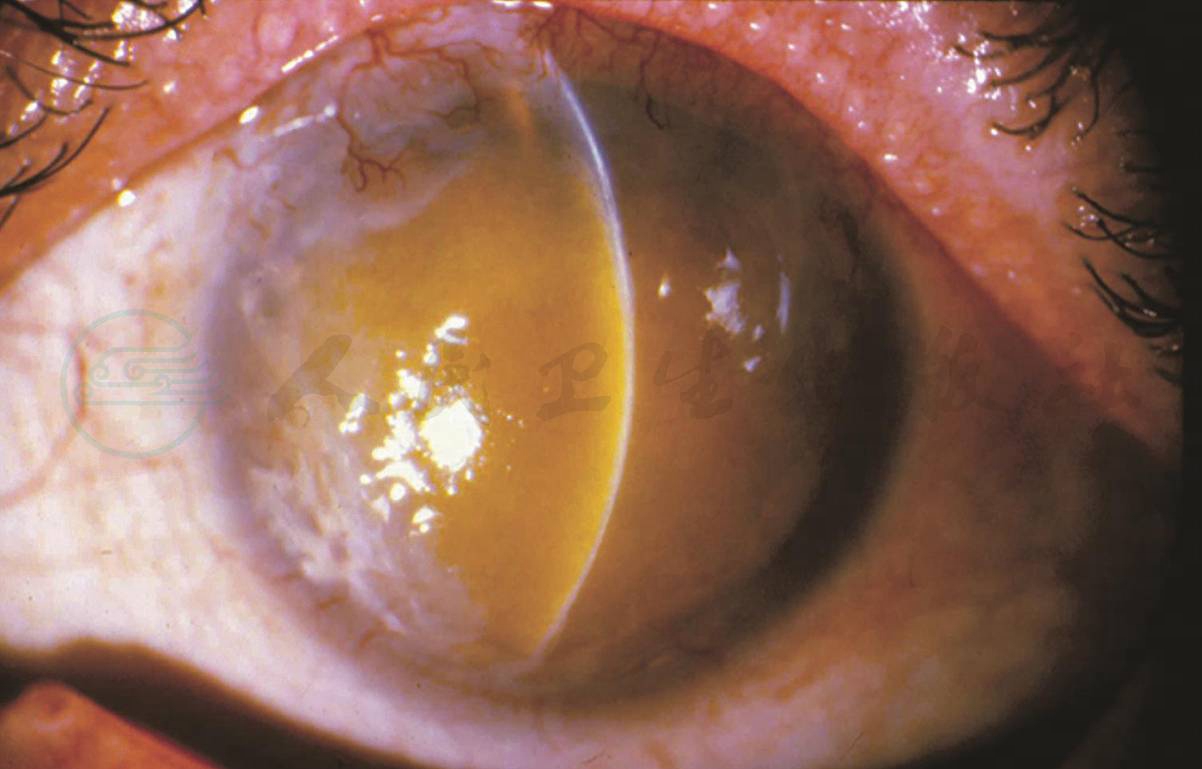
图3角膜血染中央角膜呈棕黄色混浊
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
无并发症的前房积血可采用非手术治疗,一般所有减少再出血或促进血液吸收的药物治疗效果不肯定。减少房水生成药物和高渗剂可预防角膜血染和视神经损害。如药物治疗不能控制眼压,可手术冲洗前房积血或取出血块。
3.溶血性青光眼(hemolytic glaucoma)
眼内出血,尤其是玻璃体积血后,红细胞的破坏产物和含有血色素的巨噬细胞,有时可阻塞小梁引起急性眼压升高。其治疗与单纯性青光眼相同,但也可将红细胞碎屑冲出,使眼压下降。
4.血影细胞性青光眼(ghost cell glaucoma)
各种原因所致玻璃体积血,红细胞发生变性,从红色、双凹、柔韧的细胞变为土黄色、圆形不柔韧的血影细胞,通过破损的玻璃体前界膜进入前房,进入前房的血影细胞可机械性阻塞小梁网,可引起急性眼压升高的开角型青光眼。患者症状取决于眼压的高度。角膜后壁可有土黄色细胞沉着,房水中有棕黄色细胞浮游,可有假性前房积脓,如有新鲜红细胞则位于土黄色血影细胞下方(图4)。前房角为开角,覆以薄层土黄色细胞,使小梁网呈棕黄色或完全遮盖房角结构,下方尤为明显。玻璃体呈典型土黄色,在前玻璃体中可见多数细小黄褐色颗粒。抽取房水或玻璃体用相差显微镜可直接查到血影细胞,或染色后用普通显微镜检查。
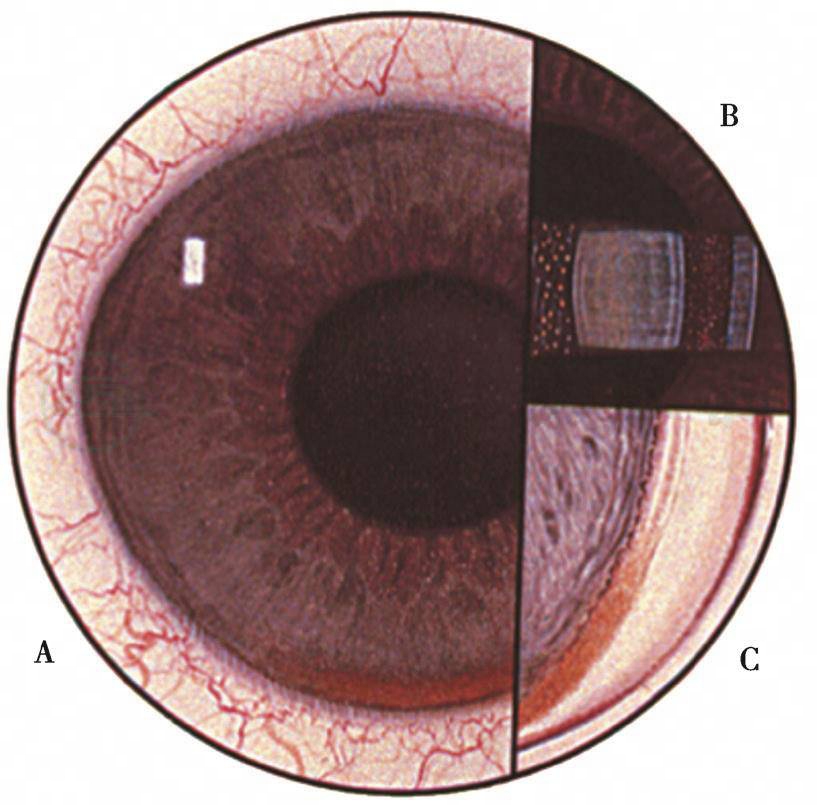
图4血影细胞性青光眼
A:前房下方有土色血影细胞;B:裂隙灯所见前房、玻璃体血影细胞; C:前房角镜所见
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
李志辉等认为用普通光学显微镜,能清晰准确地识别血影细胞。当血红蛋白发生不可逆性变性,形成变性株蛋白小体而沉淀时,可用结晶紫将其细胞染色后进行观察。钟国庆报道用1%甲紫染色,在光学显微镜下检查血影细胞的胞膜呈紫红色斑点状,而正常红细胞不被甲紫染色。因甲紫是一种碱性染料,沉积在血影细胞膜上的变性株蛋白为酸性物质,故能使血影细胞着色。检查时如轻击载玻片,可见染色的不能变形的血影细胞在悬浮的标本内漂动。血影细胞性青光眼为一过性;可持续数月,未有报告引起小梁永久性损害者。开始用抗青光眼药物治疗;如不能控制眼压则彻底冲洗前房,必要时可重复做,很少需做玻璃体切除。
5.血铁质沉着性青光眼(hemosiderotic glaucoma)
为一种慢性继发性开角型青光眼,多有长期反复眼内出血史。小梁内皮细胞吞噬溶解变性的血红蛋白,血红蛋白的铁离子氧化成氧化铁,它与组织蛋白或含巯基类蛋白质结合成铁蛋白质化合物沉着于角膜、视网膜、小梁网等眼内组织,可使小梁变性、硬化和间隙闭塞而致眼压升高。可根据出血病史、眼组织的铁锈样沉着物、小梁网呈棕红色、房水中查不出血影细胞等作出诊断。治疗用抗青光眼药物控制眼压。
6.新生血管性青光眼(neovascular glaucoma)
是指虹膜和小梁表面有新生的纤维血管膜,使虹膜与小梁和角膜后壁粘连所造成的青光眼。虹膜上的新生血管形成典型的虹膜新生血管丛或称虹膜红变(rubeosis iridis),使虹膜组织模糊不清,呈暗红色,瞳孔开大,对光反应消失,由于血管膜收缩而使瞳孔缘色素上皮外翻。因虹膜新生血管丛容易破裂,反复发生前房积血,故又名出血性青光眼(hemorrhagic glaucoma)。本病极顽固,患者异常疼痛,常导致失明(图5)。
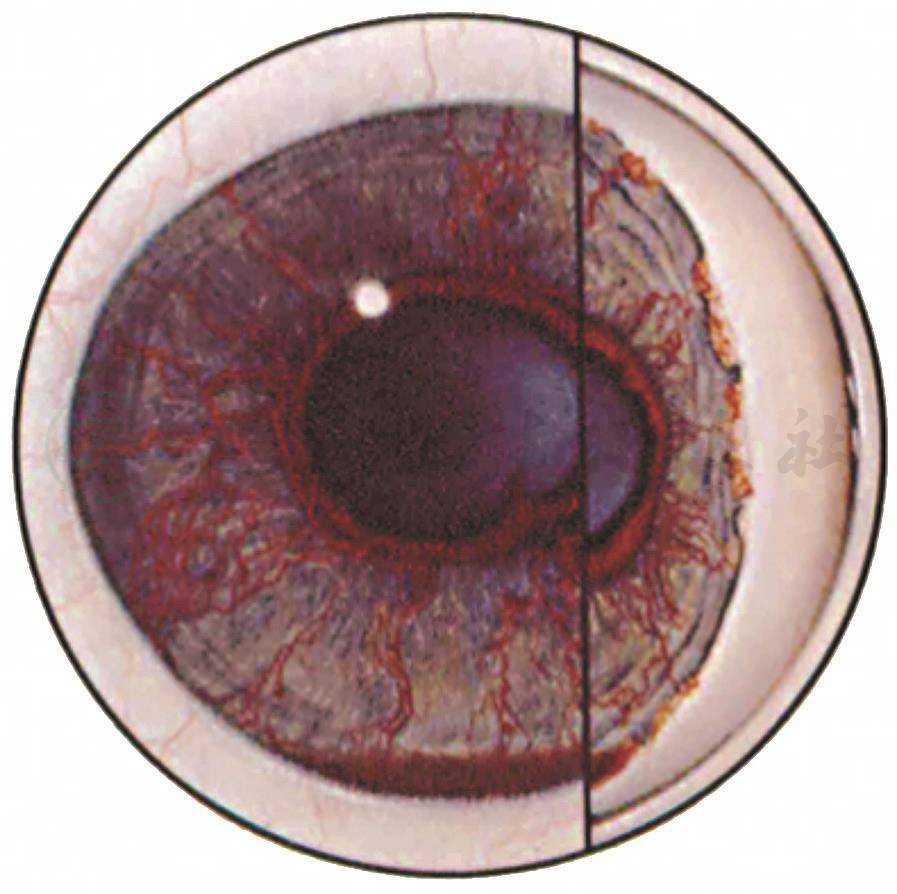
图5新生血管性青光眼
虹膜及房角有新生血管
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
虹膜新生血管丛易发生于一些引起视网膜缺氧的疾病,如视网膜中央静脉阻塞、糖尿病性视网膜病变、视网膜中央动脉阻塞、恶性黑色素瘤和视网膜脱离等,尤以前两种病比较多见。由糖尿病引起者常发生于有增殖性视网膜病变及反复出血者。由于视网膜缺氧而产生血管形成因子,引起虹膜表面和小梁网的纤维血管膜增殖。目前的研究发现具有促进血管生成活性的因子有血管内皮生长因子(VEGF)、胰岛素样生长因子1和2、胰岛素样生长因子结合蛋白2和3、血小板来源的生长因子、转化生长因子α等,其中VEGF被认为是最主要的影响因子。初期它们覆盖开敞的房角,后期纤维血管膜收缩形成房角周边前粘连,均可导致顽固的眼压升高(图6)。其临床过程可分为三期:
(1)青光眼前期:
瞳孔缘周围虹膜有毛细血管丛扩张和细小新生血管,逐渐向虹膜根部进展。前房角正常或有少量新生血管。此期眼压正常。
(2)开角型青光眼期:
虹膜新生血管融合,前房有炎症反应。房角开放但有多量新生血管,眼压突然升高。
(3)闭角型青光眼期:
纤维血管膜收缩,虹膜变平,瞳孔开大,瞳孔缘色素层外翻,虹膜与晶状体间距离加大,房角广泛周边前粘连或完全关闭。眼压升高。
完全性视网膜中央静脉阻塞在发病后3个月内约有20%发生继发性青光眼,而单纯性青光眼又常容易发生视网膜中央静脉阻塞。这两种疾病常相继发生的机制目前尚不清楚。
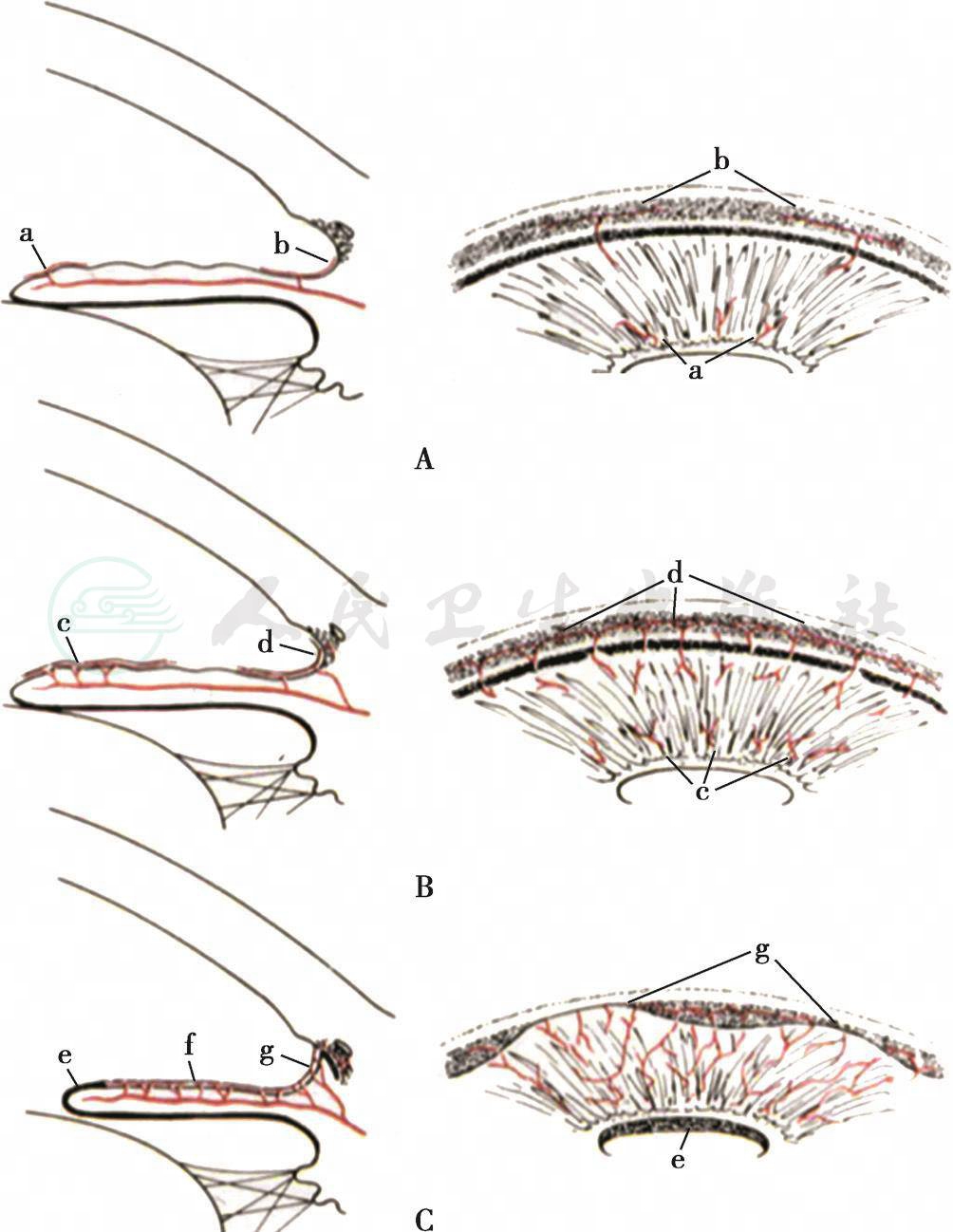
图6新生血管性青光眼
A.青光眼前期;B.开角型青光眼晚期;C.闭角型青光眼期a、b、c、d、e、f、g 为新生血管
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
视网膜中央动脉阻塞后发生继发性青光眼者仅占1%,眼压升高大多发生在动脉阻塞后5~9周,较静脉阻塞继发青光眼所间隔的时间要短得多。
对本病的治疗,分泌抑制剂或手术治疗效果均不满意。用缩瞳剂可使充血及疼痛加重。局部应用皮质激素和阿托品能缓解症状,但不能降低眼压。由于视网膜血管病变及继发性青光眼而已失明者,为解除痛苦可摘除眼球。如尚残存有用视力,可行引流阀置入术和睫状体功能减弱性手术,引流阀置入术效果较其他引流手术好,术前应降低眼压,术中穿刺前房时动作要慢,以尽可能减少前房积血。也可试行小梁切除术。强化的冷凝治疗可使虹膜血管暂时消退。
随着对新生血管性青光眼的发病机制的深入研究和抗VEGF药物在眼科领域的应用,目前已将抗VEGF药物的应用作为新生血管性青光眼的辅助治疗。有许多研究报道玻璃体腔注射抗VEGF药物可以使虹膜和视网膜的新生血管迅速消退,从而减少抗青光眼术中的出血和术后结膜的瘢痕化,提高了手术成功率。
另一方面,应用全视网膜激光凝固治疗出血性青光眼取得了一定的疗效。全视网膜光凝可使视网膜萎缩,使其不至于缺氧,消除了产生血管新生的因素,并可使虹膜和房角的新生血管萎缩。此疗法适用于早期病例,在房角被纤维血管膜封闭以前,可使房角的血管消退,并能使部分粘连拉开。如同时加用药物,眼压可能被控制。
青光眼前期行全视网膜光凝全视网膜光凝是预防虹膜红变和新生血管性青光眼最有效的治疗方法。视网膜中央静脉阻塞,在虹膜红变前期,即视网膜有广泛毛细血管非灌注区或虹膜有异常血管荧光渗漏,也适于行预防性全视网膜光凝。屈光间质混浊时可行全视网膜冷凝全视网膜冷凝或房角新生血管直接光凝。所有新生血管性青光眼病例,除行降眼压手术外,均应行全视网膜光凝或冷凝术,以解除其产生视网膜或虹膜新生血管的病因,可根据具体情况,选择在降眼压手术之前或手术后做。
7.上巩膜静脉压升高引起的继发性青光眼
上腔静脉阻塞、纵隔肿物、颈动脉海绵窦瘘、球后占位性病变和内分泌性眼球突出等可使上巩膜静脉压升高,房水排出因而受阻而导致眼压升高。此时C值正常,房角也无异常,但Schlemm管内可有血液,常伴有球结膜水肿和血管迂曲扩张、眼球突出以及视盘水肿。卧位时眼压明显升高。在动静脉瘘的患者,偶尔合并新生血管性青光眼。应针对原发病治疗。
六、继发于眼部退行性变
1.虹膜角膜内皮综合征(iridocorneal endothelial syndrome,ICE syndrome)
为一组原发性角膜内皮异常疾病,其特点是单侧角膜、虹膜、房角异常和继发性青光眼(图7)。多见于年轻成人和女性。临床改变可分以下三种类型:
(1)原发性进行性虹膜萎缩(progressive essential atrophy of iris):
本病是虹膜的慢性进行性萎缩,常可形成虹膜穿孔房角粘连,房角有内皮细胞增殖,从而导致青光眼。随着病程的进展,房角粘连范围也逐渐扩大,严重时可累及房角全周;当房角粘连达一定程度时即可引起眼压升高。在病变过程中并无炎症现象,不发生后粘连。病变进展缓慢,继发青光眼也较晚,最后常导致失明。
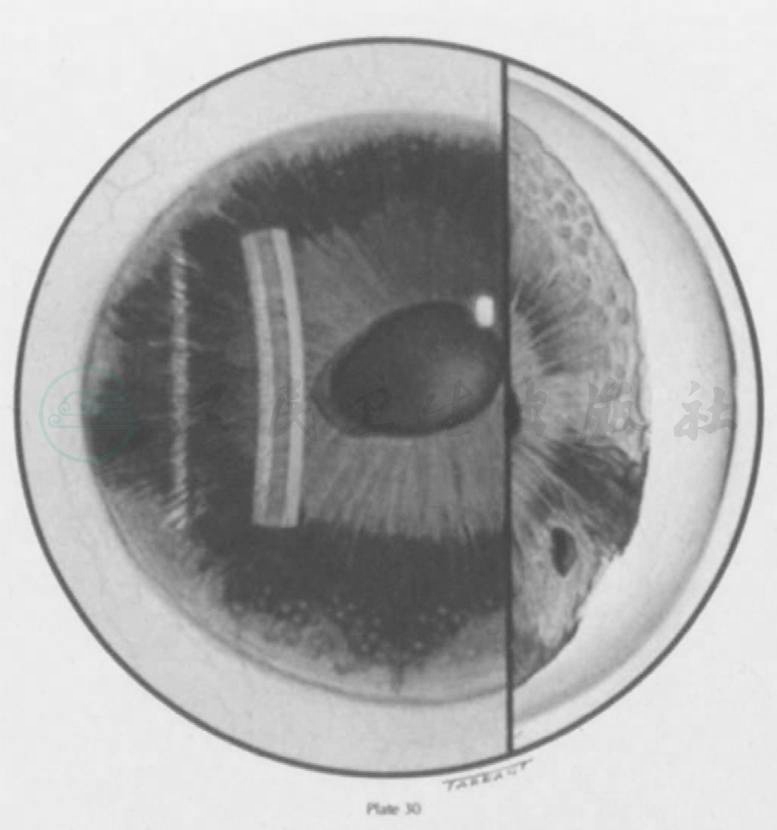
图7虹膜角膜内皮综合征
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
其治疗措施是用前列腺素药物、肾上腺素和碳酸酐酶抑制剂控制眼压。如前粘连有所发展,则应及早手术,但手术效果并不肯定。
(2)Chandler综合征:
本病是上述疾病的一种变异,也是单侧发病。虹膜萎缩较轻且不形成穿孔,但伴有角膜内皮营养不良。继发青光眼时,其程度也较轻。当眼压轻度升高甚至正常时,即可引起角膜实质和上皮的水肿,甚至发生大泡性角膜病变。随着时间的进展,角膜内皮的耐受性下降,更易产生角膜水肿。角膜后壁无沉着物,前房闪光阴性。
治疗措施是用药物将眼压降至最低水平,以防止角膜发生永久性损害。必要时可做滤过手术,也可试用绷带接触镜治疗大泡性角膜病变。
(3)虹膜-痣综合征(iris-nevus syndrome)或Cogan-Reese综合征:
病因不明,其临床表现与Chandler综合征相似,有持续性角膜水肿,虹膜很少穿孔,但虹膜上有弥漫性结节,最初为细小黄色隆起,晚期形成暗棕色有蒂的结节。瞳孔缘色素外翻,眼压正常或稍高。
治疗与前者相同。
2.剥脱综合征(exfoliation syndrome)
剥脱综合征是由于脱屑阻塞房角而引起的一种继发性青光眼,见于老年人。在瞳孔缘、虹膜两面、房角、晶状体囊膜及其悬韧带上均有蓝白色或灰色脱屑及少量色素沉着。在开大瞳孔时,可见云雾状的色素微粒经瞳孔流向前房,晶状体前碎屑的沉着分布成三个区域,中央为半透明的圆盘,周边部有散在的疏密不等的沉着物,两者之间为透明区。
关于这些碎屑的来源,目前的看法还不一致,以往误认为是由晶状体的囊膜剥脱而来,故称为囊膜性青光眼(glaucoma capsulare);有人认为是碎屑沉着于晶状体之上,而不是由囊膜脱下来的,所以称为假性剥脱(pseudoexfoliation)。近年来用电镜观察,发现在晶状体囊内和囊下也有类似的沉着物,证明后一种看法是正确的。最近还发现在虹膜、结膜血管周围和小梁的基底膜上均有一种原纤维性物质(fibrillar material),因而认为这是一种广泛的眼基底膜疾患。因为剥脱物质广泛分布于眼的不同部位故称为剥脱综合征(图8)。
在有脱屑的患者中约30%~80%继发青光眼。剥脱综合征患者的对侧眼的青光眼发生率为15%,较原发性青光眼者明显少,这种病例的皮质激素高度反应者,也较原发性开角型青光眼者为少,这都说明此病是继发性的。既往认为我国此类患者较少,近年来随着对该病的认识,临床仔细观察及我国人口的老龄化,本病并不少见。
本病的临床过程及治疗原则与单纯性青光眼相同。晶状体摘出并不能使病变减轻或停止进展。
3.色素播散综合征(pigment-dispersion syndrome)
是虹膜中周边部后面的色素脱失沉着在眼内各部分,如角膜后面、晶状体表面、晶状体韧带和小梁等处。色素播散综合征可合并或不合并色素性青光眼,而色素性青光眼几乎均有色素播散综合征的表现。
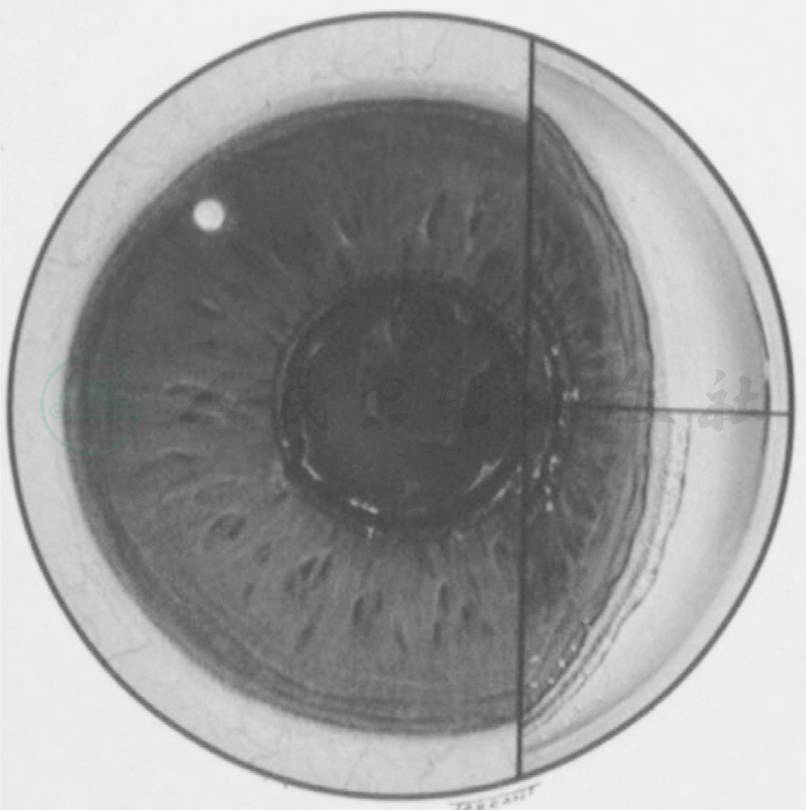
图8剥脱综合征
引自:实用眼科学.第4版.ISBN:978-7-117-31146-5.主编:
4.视网膜色素变性合并青光眼
本病少见。在视网膜色素变性中约3%合并青光眼,常发生于晚期。因视网膜色素变性患者的视野有环形暗点或向心性收缩,故不易由视野改变发现青光眼。治疗与单纯性青光眼相同,因并发白内障,缩瞳剂可使视力明显减退。
七、继发于眼内肿瘤
由于眼内肿瘤使眼内容量增加,或压迫、阻塞房角而引起青光眼。但是眼压升高的程度和青光眼发病的早晚,并不一定与肿瘤的大小和增长的速度一致,而是与肿瘤的部位有密切的关系。房角附近的肿物因直接侵犯房角,或肿物反复出血、机化而破坏了房角结构,可在早期就并发青光眼;眼球赤道部的肿物容易压迫涡静脉,影响脉络膜血液的回流,因此比位于后极部的肿物容易引起青光眼。有时肿物虽然很大,但伴有继发性视网膜脱离,眼压反可正常或较低,而不并发青光眼。治疗时应针对肿物的不同性质选择手术方式。
八、医源性青光眼
1.糖皮质激素性青光眼(corticosteroid glaucoma,简称激素性青光眼)
局部或全身长期应用皮质激素可引起眼压升高。正常人局部滴皮质激素后可引起低度、中度及高度眼压反应(其升高幅度分别为:≤5mmHg、6~15mmHg和≥16mmHg)。正常人的子女中三种不同反应百分比的分布情况与遗传规律所应出现的百分比完全一致,说明皮质激素所引起的眼压升高幅度是由遗传基因决定的。开角型青光眼患者局部滴皮质激素后所引起的高度及中度眼压反应较正常人明显增多。
皮质激素引起的眼压升高是可逆的,停药后可恢复正常,约20%可出现青光眼性视野改变,停药后可消失。地塞米松、倍他米松、泼尼松龙局部应用较易引起眼压升高,而可的松则较少发生。四氢氟羟泼尼松龙(tetrahydrotriamcinolone)和羟甲基孕酮(medrysone)等较少引起眼压升高。局部用药较全身用药引起反应的多见。单眼用药眼压升高明显者,其不用药的对侧眼也可有轻度眼压升高。开角型青光眼患者在用降眼压药物的同时如果应用皮质激素仍可引起眼压升高,其幅度与是否应用降压药物无关。
糖皮质激素试验呈明显高眼压反应者,将来发展为开角型青光眼的可能性较大,可利用皮质激素试验作为一种激发试验。
糖皮质激素引起的高眼压如被忽视而造成永久性的视盘和视野损害,则称为糖皮质激素性青光眼。其临床表现与开角型青光眼相似,但有自愈倾向。
糖皮质激素性青光眼的诊断要点为:有明确的眼局部或全身使用糖皮质激素历史;眼压升高时间、幅度及视功能损害程度和糖皮质激素用量一致;停用糖皮质激素后数天或数周眼压恢复正常;眼局部可出现糖皮质激素所致的其他损害如后囊下型白内障;排除了其他继发性开角型青光眼,如葡萄膜炎性继发性青光眼等。
糖皮质激素性青光眼停用糖皮质激素后,眼压可恢复正常,有些眼压下降但未达正常水平,有些眼压不下降,应进一步鉴别是否合并有原发性开角型青光眼,并对其进行治疗。
防治:首先应注意勿滥用皮质激素。必要时应密切观察眼压,如眼压升高,应及时停药或改用仅有抗炎作用而引起眼压升高作用轻的糖皮质激素如hydroxymesterone。
经药物控制满意的开角型青光眼,在使用皮质激素的过程中而眼压升高时,切勿轻易决定手术,应考虑到皮质激素的作用,首先停用皮质激素,调整和增加抗青光眼药物,一般多能控制眼压。
2.散瞳剂诱发的青光眼(mydriatic glaucoma)
窄房角眼或高褶虹膜者,周身或局部应用阿托品类药物后,可能引起青光眼。可使用缩瞳剂,同时用碳酸酐酶抑制剂及高渗剂治疗。
3.缩瞳剂所致青光眼(miotic glaucoma)
有些病例在用强缩瞳剂(如碘化磷酰胆碱)一段时间后,前房进行性变浅,房角变窄,眼压升高。这是由于晶状体韧带松弛、瞳孔阻滞增加、以及睫状体充血水肿使虹膜根部与小梁相贴而引起的。这种情况易发生于晶状体较厚,尤其是球形晶状体的患者。用散瞳剂可使眼压下降,故又称为逆药性青光眼逆药性青光眼(inverse glaucomainverse glaucoma)。
九、继发于视网膜脱离
视网膜脱离合并青光眼的发生率大约为12%~17%,可由于以下几种情况引起:巩膜缩短术后眼球容积变小,使虹膜晶状体隔前移,或因巩膜缩短部位太靠前而引起房角闭塞。视网膜长期脱离患者的巩膜和睫状体发生水肿,使房角关闭。此病常伴有慢性睫状体炎,其炎性产物可阻塞小梁间隙,但由于房水分泌减少而眼压偏低,当视网膜复位后,房水分泌恢复正常,遂发生急性青光眼。有破孔的视网膜脱离,视网膜色素上皮脱落下来的色素经破孔沉积于小梁网上而引起眼压升高,封闭破孔有助于控制眼压。













