英文名称 :intracranial hemorrhage
中文别名 :出血性脑血管病;出血性卒中
颅内出血(intracranial hemorrhage,ICH)是新生儿期常见病,可分为不同类型,最具特征性的出血类型为早产儿脑室周围-脑室内出血,也可发生硬脑膜下出血、蛛网膜下腔出血、脑实质出血,小脑及丘脑、基底核等部位出血。严重颅内出血可引起小儿远期神经系统后遗症,且近年小胎龄早产儿和极低出生体重儿增多,严重颅内出血及其后遗症仍始终为儿科医生所关注。
脑室周围-脑室内出血(periventricular-intraventricular hemorrhage,PIVH)是早产儿最常见的颅内出血类型,也称生发基质出血,或室管膜下出血(subependymal hemorrhage,SEH)。当出血量增加,血液经破溃的室管膜流入脑室形成脑室内出血(IVH),成为逐渐加重的颅内出血。
1.流行病学
脑室周围-脑室内出血多发生在早产儿,尤其是胎龄<32周、出生体重<1500g的VLBW儿,随胎龄和出生体重降低,发病率增加。有统计,早产儿孕周每减少1周,IVH发生率增加3.5%且重度IVH增加。美国1990年后期报告,出生体重<1500g的VLBW儿,IVH的发生率为20%,出生体重<1000g的ELBW儿,IVH发生率升至45%。美国儿童健康和发育研究所2010年报告,28周前的超早产儿IVH发生率分别是:28周7%,27周11%,26周14%,25周21%,24周26%,23周36%,22周38%。
中华医学会儿科学分会新生儿学组2005~2006年组织了一项我国早产儿脑室周围-脑室内出血发病情况调查,在3769例早产儿中,颅内出血总发生率10.8%,其中重度颅内出血占23%。
在足月儿也可发生PIVH,但重度IVH极少见,且与特殊病因有关,如产伤,同组免疫性血小板减少,血管畸形破裂,静脉窦血栓,血友病或其他凝血功能障碍等。
2.病理与病理生理
脑室周围出血来源于侧脑室的腹外侧室管膜下的生发基质小血管,在尾状核和丘脑之间部位,Monro孔水平。
在胎儿期12~20周时,生发基质是脑神经母细胞和胶质细胞的发源地,进行细胞的快速增殖和移行过程,在此处形成丰富的毛细血管网,满足胎儿期神经细胞、胶质细胞发育,直至32周后绝大部分移行完结,毛细血管网也逐渐消失。
出血原发于这里的微动脉和微静脉收集区。这里的小血管十分脆弱,内皮与外皮细胞缺乏,基底膜细胞不成熟,紧密连接不足,构成血管结构星形胶质细胞足突的胶质纤维酸性蛋白也不足。因此,当缺氧、静脉压增高和渗透压增高时,这些小血管很容易破裂出血。
另与出血相关的组织解剖因素是静脉系统。通过生发基质毛细血管网,组成了深部静脉系统,汇聚成端静脉、髓静脉,不断沿侧脑室侧壁弯曲下行,自然形成“U”字形回路,最终进入中央大静脉。这种特殊的静脉走行使得静脉易于充血、瘀滞,客观上增加了脑静脉压,导致出血(图1)。
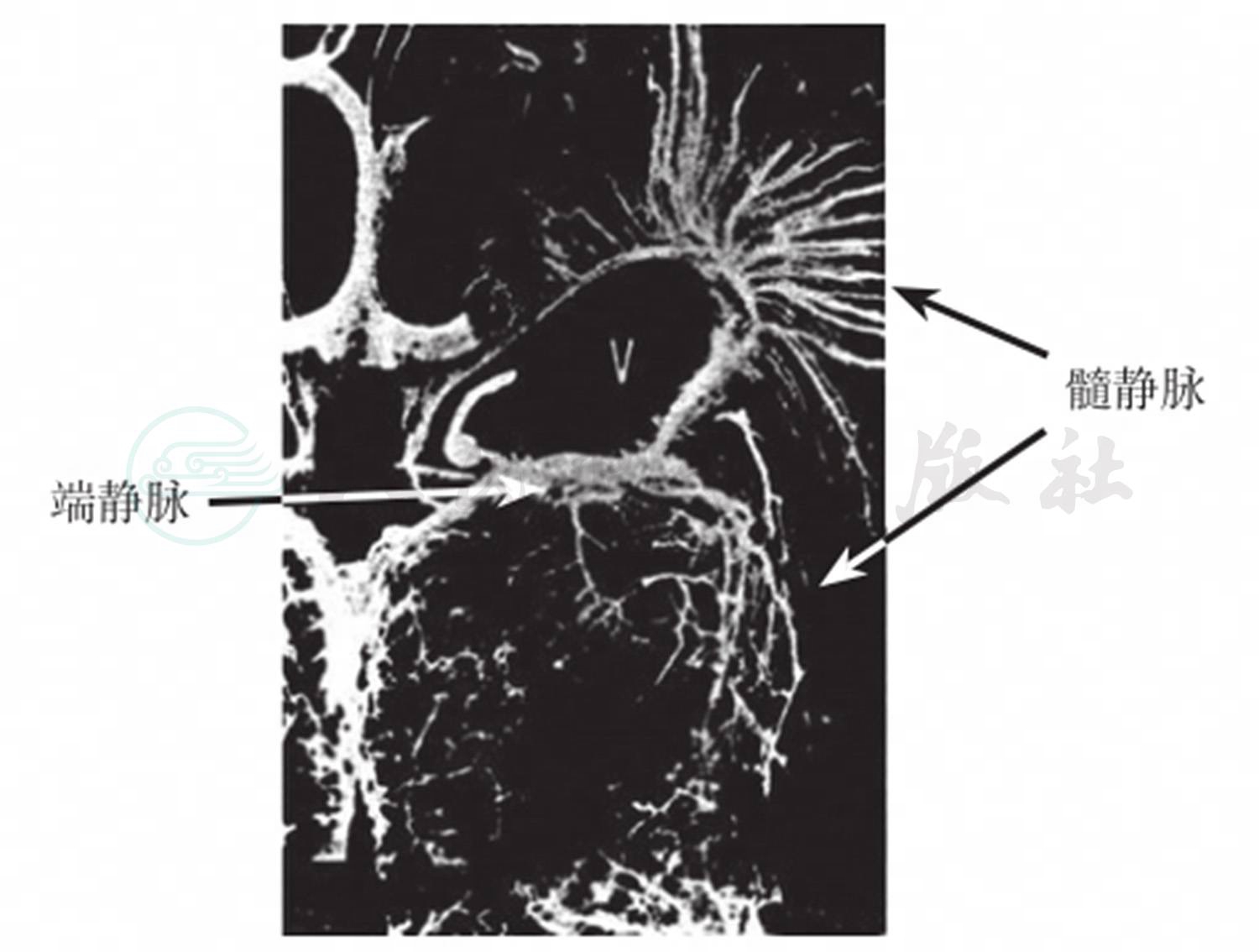
图1 生发基质附近的静脉回流
脑室周围出血后,血液可突破紧邻的室管膜,进入侧脑室。
3.病因
从发病机制而言,所有引发脑生发基质小血管血压、渗透压改变和血管内皮损伤的因素,包括脑血液灌注、颅内静脉压力、血液渗透性改变等病理状态,均可归为出血病因,因此,与产前和产时多种母亲、小儿自身疾病状态有关,同一患儿常多因共同作用而发病。
(1)产前:
多与缺氧有关,如母亲先兆子痫、HELLP综合征、胎儿宫内窘迫。母亲绒毛膜羊膜炎及其他感染性疾病也可通过炎症因子损害血管内皮。母亲产前用药,如吲哚美辛,阿司匹林也可导致胎儿、新生儿颅内出血的发生。
(2)产时:
与异常的分娩方式和过程有关,根本的原因是困难的分娩过程造成小儿脑灌注异常和静脉压增高,危及到脑内小血管,如臀位、肩难产、胎头过度挤压等,这些小儿往往伴随生时、生后窒息缺氧,加重了脑循环异常和小血管损伤。
(3)产后:
与早产儿一些疾病状态和必要的救治过程有关。如呼吸窘迫时呼吸机治疗,新生儿窒息复苏加压给氧,呼吸道、消化道吸引刺激等,易造成脑内动静脉血压升高,血流不稳甚至涨落型脑血流。低碳酸血症、高碳酸血症会影响到脑血管舒缩功能。感染性休克等不同原因所致的低血压,会减少脑灌注,在复苏扩容过程中,过快的输液速度或高渗液体,容易增加脑内小血管的负荷。
4.临床表现
宫内发生的颅内出血很少见,严重出血者多有特殊原因。早产儿PIVH50%发生在生后第1天内,第2天约25%,第3天约15%,4天后发生的出血仅10%。
在临床上表现为以下3种类型:
(1)临床无表现型:
见于出血量较少的病例,占颅内出血病例的25%~50%。此型最为常见,多在早产儿生后常规头颅B超筛查中发现。
(2)断续进展型:
症状在数小时至数天内断续进展,由于出血量较大或渐进性出血所致。此类出血初始表现为兴奋性增高,烦躁不安、易激惹,发展严重时出现颅压高,脑性尖叫、惊厥。进一步恶化继而出现抑制症状,神志异常、四肢张力低下、运动减少、中枢性呼吸异常。
(3)急剧恶化型:
极少见,也称凶险型,发生在短时间内严重出血的早产儿。在数分钟至数小时内病情急剧进展,很快出现意识障碍、眼球固定、光反射消失,有强直性惊厥、中枢性呼吸抑制。同时可出现血压降低、心动过缓、抗利尿激素分泌异常,患儿在短时内死亡。
5.诊断
由于早产儿颅内出血时多无症状,或仅有非特异性的神经系统症状和全身症状,故对该病的确诊依据是影像学检查,在不同的影像学方法中,首选头颅B超,原因是便捷、无创,可床边操作,利于不能搬动的早产儿检查;对脑中央部位病变显示最佳,可冠矢状位扫描,对脑室周围—脑室内出血的诊断具有很高的特异度和敏感度。其检查的作用是:通过超声筛查发现出血,评价出血严重程度,对出血合并症做出诊断。
(1)颅内出血筛查:
对胎龄≤32周的早产儿和具有颅内出血高危因素的近足月早产儿、甚至足月儿,在生后3天内常规进行颅脑B超筛查,及时确诊颅内出血。
(2)对颅内出血严重程度的评价:
颅内出血逐渐严重的基本含义是:生发基质出血量增多,血液突破室管膜进入侧脑室内,又危及到脑室周围脑实质,可能由此造成小儿远期后遗症。1978年Papile提出了PIVH分度标准,在世界各地沿用多年。2008年Volpe又在原有基础上修订了分度标准(图2),如下:

图2 脑室周围—脑室内出血分度
注:A.Ⅰ°颅内出血(生发基质出血);B.Ⅱ°颅内出血;C.Ⅲ°颅内出血;D.Ⅳ°颅内出血。(粗箭头所指为出血性脑梗死)
● Ⅰ度:出血局限于生发基质。
● Ⅱ度:血液在侧脑室内占据容积≤50%。
● Ⅲ度:血液在脑室内占据容积>50%。
● Ⅳ度:在出血同侧的侧脑室旁发生出血性脑梗死。
其中Ⅰ、Ⅱ度为轻度出血,Ⅲ、Ⅳ度为重度出血。不同程度的出血可发生在单侧或双侧。
新的分度标准更注对重脑室内出血量的估计,强调了出血导致的脑实质损伤,即脑室旁出血性梗死,由于生发基质和脑室内出血,发生了静脉血回流障碍现象。
(3)颅内出血合并症的诊断:
指由于脑室周围-脑室内出血引发的脑内其他病变,并造成脑实质损伤,成为神经系统后遗症的病理学基础(图3)。

图3 脑室周围—脑室内出血的合并症
注:A.出血性脑梗死,粗箭头所指为阻碍静脉回流的生发基质出血;B.出血后梗阻性脑积水,双侧脑室扩张;C.出血后脑白质损伤,侧脑室内存在陈旧出血,脑室增宽,箭头所指为受压后损伤的白质。
1)脑室旁出血性梗死(periventricular hemorrhagic infarction,PHI):
最多见于较严重的生发基质出血,脑室内出血也可引发,是早产儿脑室周围-脑室内出血后脑实质损伤类型之一。出血团块影响了侧脑室旁静脉血液回流,使局部静脉血管淤血,继而破裂出血,最终病变区域脑组织坏死、液化,并与脑室相通。头颅B超可显示侧脑室旁出血的生发基质区域回声增强,后发展为液性暗区的病变全过程。
2)出血后脑积水(posthemorrhagichydrocephalus,PHH):
当侧脑室内血液及凝血物质进入第3脑室,又经过狭细的中脑水管时,可发生阻塞,影响脑脊液的正常循环通路,导致双侧脑室、第3脑室内积水,成为梗阻性脑积水。脑积水使脑实质受压甚至变得菲薄,是出血后脑实质损伤的另一严重类型。脑积水发生在重度颅内出血病例,一般在出血后1~2周开始出现,初始无明显症状,脑积水严重时因颅压高而头围增大,前囟隆起,颅缝分离,双眼呈“落日征”。影像学特征是伴随重度脑室内出血,侧脑室进行性增大,直至扩张,伴第3脑室增宽。有时颅内出血后也会发生非梗阻性脑积水,是由于出血后炎症反应影响了蛛网膜颗粒绒毛对脑脊液的再吸收。
诊断出血后脑积水应与脑萎缩相鉴别。有时在脑损伤后脑实质萎缩,脑室被动性增宽,也称稳定性脑室增宽,此时脑室为轻度~重度增宽,脑室内张力不高。
3)脑白质损伤:
重度脑室内出血的显著特征是出血造成脑室增宽,由此挤压脑室周围白质而引发损伤,损伤的结局是脑室周围组织坏死后钙化,或软化灶形成。另外,前述的出血后梗阻性脑积水、出血性脑梗死无疑都会造成脑白质损伤。
(4)颅内出血诊断的其他方法学:
CT、MRI对重度IVH及其合并症同样可以做出明确诊断,而且对同时伴有的脑周边其他损害诊断优于B超,但由于搬运患儿不便,不是理想的筛查手段,对颅内出血的诊断不作为首选。
在无影像学检查的年代,常通过腰椎穿刺脑脊液检查诊断颅内出血。脑室内出血数小时后,脑脊液颜色变黄,葡萄糖减少,蛋白增高。这些变化与细菌性脑膜炎时脑脊液改变相仿,且有局限性,是有创性检查,在影像学广泛应用的今天,几乎不用此方法诊断颅内出血。
在新生儿还可见到颅内其他不同部位的出血,出血病因各不相同,早产儿和足月儿均可发生(图4)。

图4 其他部位的颅内出血
注:A.硬膜下出血;B.蛛网膜下腔出血;C.颞叶脑实质出血;D.小脑出血;E.背侧丘脑出血;F.基底核出血。(除B为CT图片外,其他均是B超图片)
1.硬膜下出血
硬膜下出血(subdural hemorrhage,SDH)多因机械性损伤使硬膜下血窦及附近血管破裂而发生严重出血,所涉及的部位包括上矢状窦、下矢状窦、直窦和横窦,严重时伴大脑镰、小脑幕撕裂。有时硬膜下出血与硬膜外出血并存。此类出血与产伤有直接的关系,常发生于困难分娩的足月新生儿。严重的硬膜下及硬膜外出血近年已很少发生,但少量出血依旧存在,甚至巨大头颅血肿同时,存在颅骨裂隙,而发生硬膜外及硬膜下血肿。
(1)临床表现:
严重横窦和直窦及附近血管损伤所致,后颅凹积血,可压迫脑干,很快出现尖叫、惊厥、脑干症状等神经系统症状,预后凶险,短时内危及生命。下矢状窦出血范围不等,症状不一,少量出血可无突出表现。上矢状窦出血多与异常的胎头吸引产有关,当出血量少时,临床症状轻微,仅表现易激惹等;出血量逐渐增多,出现局限性神经系统异常表现。也有些患儿在新生儿期无异常表现,但由于逐渐形成硬膜下囊肿,有碍脑脊液循环,至数月左右发展为脑积水。
(2)诊断:
有异常分娩过程,特别是存在神经系统症状的小儿,应及时做影像学检查予以定位确诊。CT对早期的脑边缘部位和深部出血诊断敏感性优于B超和MRI。
2.原发性蛛网膜下腔出血
原发性蛛网膜下腔出血(subarachnoidhemorrhage,SAH)指出血原发部位在蛛网膜下腔。此种类型出血在新生儿期十分多见,病因与缺氧、酸中毒、低血糖等因素有关,产伤也可致严重SAH。出血可来自脑发育过程中软脑膜小动脉、小静脉,及其间错综复杂的小血管吻合支,也可来自蛛网膜下腔静脉。
(1)临床表现:
由于出血量不等,症状相差悬殊。出血量很少时,无临床征象,或仅有极轻的神经系统异常表现,如易激惹等,常是在因其他原因做影像学检查时发现,预后良好。此种类型占绝大多数。当出血量增多,血对脑皮质产生刺激,突出的表现是间歇性惊厥,90%预后也良好。大量并急剧进展性出血,血液存留于脑间隙及后颅凹,神经系统异常很快出现,表现为嗜睡、反应低下、中枢性呼吸异常、反复惊厥,危及生命。此类出血极少见,多有出凝血机制障碍或其他特殊原因。
(2)诊断:
蛛网膜下腔出血位于脑周边或脑池、脑窦、脑裂部位,出血早期诊断首选CT,呈现高密度影,在直窦、窦汇或小脑幕上出血时,形成“Y”形或“M”形。
3.脑实质出血
此类出血涉及多种病因,出血部位和程度也有很大不同。
(1)点片状出血:
缺氧窒息可致脑实质小点片状出血,出血很快被吸收,不易发现。有时也会因感染或不明原因的局部小血管破裂而出现局灶性出血。单纯点片状脑实质出血,临床无明显的神经系统症状,也不影响预后。但引发出血的原发病有可能较重,成为神经系统后遗症的原因。
(2)大范围脑实质出血:
多与严重的全身性疾病和脑血管畸形有关。如感染合并DIC或血液系统疾病时,血小板和凝血因子降低,多灶出血,来势凶猛,发展迅速,难以止血。脑血管畸形所致脑实质出血是难以预料的,可发生在任何年龄阶段。足月儿临床常表现为突发惊厥,有时有定位体征,但很快泛化至全身。各种影像学很容易发现脑实质中较大的出血灶。对畸形血管的具体诊断,多是在出血后外科手术和尸解时做出最后的结论。预后与出血灶部位、大小、周围脑组织受压水肿程度、治疗状况均有关。
4.小脑与丘脑基底核出血
(1)小脑出血(cerebellar hemorrhage,CEH):
可以是小脑半球和蚓部的原发性出血,也可以由其他部位出血如第四脑室周围生发基质出血、脑室内出血、后颅凹部位硬膜下出血、蛛网膜下腔出血等扩展而来,早产儿较足月儿多见。出血与产伤、缺氧、脑血流动力学改变等多因素有关。值得注意的是:早产儿颅骨可塑性较强,若枕部受压,鳞状部位前移,如同枕骨骨折,容易增加小脑静脉压,损伤枕骨窦及从属静脉而致出血。
小脑出血的诊断以CT、MRI为佳,超声次之,因出血灶部位较深的缘故。
少量小脑出血可无症状,大量出血易压迫脑干,危及生命。部分足月儿病例赢得了手术治疗时间。存活者可留有意向性震颤、共济失调、肌张力低下、运动受限等神经系统后遗症。
(2)丘脑、基底核出血:
在新生儿期偶可发生,原因可能与疾病状态下血流动力学改变有关。大脑中动脉在颅底水平段发出的豆纹动脉分支供应此区域的血液,这些小血管很细,与主干血管呈90°夹角,很容易受血流动力学影响而破裂出血,故又有“出血动脉”之称。此部位出血范围一般局限,急性期临床无特殊表现,但随访时仍见肌张力异常及脑瘫表现。在新生儿和小婴儿阶段,丘脑和基底核各神经核团间在影像上无明显界限,仅可做大致位置区分。
1.预防
(1)防止早产:
最多见的出血类型是脑室周围-脑室内出血,故减少早产是降低颅内出血发生率的根本措施,尽可能减少小胎龄早产儿。近年十分提倡高危孕妇的产前转运,对增加早产儿胎龄和减少颅内出血均是有益的。
(2)稳定脑血流:
脑血流、颅内压不稳定是脑内小血管破裂出血的直接原因,维持脑血流的平稳状态与产前、产时、产后多个环节有关。如母亲的合并症的治疗与合理用药;分娩时正确的催产、助产措施;生后对高危儿抢救过程尽量避免低氧血症、高氧血症、高碳酸血症、低碳酸血症,高糖血症、低血糖症,高渗液体和过快、过量输液,血压、体温波动,及时关闭动脉导管等,对保护脑血管自主调节功能等、防止或减轻颅内出血均是十分重要的。
(3)不推荐常规使用药物预防:
尽管有一些研究提到一些药物具有某些保护脑血管的药理功用,但尚无临床应用的循证医学依据,不能减少颅内出血和重度颅内出血发生率并改变预后,故不推荐使用,如生后应用吲哚美辛、维生素E、苯巴比妥、布洛芬,生前使用维生素K、硫酸镁等。
2.治疗
颅内出血一旦发生,无特效方法制出血发展,故最好、最直接的治疗是避免前述颅内出血的高危因素,减少任何进一步的损伤,同时监测颅内出血合并症的出现,及时相应治疗。
(1)一般措施:
维持脑内正常脉灌注,保持机体正常氧合状态,适当液量和营养支持,控制惊厥,纠正颅高压。
(2)出血后脑积水的监测与治疗
1)监测:
对重度脑室周围—脑室内出血病例,至少每周颅脑超声检查1次,以发现早期无症状的脑积水。
2)进展性脑积水的处理:
应每日测量头围,注意颅内压增高征象,如前囟隆起,颅缝增宽,每周头围增加>2cm,颅内压>80mmH2O。酌情增加颅脑超声频率,测量脑室径,观察脑积水变化,侧脑室扩张的标准是侧脑室宽4mm以上,大于相应胎龄97百分位。
外科手术治疗是迅速缓解脑积水的有效方法,包括:①侧脑室引流,可直接作脑室外引流,引流管穿过颅骨,一端置于侧脑室内,另一端接无菌引流袋,引出过多的脑脊液。也可采用储液囊的方法,在顶骨区帽状腱膜下埋置储液囊,将脑脊液从侧脑室前角引入囊内。之后用注射针头经头皮穿刺储液囊,定时、定量向外抽吸脑脊液。②侧脑室-腹膜腔分流(ventriculoperitoneal shunts,VPS)是脑积水的最终治疗,将侧脑室内的脑脊液通过分流管持续不断地匀速、定量引入腹腔,以达到持续分流缓解脑室内压力的目的,维持正常的生活质量。但在出血、脑积水早期,如脑脊液中血液及蛋白成分过多,容易梗阻,或同时伴有炎症,不适合做分流术,故前述的侧脑室外引流是分流术的前期阶段。③内镜手术,属微创手术,目前进行不多。可通过脑室镜行室间孔穿通术、第3脑室造瘘术、中脑水管成形术,形成新的脑脊液循环通路,缓解脑积水。
出血后脑积水的患儿中,约40%可自行终止发展,很轻的脑积水不一定进行干预。10%病例为快速进展型,需采取上述方法积极治疗。另有50%为缓慢进展型,其中20%经干预后缓解,无需做分流手术;30%最终需做分流手术方能缓解脑积水。有少部分患儿在新生儿期出院后1年内再次出现脑积水进展,需酌情治疗。故对出血后脑积水患儿至少要随访到1岁。
3)关于其他治疗:
对于脑积水传统的治疗方法之一是早期反复腰椎穿刺减缓脑积水的进展,对此种作法的意见不一。2000年一项Meta分析研究结果,经早期腰穿治疗的脑积水患儿,死亡率和后期残疾率与未经如此治疗的小儿无差别,也有研究报告,有一定的治疗效果。
以往也有采用一些药物减少脑脊液分泌缓和脑积水,如乙酰唑胺、呋塞米(速尿)等,现研究,这些药物均无减少分流手术和死亡的循证医学证据。
有研究,采用纤维蛋白溶解剂-链激酶作脑室内注射,防止血凝,减缓脑积水,至目前无临床应用结论。
(3)出血后脑实质损伤的治疗:
主要指出血性脑梗死、脑室旁白质损伤,以及其他部位出血后对脑实质的挤压、缺血、水肿等各类脑实质损害,是颅内出血后造成远期神经系统后遗症的主要原因。但至今并无有效的使脑细胞从损伤中逆转的药物,促红细胞生成素(rEPO)也仅有十分限局的研究证据,认为有益于脑发育的作用。因此,对出血后脑实质损伤重点是预防重度出血,减少、减轻脑实质损伤。病变早期予以针对性的对症治疗,大范围的脑实质出血、硬膜下出血、蛛网膜下腔出血,必要时予以外科手术治疗,减少对脑实质的挤压,缓解症状,挽救生命。
颅内出血小儿的近远期预后与出血程度、部位、合并症、治疗处理是否得当,以及新生儿的成熟度有直接的关系。主要后遗症为智力运动发育落后、脑瘫、视听障碍、行为异常等。
国外有一些大样本、长期预后的研究报告。小胎龄早产儿发生重度IVH,合并出血后脑梗死的病例,病死率约20%,存活者75%发展为脑积水。轻度IVH病例7%发展为脑积水。
轻度IVH的VLBW儿在3岁后直至18岁,在认知、行为能力方面与无脑损伤的VLBW儿无差别。胎龄低于33周,并发生不同程度IVH的小儿,在5岁时脑瘫的发生率分别是:Ⅰ度8%,Ⅱ度11%,Ⅲ度19%,Ⅳ度50%。













