英文名称 :acute non-lymphocytic leukemia
中文别名 :急性髓细胞白血病
急性非淋巴细胞白血病(acute non-lymphocytic leukemia,ANLL),又名急性髓细胞白血病(acute myelocytic leukemia,AML),是髓系细胞分化发育过程中不同阶段的造血祖细胞恶变转化而来的一组疾病群,其起源分别来自粒细胞系、单核细胞系、红细胞系或巨核细胞系。
AML占儿童所有白血病的20%~25%,新生儿期是发病高峰,婴幼儿至青春期发病率相当,成年期发病率逐年升高。我国发病率约11/100万。AML的发生与遗传和环境因素有关。目前已经发现50%~93%的AML患者有染色体即细胞遗传学异常。单卵双胎中一个在5岁以内患白血病,另一个患白血病的几率为25%。白血病同胞发病率比普通人群高4倍。小儿时期的某些先天性畸形和遗传性疾病如21-三体、Bloom综合征、Fanconi贫血以及先天性纯红细胞再生障碍性贫血等患者白血病的发病率明显高于正常儿童。环境因素包括孕母放射线接触、药物、吸烟及饮食习惯,出生后包括射线、化学药物和毒物接触以及病毒感染。与急性淋巴细胞白血病(ALL)不同的是,儿童AML的分子生物学行为和对治疗的反应与成人较为接近。
人类白血病的确切病因至今未明,许多因素被认为和白血病发生有关。病毒可能是主要因素,此外有遗传、放射及化学物质等因素。
(一)病毒
人类白血病的病毒病因研究已有数十年的历史,但至今只有成人T细胞白血病肯定是由病毒引起。1976年,日本首先报道了成人T细胞白血病/淋巴瘤(adult T-cell leukemia/lymphoma,ATL),美国的Gallo和日本的昭赖夫分别从培养的患者细胞株中分离出C型反转录病毒,分别命名为人类T细胞白血病病毒-1(human T-cell leukemia virus-1,HTLV-1)和成人T细胞白血病病毒(adult T-cell leukemia virus,ATLV),后来证实两者是一致的,ATL高发区也是HTLV-1感染的高发区。HTLV-1具有传染性,可通过乳汁、性交和输血传播。其他病毒如HTLV-2和毛细胞白血病、EB病毒和ALL-L3的关系尚未完全肯定。其他类型白血病无法证实其病毒病因,并不具有传染性。
(二)放射
电离辐射有致白血病作用,与放射量和照射部位有关。一次大剂量或多次小剂量照射均有致白血病作用。全身照射特别是骨髓照射,可致骨髓抑制和免疫抑制,照射后数月仍可观察到染色体断裂和畸变。放射可诱发AML、ALL及CML,但未见CLL,并且发病时常有一段骨髓抑制期,潜伏期为2~16年。孕妇胎内照射可增加出生后婴儿发生白血病的危险性。
(三)化学物质
苯致白血病的作用比较肯定,在1~10mg/L可引起染色体损害,124~200mg/L有致白血病作用,以AML和CML为主。烷化剂、拓扑异构酶Ⅱ抑制剂(如VP16)和细胞毒性药物可致继发性白血病也较肯定,称为治疗相关性白血病(therapy-related acute leukemia,t-AL),尤其是前两类药物。化疗引起的继发性白血病以AML为主,且发病前有一个全血细胞减少期。近年来国内陆续报道乙双吗啉致继发性白血病近百例。该药用于治疗银屑病,是一种极强的致染色体畸变物质,服后1~7年发生白血病(中位数4年)。乙双吗啉所致的白血病主要为AML,尤以急性早幼粒细胞白血病居多。还有报道吸烟和白血病的发病有关。
(四)遗传因素
某些白血病的发病与遗传因素有关。单卵双胎中如一人患白血病,另一个患白血病的几率为20%。家族性白血病占白血病总数的7‰,偶见先天性白血病。部分婴儿白血病被认为与遗传因素有关,常伴有11q23异常。某些遗传性疾病常伴较高的白血病发病率,包括Down综合征、Bloom综合征、Klinefelter综合征、Fanconi综合征和Wiskott Aldrich综合征等,如Down综合征的急性白血病发生率比一般人群高20倍。上述多数遗传性疾患具有染色体畸变和断裂,但绝大多数白血病不是遗传性疾病。
(一)细胞形态学分型
1980年9月和1986年9月,分别在苏州和天津召开全国白血病分类分型讨论会,在FAB形态学分类基础上,提出国内AML形态学分型诊断标准:《血液病诊断与疗效标准》。
1.原粒细胞按形态学分为两型:
①Ⅰ型:典型原粒细胞:胞浆中无颗粒;②Ⅱ型:有原粒细胞特征,胞浆量较少,有少量细小颗粒。原单核细胞和原淋巴细胞也分Ⅰ、Ⅱ型,分型标准与原粒细胞类似。
2.AML分类
(1)M0型(原粒细胞微分化型):此型少见,占AML的3%~5%,髓系过氧化酶(MPO或POX)和苏丹黑B(SBB)染色阳性的原始细胞<3%。该型形态学和ALL-L2相似,容易混淆,M0常有复杂的核型异常,但无特异性,电镜MPO阳性是可靠的诊断指标。
(2)M1型(原粒细胞白血病未分化型):骨髓中原粒细胞占非红系有核细胞≥90%,POX或SBB阳性的原粒细胞≥3%。
(3)M2型(原粒细胞白血病部分分化型):分为M2a和M2b2个亚型,M2a为骨髓中原粒细胞占非红系有核细胞的30%~89%,早幼粒细胞以下阶段>10%,单核细胞<20%,POX或SBB阳性的原粒细胞≥3%。M2b的特点是骨髓中异常原粒和早幼粒细胞明显增多,以异常的中性中幼粒细胞为主,胞核常有核仁,明显核浆发育不平衡,此类细胞的比例大于非红系有核细胞的30%。
(4)M3型(急性早幼粒细胞白血病):骨髓中以颗粒增多的异常早幼粒细胞为主,占非红系有核细胞的30%以上。分为M3a(粗颗粒型)、M3b(细颗粒型)和1种特殊的类型是M3v(细胞呈双叶状或胞浆呈肾型,胞浆内极少颗粒或无颗粒,POX和SBB强阳性),染色体t(15;17)阳性(常为短型,S型)。M3v要注意与M2和M4型白血病鉴别。
(5)M4型(急性粒-单核细胞白血病):按粒细胞和单核细胞形态不同,分为以下4种类型:M4a原粒和早幼粒细胞增生为主,原、幼和成熟单核细胞占非红系有核细胞≥20%;M4b:原、幼单核细胞增生为主,原粒和早幼粒细胞占非红系有核细胞>20%;M4c:原始细胞既有粒细胞系又有单核细胞系形态特征者占非红系有核细胞>30%;M4EO除上述特点外,有嗜酸颗粒粗大而圆,着色较深的嗜酸性细胞占1%~30%。
(6)M5型(急性单核细胞白血病):分为M5a和M5b两种亚型。M5a为未分化型,骨髓原始单核细胞占非红系有核细胞≥80%;M5b为部分分化型,骨髓原单核细胞占非红系有核细胞<80%,原幼单核细胞>30%。
(7)M6型(急性红白血病):骨髓中原始细胞(原粒细胞或原幼单核细胞)占非红系有核细胞≥30%,红系占骨髓有核细胞≥50%,且常有形态异常。若外周血片中原粒细胞或原单细胞>5%,骨髓中原粒细胞或原幼单核细胞应>20%。该型儿童少见。
(8)M7型(急性巨核细胞白血病):外周血有原巨核细胞(小巨核),骨髓中小巨核细胞≥30%,POX和SBB均阴性,需依赖电镜(血小板过氧化酶PPO阳性)或抗血小板单抗(CD41、CD42和CD61阳性)证实。细胞少往往干抽,需要骨髓活检,可见原始和巨核细胞增多,网状纤维增加。M7少见,主要发生于3岁以下婴幼儿。
(二)免疫学分型
在细胞定向分化到红细胞系时,细胞表面出现CD71伴有CD34和CD33的丢失以及CD45表达下降。随着进一步分化,CD71表达也下降,但血型糖蛋白(glycophorin)表达上调,在分化终末期CD45消失;CD33是髓系分化中最早出现的抗原,CD34+及CD33+的细胞可以形成红细胞爆式形成单位(CFU-B)和粒细胞-单核细胞集落形成单位(CFU-GM)。未成熟髓细胞是CD13+,随后出现CD15和CD11b。只在分化终末期才表达CD16和CD10。粒细胞是CD15强阳性,而CD33弱阳性,同时有细胞分布呈高度异质性,CD13和CD11b中度表达。相反,单核细胞是CD33强阳性,但CD15弱阳性,表达CD4。
目前免疫表型尚不能对FAB各亚型进行分析,在髓系白血病的单抗免疫分型及其与FAB分型关系不如急性淋巴系白血病清楚,但对于形态学难以辨认的AML,免疫学分型起重要作用。目前与AML相关的单克隆抗体(表1):
1.粒、单核系:MPO、CD33、CD13、CDW65、CD64、CD15和CD11b。
2.红细胞系:转铁蛋白受体CD71,血型糖蛋白A、C及H。
3.巨核系:HLA-DR、CD41/CD61、CD42、CD36及CD68。
表1 与AML相关的免疫标志
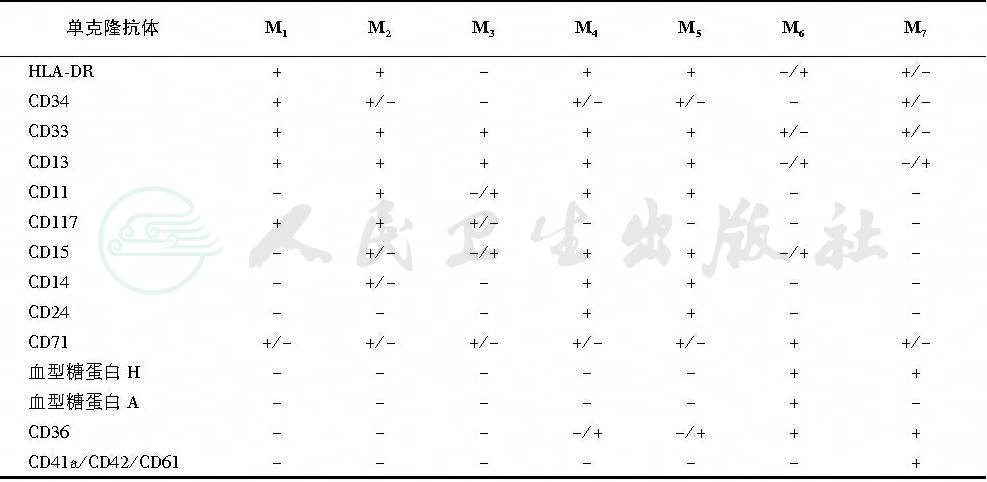
注:免疫标志是指白血病细胞的免疫标志,与正常同系列细胞的标志不完全相同,+、+/-、-/+分别表示抗原表达的强、中、弱
表2总结了AML各亚型流式细胞仪技术分析的特点,结合形态学、免疫学和细胞遗传学(MIC)方法,以达到最大程度的鉴别诊断。
表2 各亚型急性髓细胞白血病流式细胞仪技术分析特点

(一)血象
AML初诊时79%的病例呈中等程度贫血,且呈进行性加重。贫血呈正细胞性,仅少数有红细胞大小不等、嗜碱性点彩、多染性红细胞及幼红细胞,半数病例网织红细胞数偏低。白血病可引起血型抗原减弱,造成血型鉴定困难。初诊时外周血白细胞计数可降低、正常、增高或显著增高。约28.7%的AML患者白细胞计数可低于4.0×109/L,甚至低于1.0×109/L。7.4%的AML患者白细胞可超过100×109/L,称为高白细胞急性白血病。外周血白细胞分类示原始和幼稚(早幼)细胞百分比显著增多,范围在5%~100%,但白细胞不增多性白血病外周血中可仅有极少量甚至没有原始及幼稚细胞出现。初诊时均有不同程度的血小板减少,约半数以上病例低于60×109/L,50.4%患者血小板数低于50×109/L。
(二)骨髓象
初诊时骨髓象大多数呈增生活跃、明显活跃或极度活跃,分类中原始和幼稚(早幼)细胞大量增生,而正常造血细胞如幼红细胞和巨核细胞则明显受抑制。约10%的AML骨髓活检呈增生减低,称为低增生性急性白血病。白血病细胞具有共同的形态特点:大小不一,多数体积增大;核浆比例增大,细胞核形态不规则,常有异形;核染色质粗糙,分布不均,核仁较正常原始细胞大,核分裂象多见;核浆发育失调,细胞分化停滞在原始或幼稚(早幼)细胞阶段,而趋向于稍成熟的细胞极少见,杆状核及分叶核粒细胞尚有保留,呈现所谓“裂孔”现象。Auer小体是白血病细胞的形态学标记,系嗜苯胺蓝颗粒聚集和浓缩过程紊乱融合而成,它的出现率按高低排列如下:AML-M1、M2、M4、M3(34.9%)、M6和M5。Phi小体在AML中的检出率可达92%,其诊断价值较Auer小体为高。不同类型的白血病细胞的形态特征也可有不同(表3),有助于分型诊断。
表3 急性非淋巴细胞白血病细胞的形态特征

(三)细胞化学染色
细胞化学染色体在急性白血病的分型诊断中有重要意义,常用的有过氧化物酶(POX)、过碘酸雪夫染色(PAS)、中性粒细胞碱性磷酸酶(NAP)、α-萘酚醋酸酯酶(α-NAE)及血清溶菌酶等(表4)。
表4 急性非淋巴细胞白血病各型的细胞化学特征
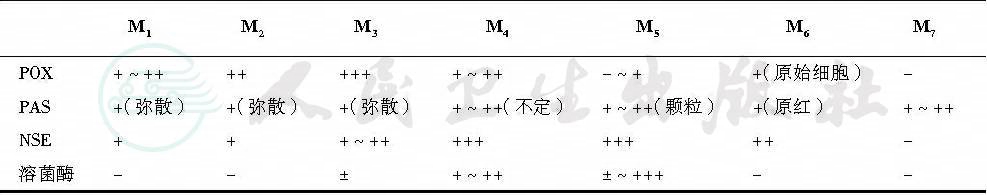
(四)细胞免疫学检查(见前述)。
不同危险组别预后不同,应采用不同的治疗方法,目前多数学者达成以下共识:①低危组除APL外,治疗应以含HD-Ara-C的高强度化疗方案治疗,也可进行自体造血干细胞移植(autologous-hematopoietic stem cell transplantation,AHSCT),不主张采用异基因造血干细胞移植(allo-hematopoietic stem cell transplantation,Allo-HSCT),Allo-HSCT应留待CR2时应用;②中危组复发率较高,一旦复发再次缓解的机会小,因此CR1后应尽早行造血干细胞移植,同胞相合供体的Allo-HSCT是首选,长期DFS约50%,如无法找到合适的同胞供体,也可选择AHSCT或无关供体Allo-HSCT,CR1后单纯用含HD-Ara-C方案进行巩固化疗的DFS只有30%~40%;③高危组缓解后应进行相关或无关供体的Allo-HSCT,长期DFS只有30%左右或更低,而单纯化疗难有治愈的机会。
目前多数化疗方案主要由三类药物组成:第一类是抗代谢类药物阿糖胞苷(Ara-C),第二类是拓扑异构酶抑制剂,如蒽环类、VP16和安吖啶等,第三类是三尖杉酯碱(HA)。近来研究发现在AML治疗中有潜在价值的新药有:①核苷类似物:氟达拉滨(fludarabine)和氯脱氧(chlorodeoxyadenosine);②拓扑异构酶Ⅰ抑制剂:拓扑替康(topotecan)等;③去甲基化制剂:5-胞嘧啶(5-azAra-Cytidine)和地西他滨(decitabine);④铂和烷化剂类似物:卡铂(carboplatin)和tablimustine,主要试用于难治性AML的治疗。抗体靶向治疗和免疫治疗则是新兴的有发展前途的治疗手段。
AML的治疗是以最大程度耐受性的诱导和缓解后治疗为基础的,重视诱导缓解后分层治疗,倡导缓解后尽早采用更强烈而短期的化疗,巩固治疗的疗程尚无定论,掌握造血干细胞移植的适应证,必要时尝试靶向药物治疗。













