急性髓细胞性白血病(acute myelocytic leukemia,AML)可发生于小儿任何年龄,约占小儿白血病20%~30%,无发病年龄的高峰期,男女发病数无差异。其主要临床症状与急性淋巴细胞性白血病(ALL)相似,如:①早期都出现倦怠、无力、烦躁、食欲缺乏、关节痛、多汗、虚弱等;②都出现进行性苍白,贫血逐渐加重,出现活动后心悸、气促,更为虚弱无力;③发热:热型不定,易继发感染;④出血症状:患儿有鼻出血、齿龈、皮肤出血和瘀斑,主要是血小板减少和毛细血管壁被白血病细胞浸润所致渗透性增加;⑤脏器浸润:淋巴结、肝、脾等以及中枢神经系统及睾丸浸润等。
以上主要症状与急性淋巴细胞性白血病基本相同,但是AML还有其特点:①早幼粒细胞白血病(APL、M3)常合并严重出血和DIC。②单核细胞白血病(M5)和粒-单型白血病(M4)多见齿龈肿胀和皮肤浸润。③急性粒细胞白血病(M1、M2)可见眼球突出、复视甚至失明。浸润颅骨、胸骨、肋骨或肝、肾、肌肉等,在局部呈块状隆起而形成绿色瘤,此瘤切面呈绿色,暴露于空气中绿色迅速消退,这种绿色素的性质尚未明确,可能是光紫质或胆绿蛋白的衍生物。④淋巴结、肝和脾大不如ALL显著。
AML的FAB分型:可分为7个亚型:
(1)M1
即急性粒细胞白血病未分化型,骨髓中原始粒细胞≥90%(非幼红系细胞)。
(2)M2
即急性粒细胞白血病部分分化型,又分为2个亚型:
1)M2a:骨髓中原粒细胞占非幼红细胞的30%~80%,单核细胞<20%,早幼粒细胞以下阶段>10%。
2)M2b:骨髓中异常的原始及早幼粒细胞增多,以异常的中幼粒细胞增生为主,其胞核常有核仁,有明显的核浆发育不平衡,此类细胞>30%。
(3)M3
即急性早幼粒细胞白血病,骨髓中以颗粒增多的异常早幼粒细胞增生为主,占非幼红细胞的>30%,其胞核大小不一,胞质中有大小不等的颗粒,又分2个亚型:
1)M3a:为粗颗粒型,嗜苯胺蓝颗粒粗大、密集甚或融合。
2)M3b:为细颗粒型,嗜苯胺蓝颗粒密集而细小。
(4)M4
即为粒-单核细胞白血病,按粒和单核细胞形态不同,可包括下列4种亚型:
1)M4a:以原始和早幼粒细胞增生为主,原幼单和单核细胞占非红系细胞>20%。
2)M4b:以原幼单核细胞增生为主,原始和早幼粒细胞占非红系细胞的>20%。
3)M4c:原始细胞即具粒系,又具单核细胞系形态特征细胞>30%。
4)M4Eo:除上述特征外,有嗜酸颗粒粗大而圆。着色较深的嗜酸性粒细胞占5%~30%。
(5)M5
为急性单核细胞白血病,又可分2个亚型:
1)M5a:未分化型,骨髓原始单核细胞占非红系细胞的≥80%。
2)M5b:部分分化型,其骨髓中原始和幼稚单核细胞占非红系细胞的>30%,原单核细胞<80%。
(6)M6
红白血病,骨髓中幼红系细胞>50%,且常有形态学异常,骨髓非红系细胞中的原始粒细胞(或原始+幼单核细胞)>30%,血片中原粒(或原单)细胞>5%,骨髓中非红系细胞中原粒细胞(或原+幼单)>20%。
(7)M7
巨核细胞白血病。
1)未分化型:外周血有原巨核(小巨核)细胞;骨髓中原巨核细胞>30%,原巨核细胞由组化电镜或单克隆抗体证实;骨髓造血细胞少时往往干抽,活检有原始和巨核细胞增多,网状纤维增加。
2)分化型:骨髓及外周血中以单圆核和多圆核病态巨核细胞为主。
白血病的原始细胞有时形态学难以区分,可借助细胞化学作出鉴别(表1)。
表1 三种白血病细胞化学染色比较
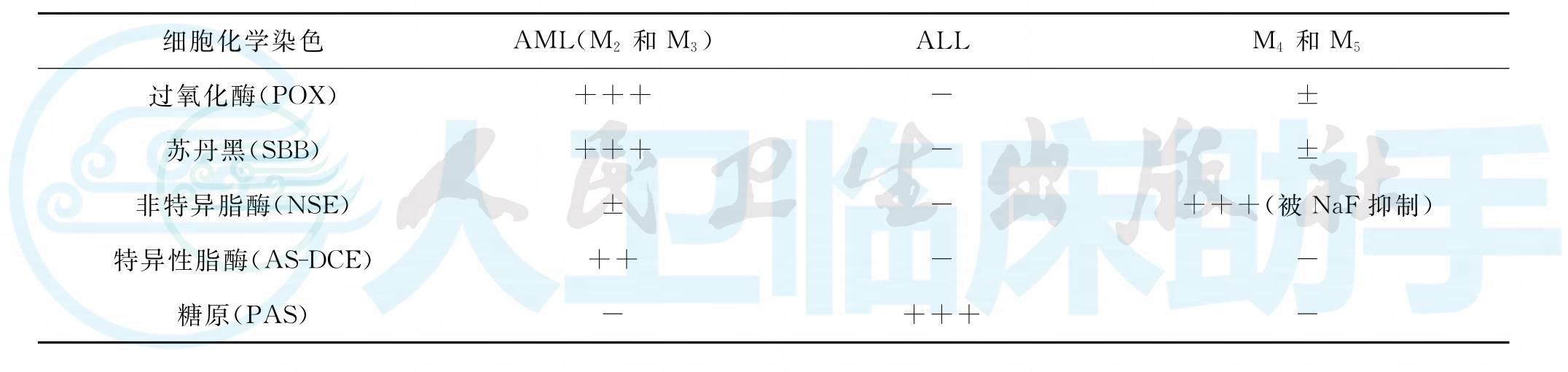
AML应用免疫学标志进行分型尚正在探索中,髓细胞系的免疫膜标志:粒细胞系为过氧化物酶+、CD13+、CD34+;单核细胞系为α-萘酚醋酸酯酶+,可被氟化钠抑制,CD34+、CD13+、CD14+;红细胞系为血型糖蛋白及红细胞膜收缩蛋白+;巨核细胞系为血小板膜糖蛋白Ⅱb/Ⅲa+、Ⅰb/Ⅲa+。
细胞遗传学中,t(8;21)(q22;q22)是M2型的特征;t(15;17)(q22;q12)是M3型的特征;t/del(11;)(q23)是M5型的特征(表2)。
AML的分子生物学标志主要有MLL-AF9、PML-RARα等。
表2 AML的MIC分型

对急性白血病进行染色体检查有助于白血病的正确分型及预后的估计。现在认为白血病是基因病,小儿白血病更是如此!约45%的病例有染色体异常,其中包括单倍体、超二倍体和各种标记染色体。如凡具有t(15;17)的患者几乎都为M3亚型,具有t(8;21)者多为M2亚型。具有11q异常者多为M5亚型等。有t(8;21)和inv(16)的AML患者预后较好,11q异常者预后差。
患儿,女,8岁,以“间断低热1个月,双下肢进行性瘫痪10天,尿潴留3天”为主诉入院。1个月前无诱因间断发热,37.3~38.5℃左右,轻微咳嗽,伴周身乏力不适,多汗。10天来双下肢进行性无力,乃至瘫痪,伴尿潴留3天。无大便失禁。病后偶有双下肢骨痛,无明显出血及苍白。近3天食欲差,精神不振,在当地医院按病毒性脑脊髓膜炎治疗,常规应用抗病毒药物及营养神经类药物治疗无效而来诊。
体格检查:T 38.5℃,P 102次/分,R 26次/分,Bp 12/8kPa(90/60mmHg),BW 34kg,身长134cm,体表面积1.1m2。意识清楚,营养及发育良好,精神萎靡,轻度贫血貌,皮肤无皮疹及出血点,浅表淋巴结不大。头型正常。巩膜无黄染,眼耳鼻正常,咽充血,扁桃体Ⅰ度大,呼吸略促,无三凹征,无发绀,双肺音清。心音有力,律整,心脏无杂音,心率102次/ 分,无杂音。腹平软,肝肋下3.0cm,剑突下未及,质硬Ⅱ度。脾肋下未及。脊柱四肢无畸形,双下肢骨无压痛,活动自如。神经系统:颅神经未见异常。双下肢肌力下降,为Ⅲ级,肌张力弛缓。双膝以下对痛觉不敏感,双膝反射及双跟腱反射减弱,双巴宾斯基征阴性,双凯尔尼格征阴性,布鲁津斯基征阴性。
实验室检查:①血象:WBC 23.8×109/L,N 0.44,L 0.19。见幼稚细胞:早幼粒细胞0.15,中幼粒细胞0.10,晚幼粒细胞0.12。RBC 3.40×1012/L,Hb 115g/L,HCT 31.5%,MCV 96fl,MCH 34pg,MCHC 38%,PLT 56×109/L。②尿便常规正常。③骨髓象:有核细胞增生极度活跃,无核红细胞与有核细胞之比为1000∶270,全片以异常早幼粒细胞为主(占78.4%),以下呈断尾现象,形态大小不等、不规则。胞质丰富,可见内、外质,外质量少,呈天蓝色,无颗粒;内质密布大小不匀的大量粗大嗜天青颗粒,有的掩盖核上,核形不规则(类圆形、肾形、凹陷形、蝴蝶形等),核质粗,核仁1~3个。原始粒细胞5%,淋巴细胞14.6%,红系2.0%;全片未见巨核细胞,血小板少见。过氧化物酶染色(POX)强阳性。
脊髓磁共振检查结果:腰5骶1为中心,密度改变,局部有软化灶及水肿。
诊断为急性早幼粒细胞性白血病,a型。
治疗原则是抢救治疗DIC的同时,治疗和控制感染,治疗原发病。
1.确诊后查DIC指标
凝血时间(试管法)10分钟,凝血酶原时间28秒(对照18秒),凝血酶时间15秒(对照10秒),纤维蛋白原定量1.6g/L(对照2.1g/L),D-二聚体增高,血小板12×109/L,红细胞形态异常,易见三角形、泪滴形、盔甲形等,为阳性。用肝素按0.5mg/kg,加在生理盐水50ml静脉滴注,每隔8小时1次,2次以后复查凝血时间(试管法)。密切观察临床症状及治疗反应,输新鲜血小板10U,补充血小板,肝素继续应用,维持凝血时间控制在20~25分钟之内,每24小时复查DIC项目,至DIC项目逐渐好转及近于正常时,肝素减量及延长用药,10天DIC得到控制。
2.治疗原发病
选用亚砷酸0.2mg/(kg·d),溶解于500ml生理盐水中缓慢滴注5~6小时,每周2次检验血常规。第1周WBC 33.6×109/L,以早幼粒细胞为主0.32,PLT 45×109/L;第2周WBC 39.8×l09/L,以早幼粒细胞为主0.26,PLT 30×109/L;第3周WBC 12.6×109/L,早幼粒细胞下降到0.14,而中晚幼粒细胞增多,说明诱导分化逐渐成功;至第5周接近正常,幼稚粒细胞已消失,红细胞及血红蛋白、血小板基本正常,已达血象缓解。复查骨髓:增生活跃,原始、早幼粒细胞占0.03,达到完全缓解。
联合化疗开始,柔红霉素、阿糖胞苷巩固化疗。之后间断应用亚砷酸治疗,持续2.5年,每3~6个月监测血象、骨髓象及骨髓的融合基因PML-RARα表达,最后停药。
本例长期缓解已达5年,停药已6个月,现已13岁,在中学读书,一切活动正常,体检无异常,基本治愈。
3.治疗中的难点
①DIC的处理:肝素化后,应用血液支持(成分输血),输注纤维蛋白原、抗凝药物及有效控制原发病是治疗的关键。②诱导分化:确诊后立即应用亚砷酸或全反式维A酸可以使早幼粒细胞向下分化、细胞凋亡。砷制剂治疗急性早幼粒细胞白血病的作用机制是通过降解PML/RARa融合蛋白、下调Bcl2基因表达、诱导白血病细胞凋亡,达到治疗目的;治疗过程中要密切注意分化综合征,多数在应用诱导分化剂后的1~3周左右发生,可以发生严重的肺部感染、呼吸窘迫综合征、肺水肿,加重DIC,引起颅内出血,导致死亡。③控制感染:诱导分化中,常并发急性支气管肺炎、败血症、腹泻病等感染。④完全缓解后立即巩固治疗及维持治疗,方能根治。⑤诱导分化开始后DIC控制时即应酌情应用三联鞘内注射,以防治中枢神经系统白血病。













