患者女性,30岁。因“反复腹痛7个月,四肢无力、呼吸困难1周”于2012年4月23日入院。
现病史
患者于7个月前(2011年9月)无明显诱因出现腹痛,为中腹部绞痛并阵发性加重,并停止排气、排便、伴恶心、呕吐,但无发热、皮疹、关节痛等症状或体征。外院就诊立位腹部X线平片提示结肠胀气,诊断“不完全性肠梗阻”。经禁食水、补充液体、灌肠等治疗后症状缓解,结肠镜检查未发现器质性病变。2011年9月至2012年3月上述症状共发作4次,其中1次发作后数天月经来潮,伴四肢近端肌肉疼痛,程度较轻可自行缓解,无肌肉压痛、肢体无力症状与体征。在2次腹痛发作时实验室检测血清抗核抗体谱阴性、红细胞内锌卟啉为2.80μg/gHb(0~3μg/gHb)。10天前(2012年4月13日)再次腹痛发作,伴停止排气、排便、恶心、呕吐,无发热。当地医院实验室检查血常规各项指标均于正常值范围;肝肾功能试验血清谷丙转氨酶122U/L、谷草转氨酶128U/L,血清钠130mmol/L、钾2.80mmol/L,血清肌酐28μmol/L。全消化道造影显示腹部气液平,空、回肠扩张,考虑肠梗阻。腹部CT检查可见胆囊结石,小肠及结肠积气、积液。采取补充液体、纠正电解质紊乱、灌肠治疗。8天前(2012年4月15日)突然出现右侧面部及口角向上抽动,症状持续3~5分钟,共发作2次,发作时无意识丧失、肢体抽搐、大小便失禁,给予苯巴比妥肌内注射,症状未再发作。实验室检查血清钠130mmol/L、钾3mmol/L;头部CT检查未见明显异常。之后患者即出现四肢无力,并逐渐自近端向远端发展,伴肌肉酸痛,但不伴肢体麻木,四肢无力症状呈渐进性加重,并逐渐出现排尿困难。实验室检查血清钠128mmol/L、钾3.50mmol/L;肌酸激酶及甲状腺功能试验正常;反复晒尿未见尿色变深。腰椎穿刺脑脊液检查压力160mmH2O、无色透明,脑脊液白细胞计数0×106/L,葡萄糖、氯化物、蛋白定量均于正常值范围。2012年4月19日出现呼吸困难、咳痰费力,血氧饱和度下降,行气管插管、呼吸机辅助呼吸治疗。监测血清钠124~134mmol/L、钾2.80~3.80mmol/L;2天前出现发热,体温最高时达38℃,为求进一步诊断与治疗入我院急诊抢救室。患者自发病以来一般状况差,纳少、消瘦,发病前曾口服避孕药。否认脱发、皮疹、光过敏、尿色改变、口腔溃疡。
既往史
否认高血压、糖尿病、慢性肝炎、结缔组织病、血液系统疾病病史及长期服药史。个人史、月经婚育史、家族史等无特殊。
入院后体格检查
气管插管、呼吸机辅助呼吸,血压146/90mmHg,心率120次/min。消瘦,神志清楚,查体合作。双侧瞳孔等大、等圆,双眼直接和间接对光反射均灵敏;眼球各向运动充分,未见眼震;面纹对称,闭目有力。双上肢肌力1级、双下肢肌力2级;无肌肉压痛,四肢肌张力降低;腱反射降低,双侧掌颌反射阴性,双侧Babinski征、Chaddock征阴性;四肢末端痛觉过敏,以双足明显,余针刺觉对称。
入院后诊断及治疗经过
入院后完善相关检查,血常规,白细胞计数12.94×109/L、中性粒细胞比例0.82,血红蛋白101g/L,平均红细胞体积83.20fl,平均红细胞血红蛋白浓度371g/L,血小板计数180×109/L;尿、粪便常规正常;肝、肾功能试验,血清谷丙转氨酶、胆红素、肌酐、葡萄糖水平正常;血液电解质检测,钠122mmol/L、钾4.20mmol/L;血液有机化合物、临床酶学检验,血清肌酸激酶、肌红蛋白、红细胞沉降率及C反应蛋白无异常;临床免疫学检验,补体、免疫球蛋白定量均于正常值范围,抗核抗体(ANA)、抗双链DNA抗体(dsDNA)、抗可提取性核抗原抗体(ENA)均呈阴性反应;血清肿瘤标志物检查甲胎蛋白、癌胚抗原、糖基类抗原125、β人绒毛膜促性腺激素于正常值范围;血清及尿液毒物重金属检测未见异常;尿卟啉(uroporphyrin)及尿卟胆原(PBG)均呈阳性反应。心电图呈窦性心动过速。腹部及盆腔超声检查无异常。临床诊断“急性间歇性卟啉病”。给予高糖、大量维生素C、B族治疗,同时予头孢他啶抗感染、保肝、静脉营养、对症支持等治疗,患者病情逐渐好转,体温下降,腹痛明显减轻,呼吸稳定。1周后(2012年4月30日)患者顺利脱离呼吸机,但咳痰无力症状仍存在,无明显腹痛;1个月后(2012年5月22日)病情好转出院,出院时血压104/78mmHg、心率90次/min、血氧饱和度99%。实验室检查血液白细胞计数、血小板计数正常,血红蛋白108g/L;肝肾功能试验无异常。四肢肌力略改善,双侧上肢肌力2级、双侧下肢肌力3级,无腹痛,恢复自主排尿。
神经科医师
定位诊断示,四肢无力,肌张力、腱反射降低,病理征阴性,伴痛觉过敏,定位于周围神经;腹痛、肠梗阻、排尿困难、血压高、心率快,定位自主神经受累;面部口角抽搐,考虑癫痫样发作可能,此外患者发病后期出现持续并难以纠正的低钠血症,考虑可能存在抗利尿激素分泌失调综合征(syndrome of inappropriate antidiuretic hormone secretion,SIADH),因此不能排除中枢神经系统受累。综合定位,周围神经病变症状突出,有四肢及呼吸受累,同时伴有自主神经病变以及中枢神经系统受累可能。定性诊断:患者以腹痛发病,反复发作伴肠梗阻、低钠血症、低钾血症,以周围神经病变症状与体征最突出,发病急、进展迅速,病程中无发热,头部CT、腰椎穿刺脑脊液检查正常,因此定性诊断考虑以下疾病:①急性间歇性卟啉病(acute intermittent porphyria,AIP)。患者为青年女性,以反复发作性腹痛为主要表现,有时与月经有关,之后出现广泛神经系统受累,包括周围神经系统、自主神经系统及可疑中枢神经系统病变,同时伴有SIADH可能,定性诊断首先考虑急性间歇性卟啉病。但是患者在急性发作期血清卟啉检测于正常值水平,而且反复晒尿未见尿色变深,需完善其他相关检查以进一步明确诊断。②吉兰-巴雷综合征。患者为急性发病,四肢无力、呼吸受累,伴有肠梗阻及尿潴留,存在周围神经及自主神经受累,脑脊液检查未发现异常,应考虑吉兰-巴雷综合征的可能。但是该患者存在反复发作性腹痛,发病前无前驱感染病史,可疑癫痫样发作,用吉兰-巴雷综合征不能解释病情全貌,不支持诊断。③周期性麻痹。包括低钾性或血钾正常性周期性麻痹,该患者病程中出现四肢无力及低钾血症,需要考虑周期性麻痹。但是周期性麻痹发病前多有诱发因素,自主神经及呼吸受累者罕见,而且该患者四肢无力已超过1周,补钾、补钠治疗后症状不但无改善,反而进一步加重,因此不考虑周期性麻痹。④其他。包括自身免疫性疾病(特别是系统性红斑狼疮)、中毒、内分泌疾病、感染、副肿瘤综合征等。该患者病程中无发热,否认毒物、重金属接触史,脑脊液检测正常,炎症指标不高,血清自身抗体筛查呈阴性反应,甲状腺功能试验、血清肿瘤标志物筛查各项指标均于正常值范围。因此不支持上述疾病诊断,可进一步完善毒物筛查。
消化科医师
患者肠梗阻部位考虑以结肠为主,全消化道造影及结肠镜检查已排除机械性肠梗阻,故诊断为假性肠梗阻。假性肠梗阻分为原发性和继发性两类,原发性假性肠梗阻是由于肠平滑肌异常或肠神经系统异常造成;继发性假性肠梗阻的病因包括结缔组织病(如系统性红斑狼疮)、内分泌疾病(如甲状腺功能减退)、肿瘤、感染、神经系统疾病等。该患者假性肠梗阻病因需考虑以下情况:①自身免疫性疾病。患者为青年女性,为自身免疫性疾病好发年龄,同时伴有多系统受累,包括消化系统、泌尿系统及神经系统,首先应考虑系统性红斑狼疮,但是患者血清自身抗体筛查均呈阴性为不支持点,建议复查。②代谢性疾病。患者腹痛反复发作,有神经系统受累,需考虑急性间歇性卟啉病的可能,该病可以反复出现假性肠梗阻,一般认为是由于自主神经病变使肠平滑肌的神经支配不平衡,或卟啉前体的毒性作用引起肠痉挛所致,病情加重与月经相关也是其特点,需要警惕。但是患者血卟啉筛查呈阴性,不支持诊断。③中毒。亦应考虑重金属中毒,例如铅、砷、铊中毒均可出现消化系统、神经系统受累类似表现,可造成腹痛和正细胞性贫血,下一步可完善毒物检测。④内分泌疾病。需要警惕是否存在神经内分泌肿瘤的可能,可完善奥曲肽显像及相关检查。
血液科医师
纵观患者整体临床经过,不排除急性间歇性卟啉病的可能。卟啉病是血红素合成途径障碍造成的代谢性疾病,致使卟啉或卟啉前体过度产生并在组织中蓄积,从而造成皮肤和神经系统损害。卟啉病大致可分为3种类型:①肝细胞性卟啉病,其中以急性间歇性卟啉病最为常见。②皮肤迟发性卟啉病。③红细胞生成性卟啉病。急性间歇性卟啉病为卟胆原脱氨酶(PBGD)缺陷导致卟胆原在体内堆积,引起典型的三联征,即腹痛、神经精神异常和红色尿。但是该患者血卟啉筛查阴性、反复晒尿无颜色改变,为不支持之处,建议进一步行尿卟啉及尿卟胆原试验,必要时可多次复查。治疗方面,建议应用高糖及大量维生素C静脉输注。
神经科医师
患者尿卟啉及尿卟胆原检测均呈阳性反应,急性间歇性卟啉病诊断明确。经静脉输注高糖及大量维生素C治疗,以及抗感染、保肝、营养神经、对症支持等治疗后患者病情逐渐好转,体温下降、腹痛症状减轻,顺利脱离呼吸机。出院时生命体征平稳,四肢肌力略有改善,呼吸稳定,无腹痛发作,并已恢复自主排尿。
急性间歇性卟啉病(acute intermittent porphyria,AIP)
急性间歇性卟啉病(acute intermittent porphyria,AIP)为常染色体显性遗传性代谢病,由于血红素生物合成途径中特异性酶卟胆原脱氨酶(PBGD)的缺乏导致卟啉代谢紊乱,引起卟啉前体δ-氨基-γ-酮戊酸(ALA)和卟胆原(PBG)在体内堆积,血红素生成障碍,是卟啉病中最为常见的临床类型,可以影响周围神经、自主神经和中枢神经系统。目前急性间歇性卟啉病造成神经系统损伤的确切发病机制尚不十分清楚,现有证据显示,一方面卟啉前体的聚集具有直接的神经毒性,另一方面血红素生成减少造成能量衰竭,两者共同作用导致神经纤维轴索变性。
急性间歇性卟啉病急性发作多见于20~40岁年龄阶段,女性发病为男性的5倍,常见诱因包括药物(如巴比妥类、磺胺等)、内源性甾体激素增多特别是孕酮、饥饿或低糖饮食、吸烟、饮酒、感染、创伤、精神刺激等。其临床表现多样,常以间歇性腹痛发病,可伴有各种神经系统受损表现,其中周围神经、自主神经症状多见,中枢神经系统损害少见(表1)。由于患者体内卟啉水平并不升高,故无光感性皮损。发作时尿呈红色或日晒后变成红色。发作期可出现SIADH,考虑具有神经毒性的卟啉前体物质聚集作用于无血-脑脊液屏障保护的下丘脑渗透压中枢,导致抗利尿激素(ADH)分泌失调;部分患者发作期血红蛋白水平降低,间歇期可恢复正常。正是因为急性间歇性卟啉病的临床表现复杂而且缺乏特异性,因此临床明确诊断困难。
表1 急性间歇性卟啉病的神经系统表现
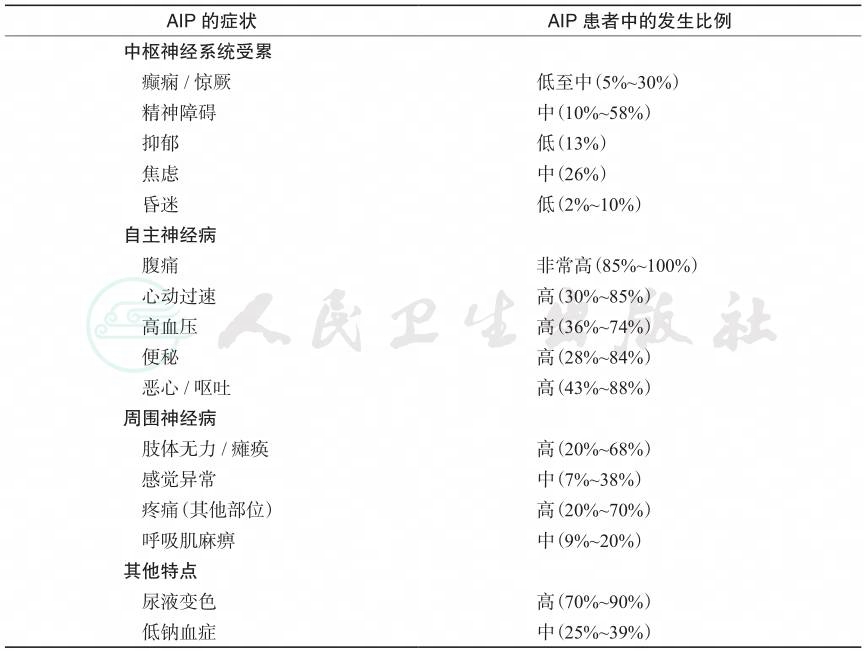
AIP的症状 AIP患者中的发生比例 |
中枢神经系统受累 癫痫/惊厥 低至中(5%~30%) 精神障碍 中(10%~58%) 抑郁 低(13%) 焦虑 中(26%) 昏迷 低(2%~10%) 自主神经病 腹痛 非常高(85%~100%) 心动过速 高(30%~85%) 高血压 高(36%~74%) 便秘 高(28%~84%) 恶心/呕吐 高(43%~88%) 周围神经病 肢体无力/瘫痪 高(20%~68%) 感觉异常 中(7%~38%) 疼痛(其他部位) 高(20%~70%) 呼吸肌麻痹 中(9%~20%) 其他特点 尿液变色 高(70%~90%) 低钠血症 中(25%~39%) |
急性间歇性卟啉病的周围神经损害以运动神经受损更为突出,发病初期可以有肌肉疼痛,之后逐渐出现肢体无力,若未予有效治疗,通常在发病约2周后出现四肢瘫,其中很少一部分患者会出现呼吸麻痹或死亡,临床少见而且知晓率较低。该例患者呈急性发病,2天后即出现四肢瘫,随即进展至呼吸衰竭,与常见的急性间歇性卟啉病临床发展过程不符,病情进展迅速、临床症状严重,究其原因不排除与病程中应用苯巴比妥治疗有关。巴比妥类药物为诱导肝细胞色素P450酶的药物,其生物代谢需消耗大量血红素,使血红素对δ-氨基-γ-酮戊酸合成酶(ALAS)的负反馈抑制作用减弱,ALAS生成增加,卟啉前体增多,诱发病情进一步加重。
目前急性期实验室检查尿卟胆原被推荐为一线首选诊断方法。如果尿卟胆原明显升高(5~10倍),即可确诊急性间歇性卟啉病;若尿卟胆原正常,即可100%排除急性间歇性卟啉病。其次还可以选择检测粪便或血清卟啉,但检测结果正常者不能排除急性间歇性卟啉病。另外,还可以行卟胆原脱氨酶的酶学分析或基因检测。临床常用检测方法是将尿液放置于阳光下暴晒,若尿色变成酒红色即支持卟啉病的诊断,原因是卟啉及其衍生物吸收日光后被激活放出红色荧光,以尿卟啉最强,然而卟胆原无光感作用,故尿液经光照后若不变红色,亦不能排除急性间歇性卟啉病。该例患者在发病初期即已怀疑急性间歇性卟啉病,进行血卟啉检查,发病后期反复晒尿均无阳性发现,直至尿卟胆原检测阳性,急性间歇性卟啉病最终得以明确诊断。因此,选择恰当而具有特异性的实验室检查方法,对疾病诊断至关重要。
急性间歇性卟啉病目前尚无有效根治方法,急性发作时具有较高的病死率,尤其是延误诊断及神经系统表现进展者。急性期治疗主要包括以下几方面:①避免诱因,特别是避免应用可诱导肝细胞色素P450酶的药物。②特异性治疗,静脉输注血红素或高糖,两者均可抑制ALAS活性,减少卟啉前体的合成。此外,高糖还可同时增加肝糖原储存,阻断因消耗、脱水、电解质紊乱所造成的恶性循环。对于危重症患者,血红素(可从国外购得)是抢救急性间歇性卟啉病的有效手段,防止因神经损害、呼吸麻痹造成死亡。糖皮质激素类药物疗效尚不肯定。③支持治疗,包括机械通气、静脉营养、止痛等治疗。癫痫发作的治疗相对困难,因为绝大多数抗癫痫药物都会加重病情,可以选择不诱导肝细胞色素P450酶的药物,例如加巴喷丁、左乙拉西坦。
综上所述,急性间歇性卟啉病的临床表现多样,应予以重视。女性患者不明原因腹痛、神经系统受累或精神症状,或伴有低钠血症者,需警惕急性间歇性卟啉病。当临床高度怀疑急性间歇性卟啉病时,选择正确的实验室检测方法尤为重要。在不排除急性间歇性卟啉病的情况下,用药需谨慎。早期发现,正确诊断,及时治疗,是避免急性间歇性卟啉病不可逆并发症的关键。
[1]Kauppinen R.Porphyrias. Lancet,2005,365 (9718):241-252.
[2]Thadani H,Deacon A,Peters T.Diagnosis and management of porphyria.BMJ,2000,320 (7250):1647-1651.
[3]Anderson KE,Bloomer JR,Bonkovsky HL,et al.Recommendations for the diagnosis and treatment of the acute porphyrias.Ann Intern Med,2005,142 (6):439-450.
[4]Kahn MJ,Gregory SA. Iron metabolism,iron overload and the porphyrias.American Society of Hematology Self Assessment Program.3rd ed. Lancaster,Pa:Cadmus Communications,2007:75.
[5]Beganovic S,Hendler F,Herzig R,et al.Porphyria:diagnosis//Djulbegovic B.Reasoning and Decision Making in Hematology.New York:Churchill Livingstone,1992:67-75.
[6]Stein PE,Badminton MN,Barth JH,et al.Acute intermittent porphyria:fatal complications of treatment.Clin Med,2012,12 (3):293-294.
[7]张君怡,朱以诚,崔丽英,等.反复腹痛四肢无力呼吸困难.中国现代神经疾病杂志,2013,13 (4):354-357.













