作者:张思寒(主任医师 福建省消化系统肿瘤与上消化道疾病临床医学研究中心)
指导者:陈丰霖(主任医师 福建医科大学附属协和医院消化科)
肝豆状核变性由Wilson(1912年)首先报道和描述,故亦称Wilson病(WD),是一种常染色体隐性遗传的铜代谢障碍性疾病,主要特征为铜蓝蛋白合成不足以及胆道排铜障碍,最终导致肝硬化和脑部基底核变性疾病。本病在中国较多见,全球范围内报道的肝豆状核变性发病率为1/30000~1/10000。致病基因携带者约为1/90。肝豆状核变性也是至今少数可治的基因病之一。肝豆状核变性好发于青少年,10~25岁出现症状,晚发者极少见。3~55岁起病较缓慢,男性稍多于女性。临床表现多种多样。临床常分肝型、脑型、混合型和其他4型,以肝型为主。儿童期患者常以肝脏损伤为首发症状,可见肝大,肝炎,非特异性谷丙转氨酶升高,质较硬而有触痛,肝脏损伤逐渐加重可出现肝硬化症状,脾大、脾功能亢进,腹水、肝昏迷、肝衰竭等,可以肝衰竭为首发症状。肝脏损害年龄为11.4岁。脑部症状根据受损部位不同,临床表现也不同,其中尾状核、壳核受损者常以细微的震颤、言语不清或动作缓慢为其首发症状。典型者以锥体外系症状为主,如帕金森综合征样症状、运动障碍;大脑皮质受损,精神症状以情感不稳和智能障碍较多见,严重者面无表情,无故哭笑;有时可出现癫痫样发作;小脑受损,共济失调、语言障碍。脑部症状平均发病年龄为18.9岁。肾脏损害:因肾小管,尤其是近端肾小管上皮细胞受损,可出现蛋白尿、糖尿、氨基酸尿等,部分患者还可发生肾小管性酸中毒。血液系统受损:急性血管内溶血,急性非免疫性血管内溶血,至少15%的患者溶血表现明显;其他部位,如骨骼、心脏、皮肤、内分泌等有受损情况。
肝豆状核变性的发病机制:从食物吸收的铜离子和血浆白蛋白结合(疏松)运送到肝脏,在肝细胞膜表面P型铜转运ATP酶的作用下与α2球蛋白结合(紧密)成具有氧化活性的铜蓝蛋白释放入血,部分通过胆道排出体外,部分通过肾脏从尿液排出。编码P型铜转运ATP酶的ATP7B基因突变,导致P型铜转运ATP酶的功能缺陷丧失,继而出现大量铜离子沉积在肝脏、肾脏、角膜、豆状核等部位,产生大量氧自由基,损伤各个脏器。
肝豆状核变性的辅助检查:①血清铜蓝蛋白降低,<0.2g/L为异常,<0.08g/L是诊断肝豆状核变性的强有力的证据(正常值为0.2~0.5g/L)。②24h尿铜增高,正常人尿铜排泄量<40μg/24h,未经治疗患者多为200~400μg/24h,个别高达1200μg/24h,亦有少数患者尿铜量正常或稍高。青霉胺试验对肝豆状核变性的诊断具有辅助意义。口服500mg青霉胺,12h后开始收集24h的尿液,24h尿铜>1 600μg则支持诊断。③头颅CT及MRI,早期无特异性改变。CT可显示双侧豆状核对称性低密度。MRI比CT特异性高,表现为豆状核、尾状核、中脑、小脑、额叶皮质等T1低信号和T2高信号。脑电图示脑诱发电位均可有不同程度的异常,但没有特异性。因此,在头颅CT及MRI上病变可以不典型,典型的熊猫脸影像学特征仅见于中国人肝豆状核变性(WD)患者。④眼科裂隙灯检查可见角膜边缘细微的色素颗粒沉积,称K-F环,宽约1.3mm,绿褐色或暗棕色色素环,为本病重要体征,一般于7岁之后可见。但仅40%的肝性肝豆状核变性患者可见此表现。⑤基因检测是金标准,对于不能确诊的儿童肝豆状核变性行肝铜检测有助于诊断。⑥Leipzig评分:若总分在0~1分,可基本除外肝豆状核变性;2~3分,有肝豆状核变性可能;≥4分,肝豆状核变性可确诊。只要发现两个部位基因突变,分值为4分,就可以确诊WD。
肝豆状核变性的治疗:①低铜高蛋白饮食。应避免食用含铜高的食物(坚果类),禁用铜制食具。若饮用水含铜高,则尽量使用去离子水或蒸馏水。②补锌治疗。减少铜的吸收,锌能够竞争性地抑制铜在肠道的吸收,使粪铜排出增加。大龄儿童或成人一般锌离子补充量为150mg/d,分3次给药;体重<50kg的儿童用量为75mg/d,分3次给药。③金属络合剂治疗。青霉胺是首选,用于驱铜,可络合血浆和组织中的铜,并促进铜从尿液排出。首次用药前应做青霉素皮试。一般起始用药量为250~500mg/d,分2~4次给药,然后每4~7d加量250mg。维持治疗用量为750~1000mg/d,小儿给药一般按20mg/(kg·d)计算,分2~3次给药。④其他金属络合剂,如三乙基四胺(trietyl tetramine)。
肝豆状核变性的预后:该病需要终身治疗,如早期确诊,规范给予有效治疗,预后可。对任何肝豆状核变性所致急性肝衰竭的患者,均应考虑肝移植治疗或立即进行肝移植治疗。对铜离子螯合剂治疗无效的失代偿肝硬化肝豆状核变性患者应立即进行肝移植评估。
1.患者基本情况
患者:女性,61岁,汉族,青海省籍,农民。
入院时间:2018年3月27日。
主诉:胸闷、乏力伴腹胀20余天。
现病史:患者于20d前无诱因出现胸闷、气喘,平躺后加重,出现乏力、食欲减退,尤其是双下肢无力,活动明显减少,在家卧床休息,继而出现腹胀,腹围逐渐增大,小便量少,伴双下肢水肿。遂就诊于××医院并住院,后完善相关实验室检查,诊断肝硬化失代偿期,肺部感染、胸腔积液、腹水,原发性肝癌?并给予抗炎、胸腔穿刺、输注白蛋白,利尿等对症治疗后患者症状缓解,出院,患者为求进一步明确肝硬化原因,遂再来我院,门诊以肝硬化原因待查收住我科。
既往史:发现头部、双上肢不自主震颤5年,曾多次就诊于我院及××医院神经科,最终诊断为特发性震颤,2008年初建议手术治疗,患者因经济困难拒绝手术,也未服用药物。2015年因子宫肌瘤住我院治疗,行子宫全切术,当时术中无出血情况,创面恢复良好,当时肝功能正常,腹部彩超提示脂肪肝。否认高血压、冠心病、糖尿病、高血脂等病史,否认肝炎、结核等病史,无输血史。
个人史:久居青海,否认饮酒史、无长期服药史。婚育史、月经史:15,3~5/30,50,G1P1,配偶及一女均体健。
家族史:否认家族遗传史,母亲健在,父亲因肺心病去世20余年,同胞兄弟姐妹5人,均体健。
2.入院查体
一般生命体征:T 36.4℃,P 71次/min,R 20次/min,BP 120/60mmHg。发育正常,步入病房,神志清楚,精神欠佳,言语清晰流利,对答切题,查体合作,体形中等。皮肤黏膜无苍白,无黄染及出血点、瘀斑等,面色萎黄,未见肝掌及蜘蛛痣。全身浅表淋巴结未触及肿大。头颅无畸形,五官端正,眼睑无水肿,球结膜无充血水肿,巩膜无黄染,头部不自主震颤。颈软无抵抗,甲状腺不大,颈静脉无怒张,肝颈静脉回流症阴性。双肺呼吸音粗,叩诊呈清音,未闻及干湿啰音及胸膜摩擦音。心率80次/min,心律齐,各瓣膜听诊区未闻及病理性杂音。腹部平坦,肝脾肋下未触及,全腹无压痛及反跳痛,移动性阴性,肠鸣音正常3~5次/min,双下肢无水肿。双下肢关节活动自如,无红肿,双上肢不自主震颤,四肢肌力及肌张力5级。双侧生理反射对称引出,病理征阴性。
3.初步诊断思维过程
(1)入院时病情总结
该患者为中老年女性,病史20余天,以胸闷、乏力、腹胀为主要表现,在外院已明确诊断为肝硬化失代偿期,同时,双上肢及头部不自主震颤表现突出,曾经在我院神经科多次就诊,最终就诊于××医院神经科,诊断特发性震颤,建议手术,患者拒绝。
(2)入院时诊疗思路
患者在外院已诊断为肝硬化失代偿期,胸腔积液,腹水,脾大,脾功能亢进,原发性肝癌可能。目前,肝硬化原因目前不明,原发性肝癌仍不明确,需进一步检查明确。患者既往已明确特发性震颤。
(3)入院初步诊断
肝功能失代偿期,脾大,脾功能亢进,原发性肝癌? 特发性震颤。
4.后续检查
入院后检查:血常规、大便常规、尿常规、生化、凝血功能、肿瘤指标、X线胸片、心电图、上腹部CT、胃镜、肝脏弹性检测、肝穿刺、血清铁、转铁蛋白、铁蛋白、铜蓝蛋白、头颅MRI、24h尿铜、血清基因检测。
部分检查结果如下:
血常规:白细胞计数2.97×109/L,血红蛋白126g/L,血小板计数51×109/L,考虑与脾功能亢进有关。
大便常规:正常;尿常规:正常。
凝血功能:PT 13.5s,PT 76.8%,INR 1.13,APTT 33.7s,活化部分凝血活酶时间比值(activated partial thromboplastin time ratio,APTT-R)1.1,均正常。
肝功能:GPT 35U/L,GOT 32U/L,TBil 16.9μmol/L,DBil 4.2μmol/L,IBil 12.7U/L,GGT 451U/L,ALP 142U/L,ALB 27.5g/L,胆碱酯酶(cholinesterase,CHE)1 755U/L,总胆汁酸(total bile acid,TBA)56.64g/L,提示肝内胆汁淤积表现。
肾功能、胰功能、心功能均正常。
肿瘤指标:AFP 112.5ng/mL,FER 261.00ng/mL,余均正常。
肝炎病毒:均阴性,自身抗体:ANA1100,其他均阴性。
X线胸片:右侧少量胸腔积液。
心电图:未见异常。
腹部CT:肝脏多发大小不等的增生结节,肝裂增宽,肝表面凹凸不平,未见肝内外胆管扩张,脾大,肝囊肿(图1)。
胃镜:慢性萎缩性胃炎,胃角溃疡A1,未见食管-胃底静脉曲张。
肝脏弹性检测:体重指数(body mass index BMI)23.7kg/m2,肝脏硬度35.5,脂肪衰减系数227,提示肝硬化。
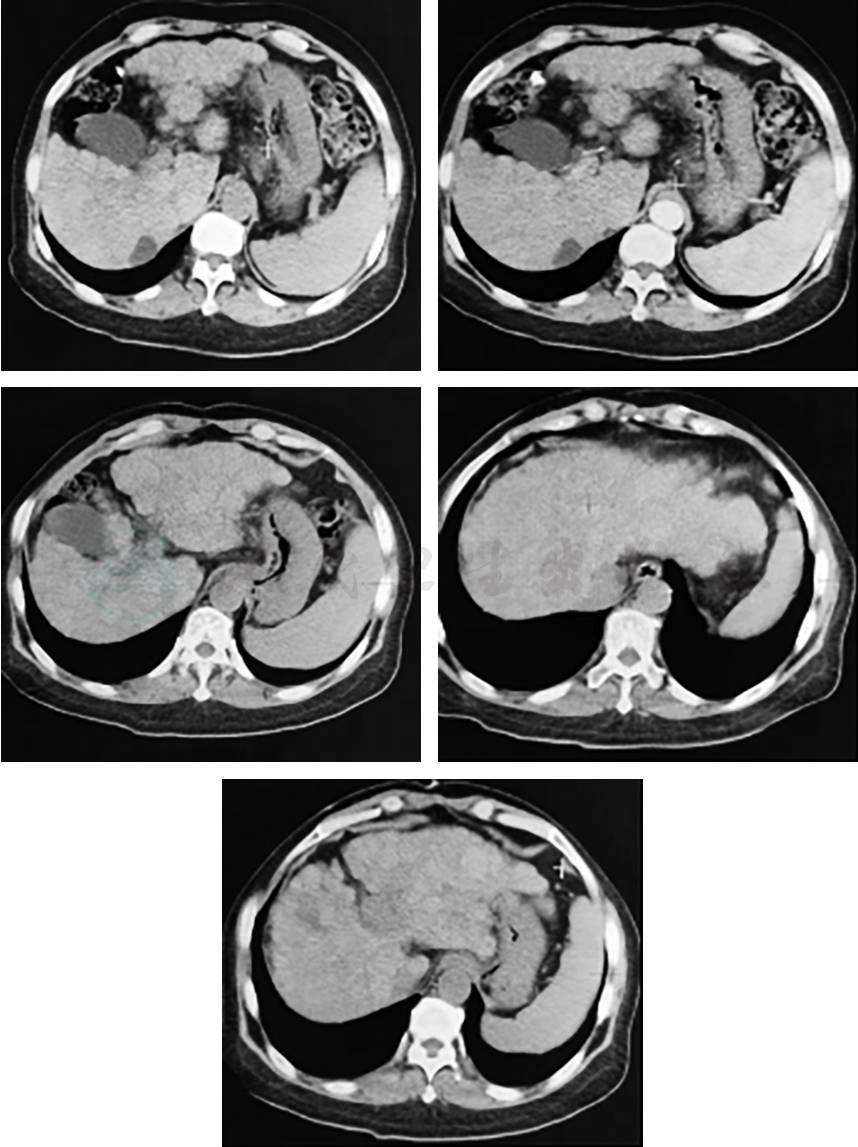
图1 腹部CT
进一步检查:结合上述实验室检查结果考虑该患者诊断肝硬化明确,但肝硬化原因仍然不明,目前初步排除病毒性肝病、药物性肝病、酒精性肝病、心源性肝病等引起的肝硬化,但临床上自身免疫指标阴性的自身免疫性肝病常见,或者非酒精性脂肪性肝病,或者有/无其他不明原因的肝硬化,故进一步完善肝穿刺。在肝结节处穿刺(图2),标本合格,未见恶性细胞,排除原发性肝癌。
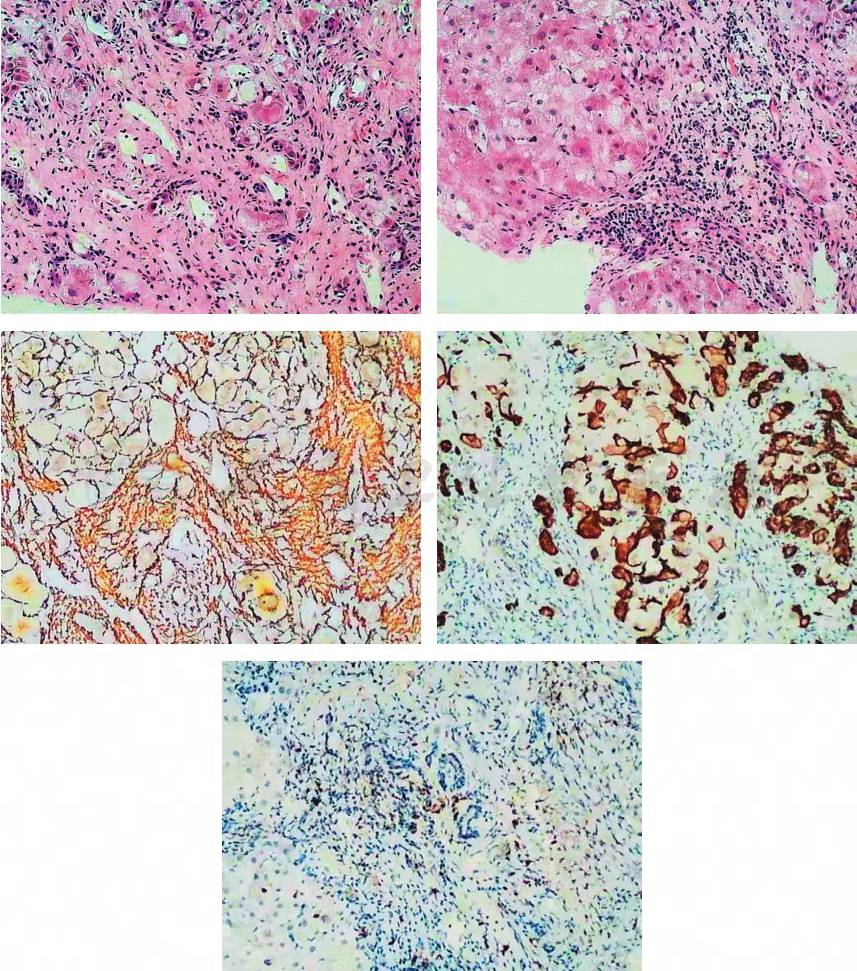
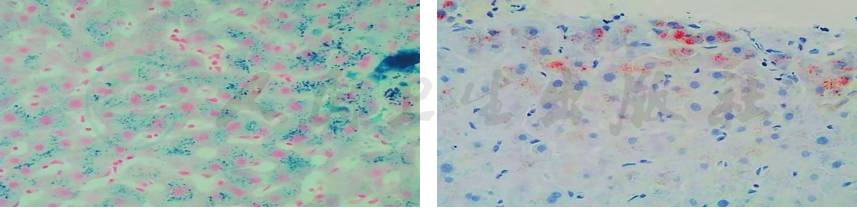
图2 肝穿刺结果(HE染色、SP染色,中倍放大)
结合肝穿刺结果考虑该患者需排除肝豆状核变性、血色病等疾病,故进一步完善相关检查。结果见:血清铁22.0μmol/L,铁蛋白261.00ng/mL,转铁蛋白128.0mg/dL,意外发现铜蓝蛋白6.6mg/dL,明显下降。眼科会诊(图3):K-F环阳性(K-F环大多出现神经症状时就可发现此环,位于角膜与巩膜的内表面上,呈绿褐色或金褐色,宽约1.3mm)。
考虑肝豆状核变性可能性大。这与患者曾经在北京××医院诊断的特发性震颤是否有联系?进一步检查头颅MRI(图4):脑内散在慢性缺血灶,双侧侧脑室旁、脑干异常信号,胼胝体压部异常信号。脑电图及脑地形图:正常。神经科会诊:肝豆状核变性。
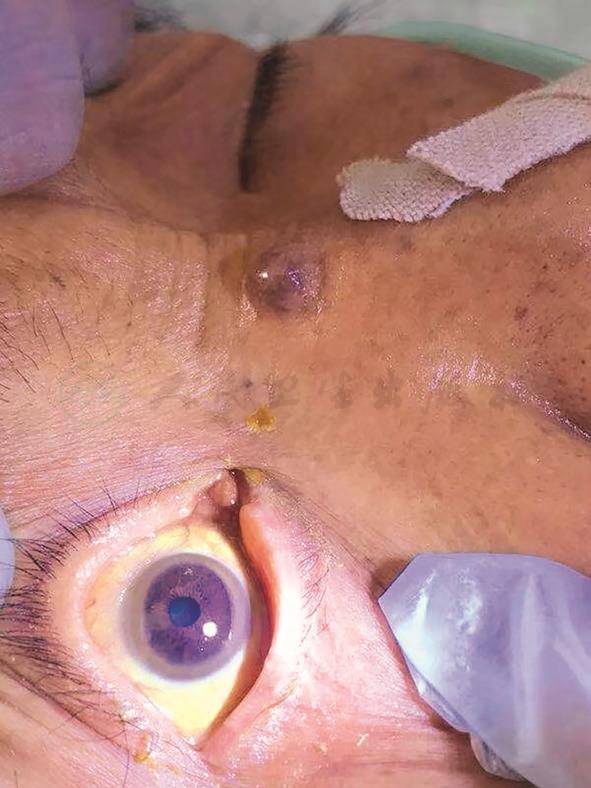
图3 眼科会诊
该患者需要进一步确诊遗传代谢性肝病——肝豆状核变性,故进一步完善相关检查。24h尿铜:63.6μg/24h。基因检测:受检者携带ATP7B两个位置杂合致病性变异阳性。因此,可排除另外一个遗传代谢性肝病——血色病。
5.最终诊疗思维过程
(1)诊断思路
对于该患者,通过病史及入院后常规化验检查,结合腹部CT,肝脏弹性检测,胃镜等检查,诊断肝硬化失代偿期明确,但肝硬化仍原因不明,最终通过肝穿刺、血清铜蓝蛋白、眼科K-F环、24h尿铜及基因检测确诊肝硬化原因为肝豆状核变性,肝硬化失代偿期,脾大,脾功能亢进,排除原发性肝癌。
(2)鉴别诊断
非酒精性脂肪性肝病是一种胰岛素抵抗和遗传易感性密切相关的代谢性应激性肝病,不仅可以导致肝炎、肝硬化、肝癌甚至死亡,还与代谢综合征、2型糖尿病、动脉硬化性心血管疾病及结直肠肿瘤等高发密切相关,是一个排除性诊断,常规通过腹部超声检查或肝脏弹性超声诊断,病理为诊断该病的金标准,但需要与肝豆状核变性相鉴别。肝豆状核变性以脂肪肝的病理模式最常见,因此肝穿刺不易鉴别,需做基因检测明确。该患者为中老年女性,体形中等,BMI 23.7kg/m2,脂肪衰减227,不排除非酒精性脂肪性肝病,最终肝穿刺及基因检测明确排除了该病。
最终诊断:肝豆状核变性,肝硬化失代偿期,门静脉高压症,脾大、脾功能亢进。
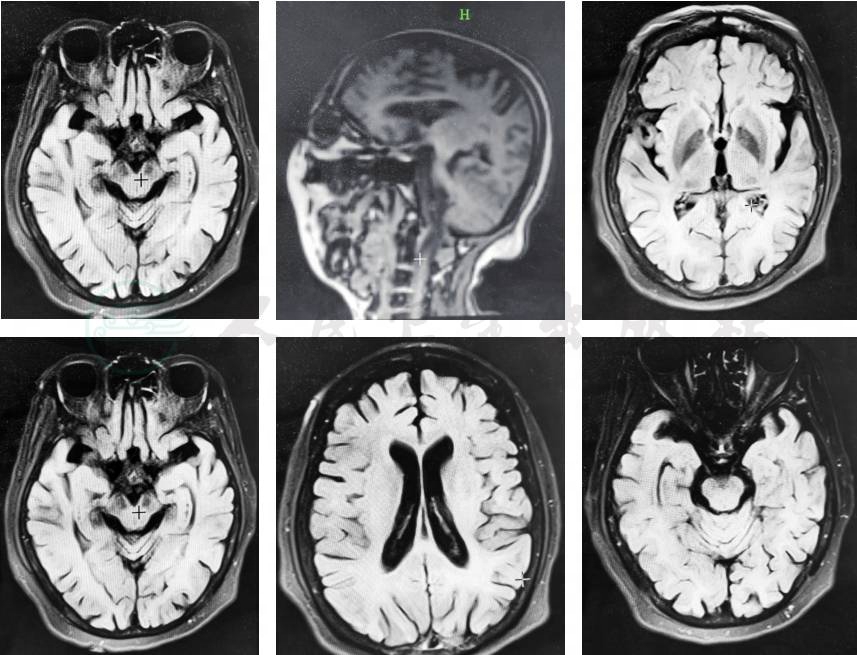
图4 头颅MRI
(3)治疗方案
对于肝豆状核变性患者,可给予低铜高蛋白饮食。首选青霉胺驱铜治疗,同时可给予补锌及曲恩汀药物等药物治疗。针对该患者,青霉素皮试(-),给予青霉胺250mg,2次/d,口服;同时针对胆汁淤积,给予熊去氧胆酸 13~15mg/(kg·d)(患者55kg,故口服 250mg,3次/d)。
6.后续随访
患者治疗1周后突发急性肝衰竭,经内科综合治疗和人工肝治疗无效死亡。
1.本例患者为中老年女性,否认有家族遗传病史,首发症状并不是肝脏疾病(肝功能一直无明显异常),而是突出的不自主的头部及双上肢震颤的神经系统症状,长期在神经科就诊,头颅MRI见非特异性改变,无典型熊猫脸样表现,在××医院神经科诊断特发性震颤,这是本病的诊断难点,导致长期误诊误治,错过了最佳治疗时间。故临床医师在遇到以不明原因震颤为首发症状的神经系统疾病时,要想到肝豆状核变性的可能性,以避免误诊误治。
2.遗传代谢性肝病的发病一般在儿童期(11.4岁),以持续肝功能异常等肝脏疾病为多见,神经系统表现的发生年龄也比较年轻,一般在青春期左右(18.9岁)。该患者为中老年女性,处于晚期发病年龄。临床上很少见晚期发病的遗传代谢性肝病,所以临床医师很难考虑到遗传代谢性肝病,容易漏诊。所以,临床医师一定要提高对遗传代谢性肝病的认识,尤其是晚期发病者不容忽视。同时,肝豆状核变性可以急性肝衰竭为首发表现,在临床上遇到不明原因的急性暴发性肝衰竭时,需要想到肝豆状核变性可能。
3.本例患者肝硬化原因不明。当肝硬化用常见肝病原因不能解释时,要考虑到遗传代谢性肝病,肝穿刺病理可起到举足轻重的作用。但是,肝豆状核变性和脂肪肝的病理模型很难鉴别,这是肝脏病理诊断肝豆状核变性的另一个难点。因此对于诊断困难的遗传代谢性肝病——基因病,最终还是需要基因检测这个金标准来确诊。
4.肝豆状核变性如果能早期诊断、早期规范地治疗,预后尚可。本例患者虽然最终明确了诊断,但为时已晚,已到了肝硬化失代偿期,肝移植可能是此时的最佳选择方案。遗憾的是,给予青霉胺治疗1周后,患者突发急性肝衰竭,经积极救治无效病故,没有进行肝移植的机会。此外,在肝豆状核变性的治疗方面,青霉胺的具体使用方案也是临床医师比较棘手的难点。
[1]张婷,彭韶,马莹莹,等.暴发性肝衰竭型肝豆状核变性2例报告并文献复习[J].临床儿科杂志,2016,34(11):825-828.
[2]MOHR I,WEISS KH.Biochemical markers for the diagnosis and monitoring of Wilson disease[J].Clin Biochem Rev,2019,40(2):59-77.













