(一)病例信息
【病史】
女性患者,46岁,有饲鸽史,主因反复声音嘶哑8年,加重2个月入院。患者8年前受凉后出现声音嘶哑,伴阵发性干咳,无咳痰及痰中带血,无气促、胸痛,每遇冬春季节变化、疲劳、言语增多时上述症状加重,严重时无法发声。患者曾于当地医院就诊,行电子喉镜检查示急性喉炎,输液治疗后症状好转。2个月前,患者再次出现声音嘶哑,且较前明显加重,输液治疗效果较差,遂就诊于我院。患者在门诊行电子喉镜检查,提示双侧声道充血肿胀,前中部分有白膜附着,气管黏膜糜烂,结节样隆起,诊断为声带炎、气道内膜肿物。胸部CT示气管管壁钙化、毛糙。门诊医师以“气道内肿物待查”将患者收住入院。患者自发病以来无皮疹、关节肿痛,无口腔溃疡及口眼干燥,体重无明显改变。
既往有子宫平滑肌瘤病史,已行子宫全切手术治疗;无烟酒等不良嗜好。
【体格检查】
体温36.8℃,呼吸19次/分,心率55次/分,血压117/68mmHg,SpO2 99%。神志清,精神可,全身浅表淋巴结未触及肿大。胸廓对称,双侧呼吸动度均等,双肺叩诊清音,听诊双肺呼吸音粗,未闻明显干、湿啰音及胸膜摩擦音。腹部无明显异常,双下肢不肿。
【影像学检查】
胸部CT肺窗示多发不规则结节突向管腔,纵隔窗可见气管、支气管管壁不规则增厚及广泛钙化影,管腔轻度狭窄(图1)。
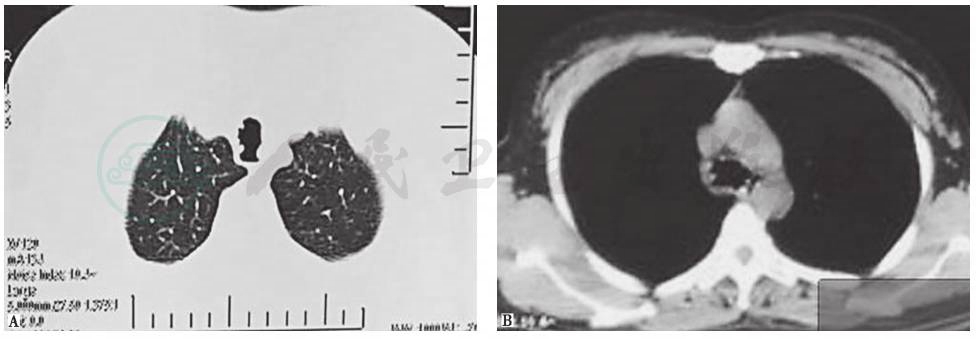
图1 胸部CT表现
引自:主编:.呼吸系统疑难病例诊疗辨析.第1版.ISBN:978-7-117-26415-0
(二)临床思辨
【临床特点】
1.患者为中年女性,呈慢性病程(8年),病情反复。
2.临床表现为反复声音嘶哑8年,对症治疗后可缓解,但易反复,无反复发热等伴随症状,近2个月病情加重。
3.患者曾在当地医院行电子喉镜检查,提示急性喉炎。此次发病,患者来我院诊治,电子喉镜检查提示双侧声道充血肿胀,前中部分有白膜附着,气管黏膜糜烂,有结节样隆起。
4.胸部CT肺窗示气管、支气管内多发不规则结节突向管腔,纵隔窗可见气管、支气管管壁不规则增厚及广泛钙化影,管腔轻度狭窄。
【思辨要点】
根据上述临床特点,对于本病例,诊断上主要定位在大气道疾病。常见可引起弥漫性大气道壁增厚的疾病有支气管结核、气道淀粉样变、复发性多软骨炎、肿瘤性疾病、骨化性气管支气管病等。
气管、支气管结核:单纯性支气管结核是气管-支气管黏膜或黏膜下层发生的结核病变,无肺部结核病灶。其临床表现无特异性,可表现为咳嗽、咳痰、咯血、胸痛、呼吸困难,部分患者伴有低热、盗汗等结核中毒症状。查体可闻干、湿啰音。胸部CT检查常可见管腔狭窄,内壁光滑或呈波浪状改变,后期管壁僵硬伴或不伴点状或条索状钙化,可伴肺结核和肺门淋巴结肿大表现。支气管镜检查早期可见黏膜慢性炎,晚期则可见黏膜溃疡或干酪样坏死、肉芽增殖和瘢痕狭窄。规律抗结核治疗有效。痰病原学、支气管镜等检查有助于明确诊断。
气管淀粉样变:临床表现为进行性气促、喘息、咯血或阻塞性肺炎,常以异常轻链克隆呈淀粉样在气管-支气管黏膜下层异常沉积,病理表现为气管、支气管黏膜组织刚果红染色阳性且偏振光显微镜下可见黄绿双色折光的嗜伊红物质。支气管镜检查可见气管、支气管黏膜局限或弥漫性鹅卵石样斑块或结节突向管腔,常累及气管膜部。对反复咳嗽、咳痰,影像学表现为气管壁不规则增厚者,需要考虑该病可能,可进行支气管镜检查以明确诊断。
复发性多软骨炎:是一种较少见的炎性破坏性疾病,其特点是软骨组织复发性退化性炎症,表现为眼、耳、鼻、喉、气管、关节、心脏瓣膜等器官组织受累。喉、气管及支气管软骨受累,表现为声音嘶哑、刺激性咳嗽、呼吸困难和吸气性喘鸣。CT检查显示气管管壁弥漫性增厚伴管腔狭窄,软骨区钙化。临床表现除呼吸道症状外,常伴有鼻及耳郭软骨慢性炎症、内耳功能受损等,糖皮质激素或糖皮质激素联合免疫抑制剂能有效改善病情。本例患者胸部影像学检查未见气管等大气道壁软骨破坏伴气道壁软组织弥漫炎性增厚,临床上未见鼻、耳等部位软骨组织损伤表现,也无气道塌陷所致呼吸困难,因此,可排除复发性多软骨炎。
肿瘤性疾病:本病例气管、主支气管黏膜表面病灶弥漫、病程漫长,未见病灶侵袭性生长等病理表现,故可排除肿瘤性疾病。
骨化性气管支气管病(TO):是一种罕见的气管内膜良性病变,主要以气管和支气管黏膜下多发骨化和软骨组织结节状增生为特征,通常引起气道狭窄。TO多见于50岁以上的中老年人,极少见于青年人和儿童。TO准确的发病率尚不清楚。TO通常无特征性临床表现,多数病例是在死后尸检时确诊的,少部分患者因气道狭窄致气管插管困难而发现。本例患者反复声音嘶哑8年、加重2个月,电子喉镜检查发现双侧声道充血肿胀,气管黏膜糜烂,结节样隆起,考虑为TO可能性大。
综上所述,本病例为TO可能性大,但尚不能排除气道淀粉样变、支气管结核,下一步完善各种呼吸道病原学(包括多种细菌、真菌、结核分枝杆菌)检查以及血清蛋白电泳、免疫电泳、轻链定量检测、抗核抗体谱检测、抗中性粒细胞胞质抗体(ANCA)检测、T淋巴细胞刺激γ-干扰素释放试验(T-SPOT)、尿轻链定量检测等多项检查,并完善术前准备,尽早实施支气管镜及组织病理活检确诊。
(一)临床信息
【辅助检查】
血常规、尿常规、凝血功能指标、肿瘤标志物、抗酸杆菌涂片、结核抗体、呼吸道多病毒检查均未见异常,降钙素原(PCT)0.09ng/ml,血沉3mm/1h,CRP<0.5mg/L,血生化(肝、肾功能等)检查正常。
肺功能检查提示阻塞性通气功能障碍。
胸部CT:气管、支气管不同程度狭窄,管壁钙化、毛糙;右肺下叶炎性病变,黏膜下环形高密度骨化斑块。
支气管镜检查:镜下见自声门至隆嵴及左右主支气管前壁及侧壁有白色结节状物,呈钟乳石样改变,突入管腔,质地较硬(图2)。支气管黏膜活检病理示气管、支气管黏膜组织慢性炎症,并见少许骨组织(图3)。
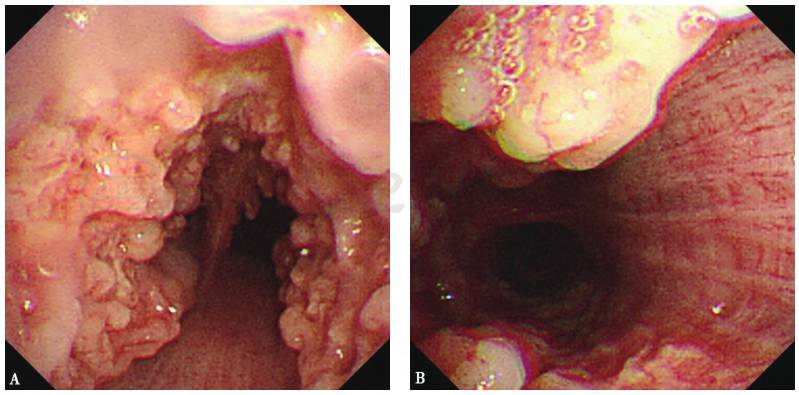
图2 支气管镜检查镜下表现
镜下见气管前壁和侧壁密布大小不等的结节,质硬,部分气管内有坏死物覆盖,致管腔明显狭窄,气管膜部病变不明显
引自:主编:.呼吸系统疑难病例诊疗辨析.第1版.ISBN:978-7-117-26415-0
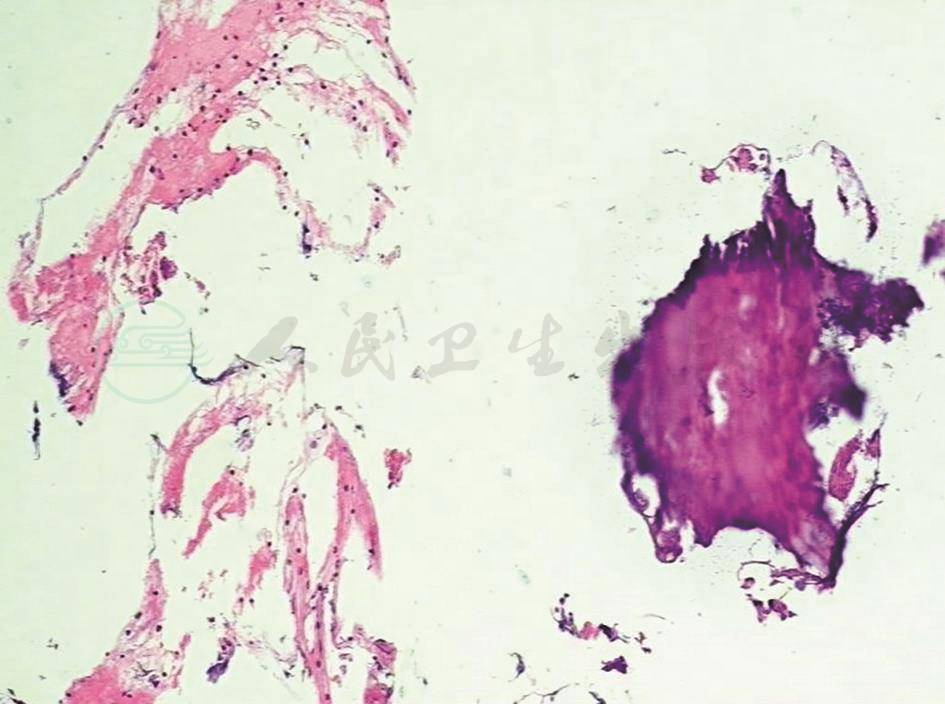
图3 支气管黏膜活检结果
显微镜下见支气管黏膜下钙化灶(HE染色,100×)
引自:主编:.呼吸系统疑难病例诊疗辨析.第1版.ISBN:978-7-117-26415-0
最后诊断:骨化性气管支气管病。
经布地奈德、异丙托溴铵等雾化吸入,辅以祛痰等对症治疗,患者症状明显减轻。出院后,患者长期规律吸入布地奈德福莫特罗,门诊随诊时复查胸部CT显示较前无显著改变。目前,患者病情相对平稳,间断有少量咳嗽,对症治疗能缓解症状。
(二)临床思辨
TO在大气道内的结节病灶较小,普通X线检查一般难以发现,CT对发现气道壁钙化影较敏感,是TO重要的非侵入性诊断手段,尤其1mm以下薄层CT扫描,能发现突入气管内结节的钙化及黏膜下的钙化斑,甚至无钙化的结节。TO典型的CT表现为气管、主支气管及叶支气管黏膜下多发钙化结节突向管腔,以前壁及侧壁受累多见,气管膜部极少累及。
TO可通过支气管镜检查确诊。支气管镜下可见:小气道前壁及侧壁灰白色的疣状结节突向管腔,结节质地较硬,散在分布或相互融合;气道可部分累及甚至全程累及;极少数患者的外周气管黏膜下可见块状病灶,容易堵塞管腔导致肺不张。病理检查可见气管黏膜上皮鳞状化生、软骨、骨组织、钙化及造血骨髓形成。
TO患者临床表现较轻,肺功能检查不敏感。重度受累者可表现为阻塞性通气功能障碍,流速-容积曲线环可出现吸气相及呼气相曲线改变。本例患者肺功能检查示中度阻塞性通气功能障碍。
TO是一种慢性良性病变,主要是针对气道炎症行抗炎等对症治疗。如果患者出现呼吸困难或气喘,吸入支气管舒张剂和激素(丙酸倍氯米松或布地奈德)可有效缓解症状。长期吸入支气管扩张剂和糖皮质激素,可改善临床预后。少数气道严重狭窄或反复发生阻塞性肺炎的患者需采用放疗、激光气化、外科手术等方法清除病灶。其中,经支气管镜激光气化治疗是目前疗效最确切的方法,但这些治疗的长期疗效尚有待评价。
本例患者起病隐匿,呈慢性病程,病情反复,主要表现为反复咳嗽、咳痰、呼吸困难,无明显发热、咯血,胸部CT提示为气管、支气管壁不规则增厚,伴有多发钙化,需与支气管结核、气道淀粉样变、复发性多软骨炎等疾病相鉴别。骨化性气管支气管病漏诊率高,诊断周期较长,对于长期慢性咳嗽患者,尤其是胸部CT表现为气管、支气管壁增厚伴有钙化者,应提高警惕,及早行支气管镜检查以明确诊断。
(姜淑娟)
1.Rokitansky K,Cited By,Dalgarred JB.Tracheobronchopathia osteochondroplastica.Acta Pathol Microbiol Scand,1947,24:118.
2.Wilks S.Ossific deposits in the larynx,trachea and bronchi.Trans Pathol Soc Lond,1857,8:88.
3.Muller UM,Gielen S,Schuler GC,et al.Endocardial calcification of left atrium,tracheobronchopathia osteoplastica,and calcified aortic arch in a patient with dyspnea.Circ Heart Fail,2008,1(4):290-292.
4.Vidal A,Lluberas N,Florio L,et al.Massive left atrial calcification,tracheobronchopathia osteoplastica and mitral paravalvular leak associated with cardiac rheumatic disease and previous mitral valve replacement.Int J Cardiol,2013,167(5):e111-e112.
5.Muller UM,Gielen S,Schuler GC,et al.Endocardial calcification of left atrium,tracheobronchopathia osteoplastica,and calcified aortic arch in a patient with dyspnea.Circ Heart Fail,2008,1(4):290-292.
6.Danckers M,Raad RA,Zamuco R,et al.A complication of tracheobronchopathia osteochondroplastica presenting as acute hypercapnic respiratory failure.Am J Case Rep,2015,16:45-49.
7.Baran A,Güngör S,Unver E,et al.Tracheobronchopathia osteochondroplastica :a case report.Tuberk Toraks,2004,52(2):183-185.
8.Jabbardarjani H,Radpey BS,Masjedi M,et al.Tracheobronchopathia osteochondroplastica:presentation of ten cases and review of the literature.Lung,2008,186(5): 293-297.
9.Karan Madan,Loganathan Nattusamy,Sudheer Arava,et al,Tracheobronchopathia osteochondroplastica :a rare cause of difficult intubation.Indian J Chest Dis Allied Sci,2014,56(3):187-189.
10.Gökhan Kırbaş,Canan Eren Dağlı,bdullah Çetin Tanrıkulu,et al.Unusual combination of tracheobronchopathia osteochondroplastica and AA amyloidosis.Yonsei Med J,2009,50(5):721-724.













