(一)病例信息
【病史】
女性患者,62岁,6个月前无诱因出现活动后喘憋,偶有咳嗽,咳少量白色泡沫痰,无发热、胸闷、胸痛,无心悸、气短,无夜间憋醒,休息1~2分钟好转,未进行正规治疗;4个月前活动后喘憋加重,活动耐量下降,当地医院胸部CT示间质性肺炎,口服泼尼松(30mg,每天1次)后病情好转不明显;2个月前无诱因出现双侧下胸侧部胀痛,与呼吸运动无关,咳嗽频繁,偶咳少许白色泡沫痰,于外院门诊采取激素加量治疗(甲泼尼龙80mg,每天1次),3天后喘憋及活动耐量明显改善,遂予口服泼尼松(60mg,每天1次)、环磷酰胺(100mg,每天1次)治疗,1个月前因出现严重脱发,头皮皮疹加重,考虑为药品不良反应,遂停用环磷酰胺,口服激素逐渐减量;1周前泼尼松减至35mg,每天1次时,再次出现上述胸痛症状,以左侧为著,进一步诊治住院。患者自发病以来,无发热、咯血,无心悸、气短,无双下肢水肿,无口干、眼干、光过敏、牙齿脱落、关节痛等,食欲差,睡眠、精神可,尿、便无异常,近6个月体重下降10kg。
患者13年前因输卵管畸胎瘤行一侧附件肿物切除术;4个多月前出现发际处头皮发红,轻度瘙痒,未重视;3个月前头顶出现红色斑块、结节,无瘙痒及疼痛;2个月前使用环磷酰胺(cyclophosphamide,CTX)后,皮疹明显加重,逐渐出现弥漫性脱发,缓慢增大至前额;1个月前出现皮肤瘙痒,外院诊断为过敏性皮炎,予依巴斯汀片及复方甘草酸苷治疗,无好转。患者长期从事财会工作,无其他特殊病史。
【体格检查】
体温36.6℃,心率103次/分,呼吸24次/分,血压130/80mmHg。头顶见弥漫性脱发,前额至枕部见弥漫性红色斑块、结节,以头顶部为著,高出皮面,皮温不高,质较硬,有少许鳞屑,无破溃、结痂、萎缩、瘢痕等。全身浅表淋巴结未触及肿大。双肺呼吸音粗,双下肺呼吸音弱,双下肺可闻Velcro啰音。心律齐,各瓣膜听诊区未闻病理性杂音。下腹正中可见一长约5cm纵行陈旧性手术瘢痕。腹软、无压痛,肝、脾肋下未触及,无移动性浊音。双下肢无水肿。无杵状指(趾)。
【实验室检查】
血气分析(面罩吸氧10L/min):pH 7.49,PaCO2 33mmHg,PaO2 82mmHg,HCO3- 25.1mmol/l,SaO2 97%。
血常规:WBC 12.34×109/L,N% 88.8%,Hb 144g/L,PLT 247×109/L。
肝肾功能、电解质、弥散性血管内凝血(DIC)相关检查(凝血酶原时间、凝血酶原活动度、INR、纤维蛋白原、纤维蛋白降解产物、D-二聚体、活化部分凝血酶原时间)、心肌酶均未见明显异常。
支气管肺泡灌洗液:回收量65ml,有核细胞总数3.77×106/L,吞噬细胞百分比89%,中性粒细胞百分比1%,淋巴细胞百分比10%。其中,T细胞亚群:CD3 90.46%,CD4 48.9%,CD8 38.8%,CD4/CD8比值1.3。
支气管分泌物结核分枝杆菌、非结核分枝杆菌复合群DNA阴性。
【影像学检查】
胸部CT:双肺弥漫间质性病变伴多发小结节(图1)。2个月后,随着病程延长,原有结节样病灶增多,病灶融合,形成磨玻璃及实变影,并出现双侧胸腔积液和少量心包积液(图2)。
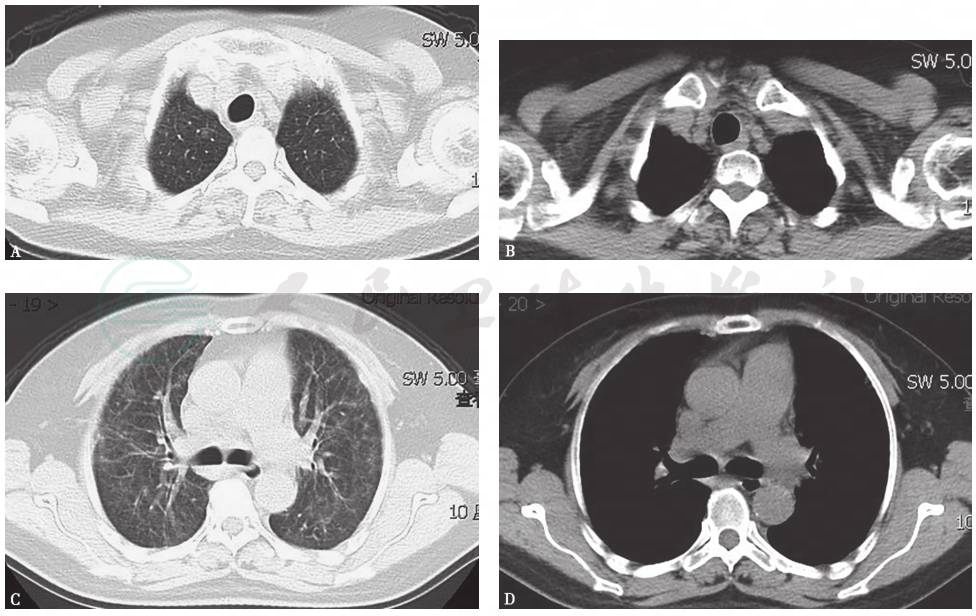
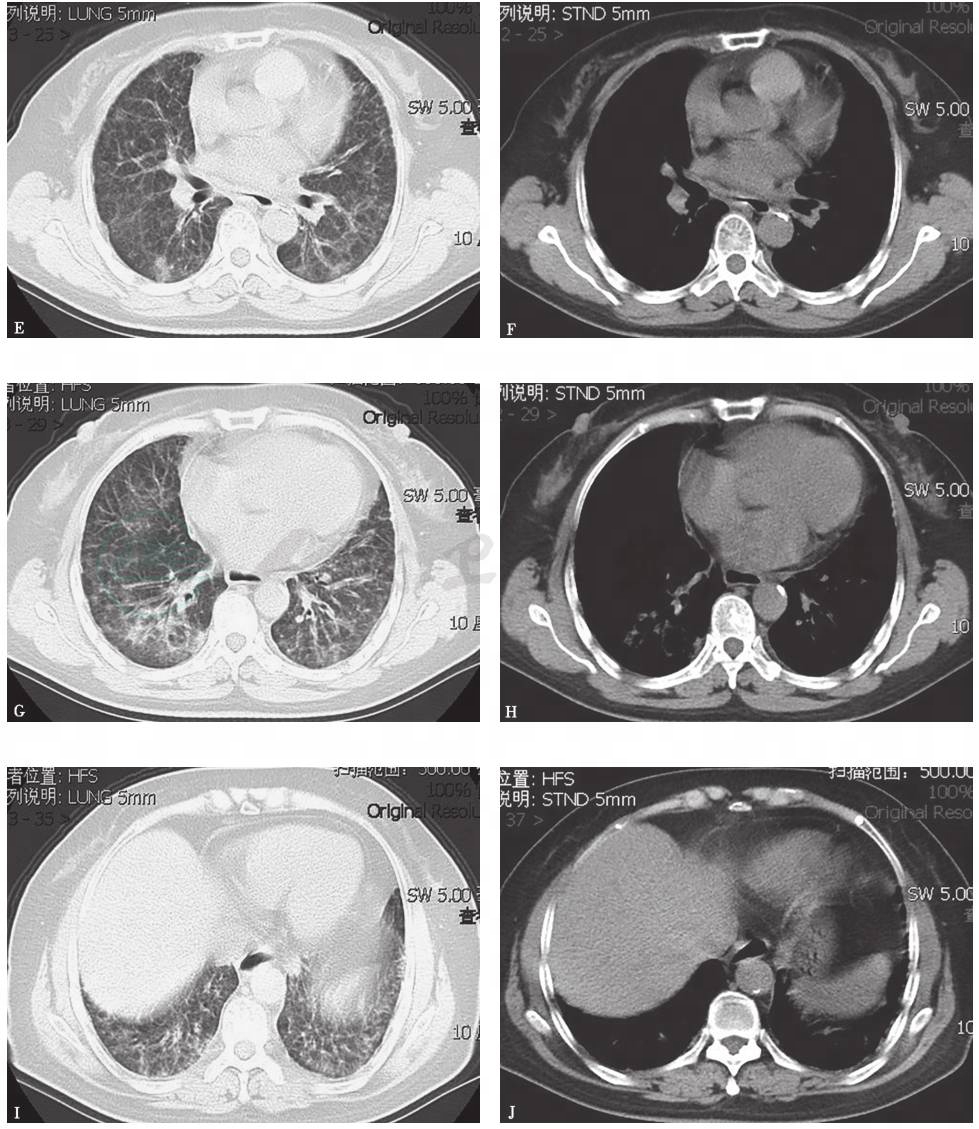
图1 胸部CT表现(2014-03-05)
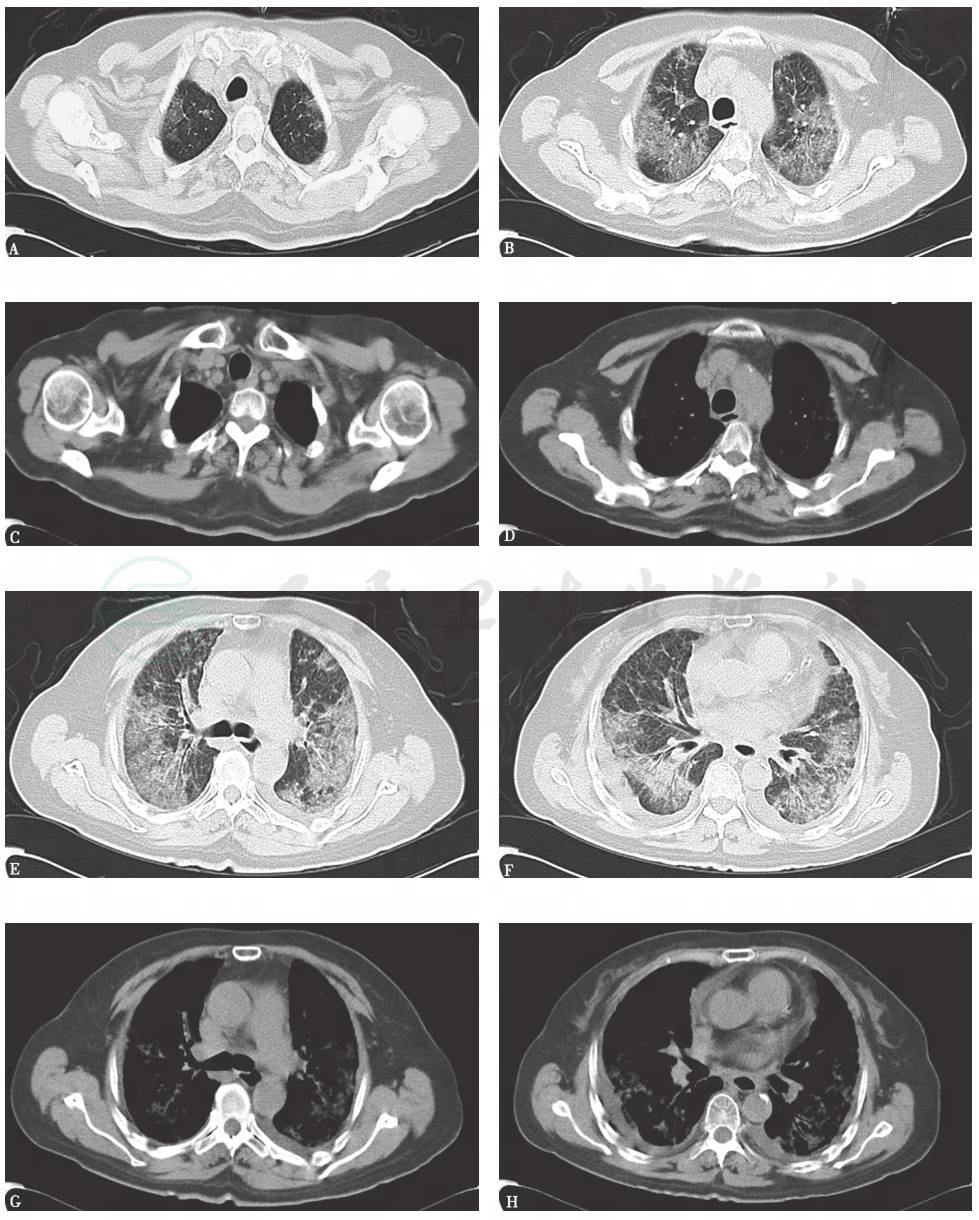
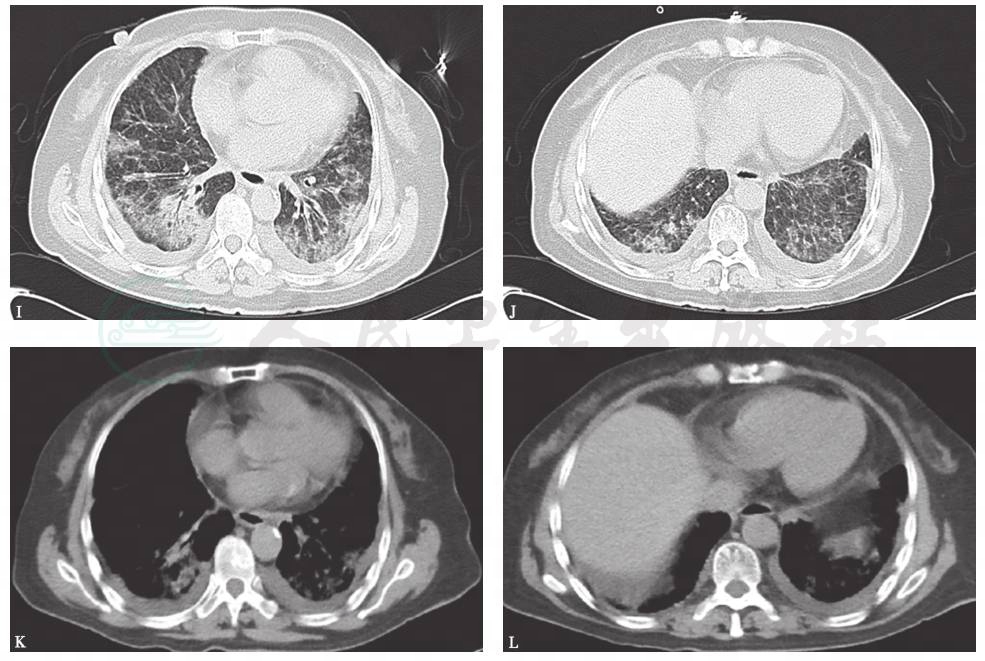
图2 胸部CT表现(2014-05-22)
(二)临床思辨
【临床特点】
1.患者为老年女性,病程呈慢性(已半年),持续进展。
2.主要症状和体征为活动后喘憋、咳嗽、少许白色黏液泡沫痰。
3.血气分析提示Ⅰ型呼吸衰竭,白细胞轻度增高。
4.胸部影像学表现由双肺弥漫性磨玻璃影并多发小结节样改变,逐渐进展至大片磨玻璃影、局部实变结节并双侧胸腔积液。
5.应用激素后,患者临床症状有所好转,但影像学表现持续进展。
【思辨要点】
肺间质病的常见临床症状是咳嗽、渐进性呼吸困难,查体可闻Velcro音,胸部影像学表现为弥漫性间质肺病,晚期患者动脉血气分析可表现为Ⅰ型呼吸衰竭。
1.哪些疾病可导致双肺弥漫性间质性病变?
弥漫性间质性肺疾病常被分为:①继发性间质性肺疾病,如继发于结缔组织疾病、感染、药物损伤、肿瘤、职业性因素等;②原发性间质性疾病,如结节病、肺泡蛋白沉积症、肺朗格汉斯细胞组织细胞增多症、肺淋巴管平滑肌瘤病、慢性嗜酸性粒细胞性肺炎(chronic eosinophilic pneumonia,CEP)、特发性肺含铁血黄素沉着症等;③特发性间质性肺炎。其中,特发性间质性肺炎又被分为3大类:①主要特发性间质性肺炎,包括特发性肺纤维化(IPF)、特发性非特异性间质性肺炎(idiopathic nonspecific interstitial pneumonia,INSIP)、呼吸性细支气管炎伴间质性肺疾病(RB-ILD)、脱屑性间质性肺炎(DIP)、隐源性机化性肺炎(COP)和急性间质性肺炎(AIP);②少见特发性间质性肺炎,包括特发性淋巴细胞性间质性肺炎(idiopathic lymphoid interstitial pneumonia,ILIP)和特发性胸膜肺弹力纤维增生症(idiopathic pleuroparenchymal fibroelastosis,IPPFE);③不能分类的特发性间质性肺炎,如急性纤维素性机化性肺炎(AFOP)等。
诊断特发性肺间质病必须首先充分评估并排除其他可导致弥漫性间质性肺疾病的原因。
2.目前获得的本病例的临床信息中是否存在继发性弥漫性间质性肺疾病的诊断线索?
临床上,提示继发性间质性肺病的线索可能非常隐匿,常不被患者及其家属注意,但可能成为确诊的关键因素。这些线索主要包括以下几方面:
(1)病史
包括既往患病情况以及环境、职业接触或吸入史、药物应用史、家族史等。
(2)症状、体征
患者可无自觉症状,也可出现不同程度的活动后呼吸困难、干咳、发绀、肺部Velcro音、杵状指等特征。如果并发皮肤、关节、神经、肌肉、五官症状或体征,应警惕继发性肺间质病。
(3)辅助检查
如果有ANA、ANCA、环瓜氨酸肽(cyclic citrullinated peptide,CCP)、IgG4等免疫学指标异常,或心、肝、肾、血液等系统受累,应警惕继发性弥漫性间质性肺疾病的可能。
(4)治疗反应
如果抗感染治疗或利尿治疗等效果显著,应考虑感染、心力衰竭等因素继发的肺间质病变。
本例患者有呼吸困难、咳嗽、少痰,逐渐进展至Ⅰ型呼吸衰竭,同时伴发头部皮疹,应用抗过敏药物效果不佳,有明显食欲缺乏、消瘦、胸痛症状,故应谨慎排查继发性肺间质病变。
(一)临床信息
【实验室检查】
尿常规、便常规、肝功能、肾功能、电解质、血脂、凝血功能、乙肝病毒、丙肝病毒、梅毒螺旋体和HIV检测均未见异常;HbA1c 6.7%;ESR 40mm/1h;PCT未见异常。
多次血巨细胞病毒、EB病毒、腺病毒PCR阴性;痰培养见鲍曼不动杆菌;痰真菌涂片可见孢子,培养示热带念珠菌;痰抗酸及结核PCR均阴性。
重新检查支气管肺泡灌洗液T细胞亚群:CD3 76%、CD4 23.7%、CD8 43.6%、CD4/CD8 0.54。
各种免疫球蛋白和自身免疫抗体未见异常。
肿瘤标志物:CA125(273.10U/ml)、CA19-9(77.26U/ml)、CEA(19.15ng/ml)、CYFRA21-1(7.57ng/ml)均增高;CA15-3、AFP、NSE未见异常。
【支气管镜检查】
对患者行床旁支气管镜检查,未见异常。于右下叶基底段行支气管肺泡灌洗,BALF外观呈洗肉水样,细胞总数0.21×106/ml(其中,巨噬细胞68%,淋巴细胞28%,中性粒细胞4%)。支气管分泌物及BALF细菌、真菌涂片及培养均阴性,抗酸染色阴性;肺孢子菌PCR、镜检均阴性。BALF病理检查见血性背景中有多量退变的肺泡上皮细胞、吞噬细胞及淋巴细胞,少量中性粒细胞,小团脱落的上皮样细胞可能源于支气管黏膜(图3)。
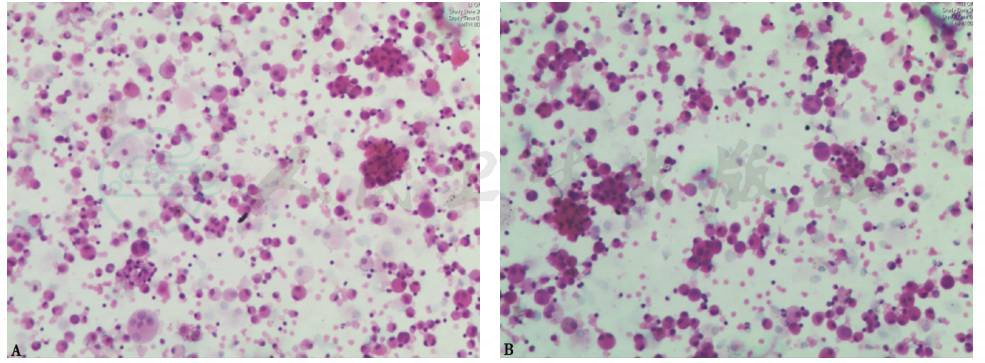
图3 BALF病理表现(瑞氏染色,200×)
【影像学检查】
胸部X线检查可见双肺弥漫高密度影,双侧少量胸腔积液(图4),1个月后病灶进一步增多、加重(图5)。胸部CT显示病灶进一步融合增多,伴双侧胸腔积液和心包积液(图6)。
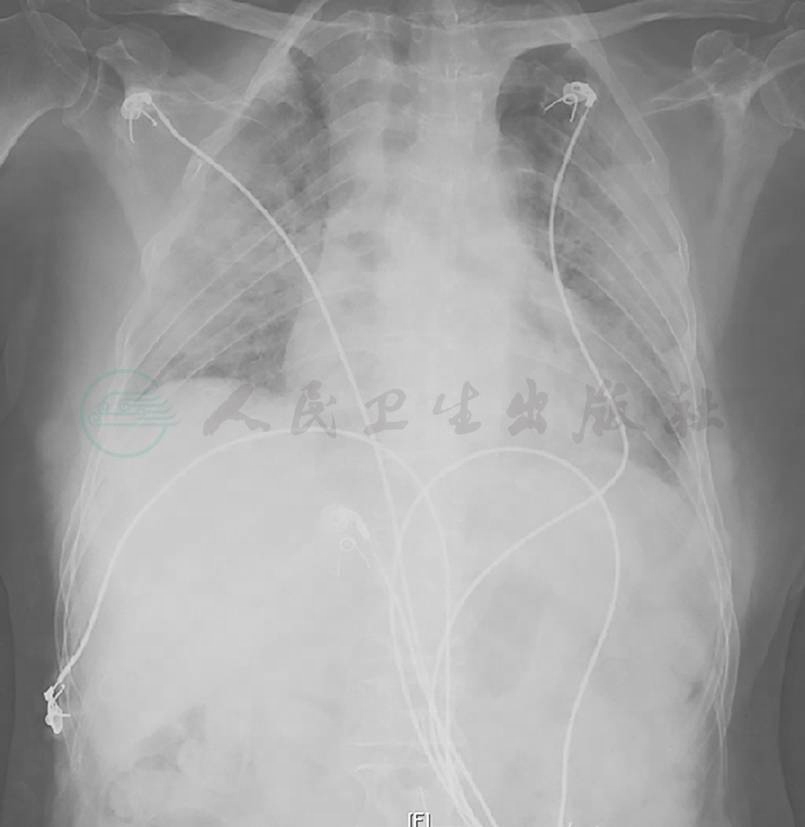
图4 胸部X线表现(2015-05-23)
胸部X线片可见双肺多发斑片影,双侧肋膈角显示不清,变钝
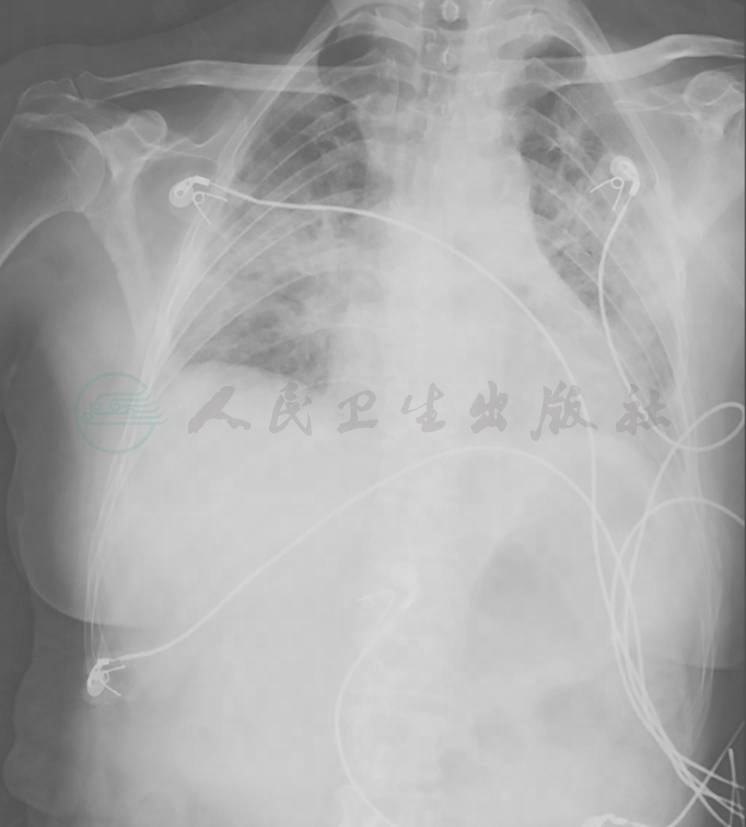
图5 胸部X线表现(2015-06-23)
胸部X线片可见双肺多发斑片影较前略加重,双肋膈角变钝
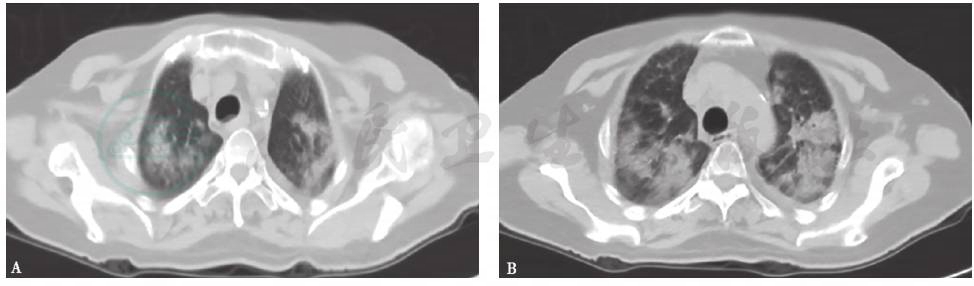
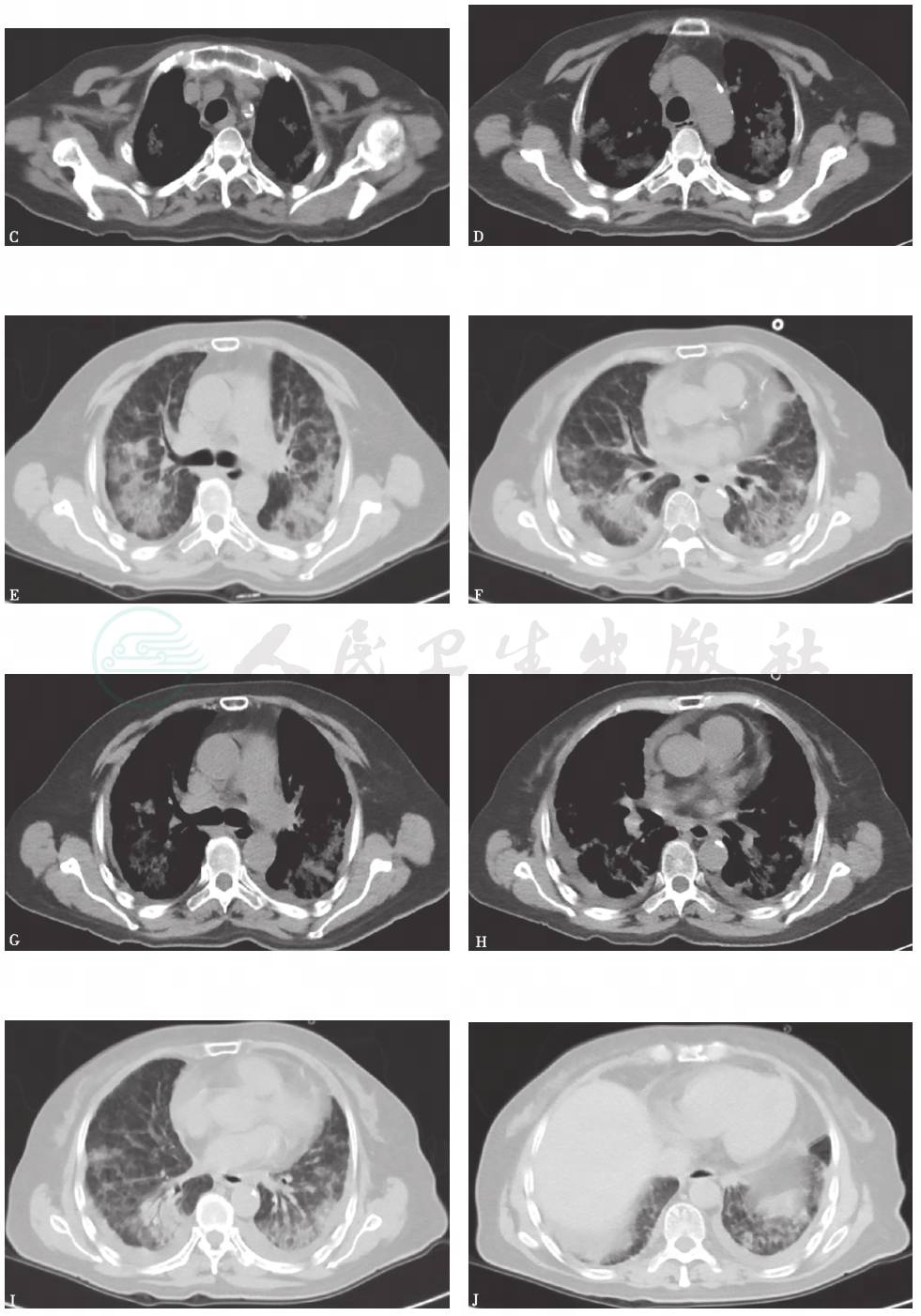
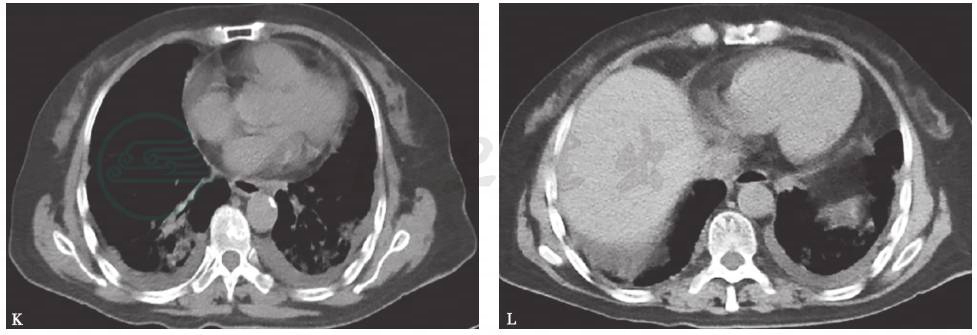
图6 胸部CT表现(2015-06-03)
胸部CT可见双肺多发斑片影、结节影,双侧少量胸腔积液,少许心包积液
【治疗过程】
在排除感染因素后,予患者糖皮质激素加量治疗(甲泼尼龙40mg,每天1次),并试用甲泼尼龙500mg冲击治疗3天,患者氧合情况一度明显改善,吸氧条件由面罩10~12L/min降至4L/min,氧合指数由100mmHg升至400mmHg以上,但继发出现较多白色泡沫痰情况。
(二)临床思辨
患者入院后所做系列检查显示:①血沉增快,PCT正常,不典型病原体及巨细胞病毒、肺孢子菌、结核分枝杆菌等病原学检测均阴性,结合发病半年来无发热,两次支气管镜检查镜下未见感染相关征象,由感染性疾病导致弥漫性肺间质病可能较小;②自身抗体均阴性,头部皮肤表现并非典型免疫病相关皮疹形态,结合其他临床表现,考虑为风湿免疫病可能小;③无明确有机、无机粉尘或化学物质吸入史,无特殊药物应用史,仅发病后开始应用激素、环磷酰胺,故考虑药物或环境因素致病可能性小; ④综合分析病史及胸部影像学表现,考虑可基本排除心功能不全、其他肉芽肿性间质性病变及其他少见肺间质病;⑤肿瘤导致的肺部间质性病变通常表现为多发转移瘤所致的结节性改变或以小叶间隔增宽为主的淋巴管癌病,仅肺泡细胞癌表现为双肺多发性腺泡结节样阴影或淡片状影,病变范围扩大时可以融合成片,类似于肺实变,可以见到支气管充气征,可以合并胸腔积液、心包积液等征象,可伴有多项肿瘤标志物水平升高,故本病例目前尚不能完全排除肿瘤性疾病;⑥经全身糖皮质激素治疗,患者临床症状一过性缓解。
此时需要思考以下问题:
1.如何考虑患者对激素治疗的反应?
本例患者的支气管肺泡灌洗液细胞计数以淋巴细胞为主,应用激素后症状一度短暂好转(不排除肿瘤性肺间质病对激素有一过性反应),但激素稍减量,病情即反复并加重,整体病情呈持续性进展,影像学表现亦可见肺部病变持续进展,无好转征象,故激素治疗效果不佳。
2.本病例出现的肺部表现如果疑似肿瘤所致,在呼吸衰竭状态下,可以进行何种检查?
(1)支气管肺泡灌洗、经皮或经支气管肺穿等手段可以协助明确肺部病变性质,但本例患者两次支气管镜检查均未得到明确肿瘤证据,患者处于呼吸衰竭状态,行肺部有创检查风险大。
(2)患者头部皮肤有异常皮疹(不能用药疹或免疫病相关皮疹解释),易进行活检,可能会提供有意义的鉴别诊断线索。
(3)甲状腺B超,胸、腹、盆腔CT或PET-CT可能会提供肿瘤原发或转移病灶的证据,可作为备选无创检查手段。
(一)临床信息
1.小块皮肤(后颈)组织活检病理结果
真皮内散在异型细胞,可见胞质内黏液(图7A);免疫组化染色:CK、EMA、Ki-67(50%)、p53阳性,CD68、Vimentin、Melan-A阴性;特殊染色:AB-PAS阳性(图7B)。病理表现符合印戒细胞癌转移表现,来源于胃癌等相关脏器肿瘤可能性大。
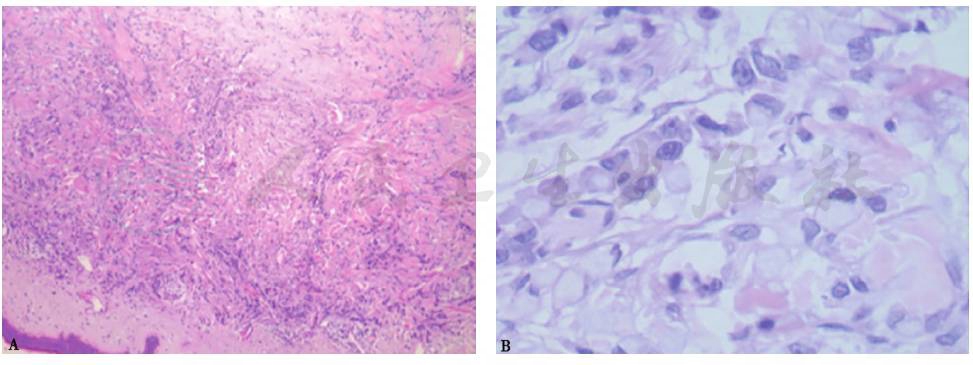
图7 颈部皮肤病理表现
A.HE染色,100×;B.AB-PAS染色,400×
2.胃镜检查
镜下见胃体上部大弯侧可见1枚直径约0.5cm的山田Ⅰ型息肉;窦体交界大弯侧可见2条黏膜皱襞,粗大僵硬,范围约4cm×2cm,表面黏膜粗糙、糜烂(图8)。胃镜下诊断:胃窦体交界皱襞粗大,胃息肉,慢性浅表性胃炎。活检组织幽门螺杆菌(helicobacter pylori,HP)阴性。
活检标本(窦体交界)病理表现:印戒细胞癌;免疫组化染色:CK、EMA、CD68、Ki-67均阳性;特殊染色:AB-PAS阳性(图9)。
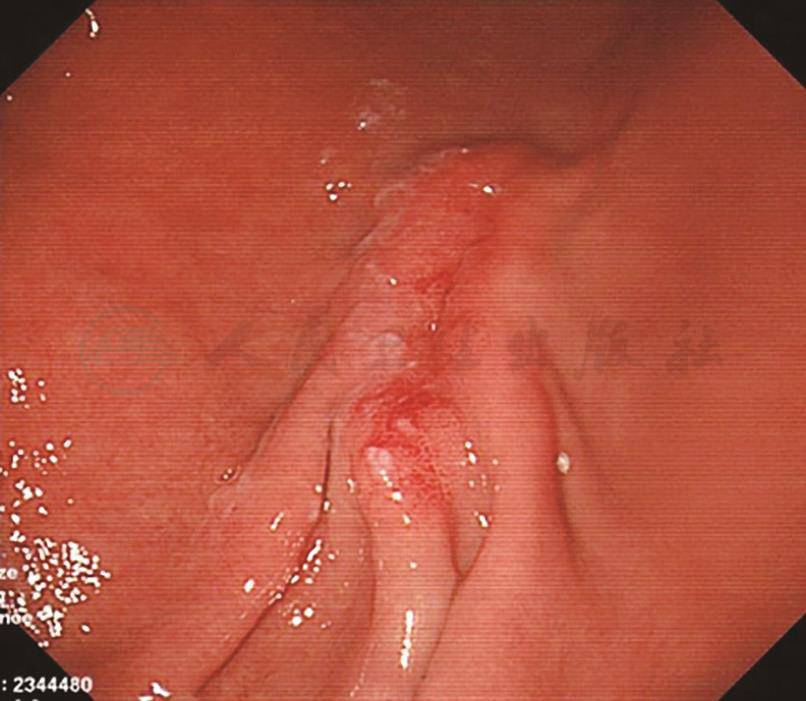
图8 胃镜检查镜下表现
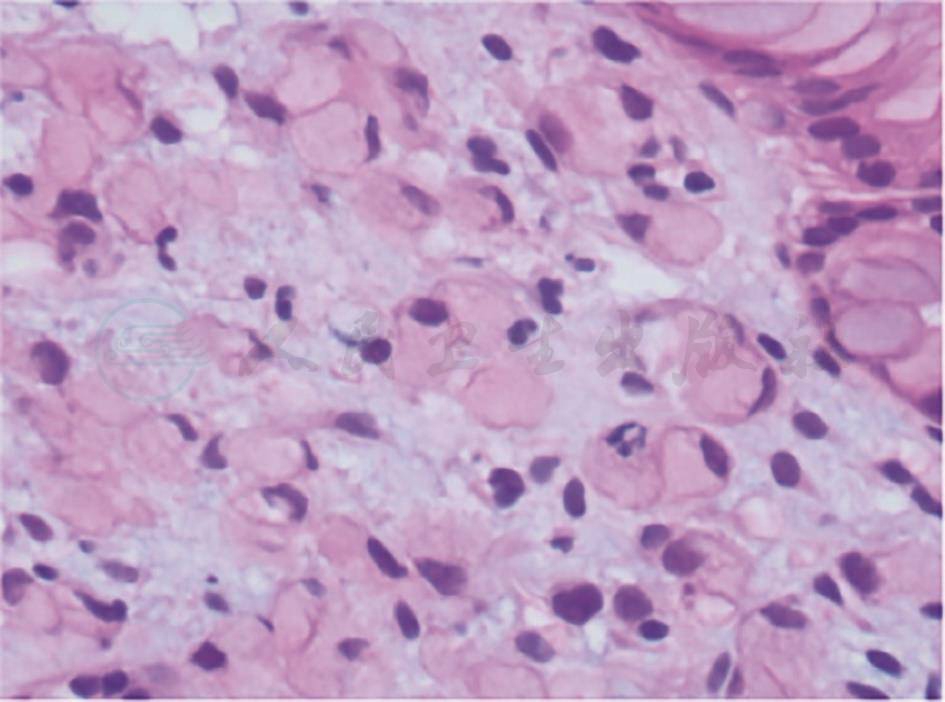
图9 活检标本(窦体交界)病理表现(AB-PAS染色,400×)
3.支气管肺泡灌洗液
再次阅片,发现BALF中有部分细胞形似印戒细胞(图10),但不能完全排除因制片过程中细胞变形所致的可能。
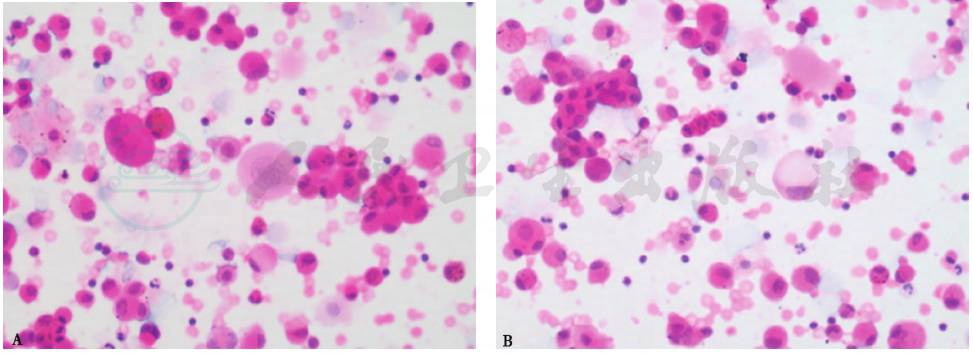
图10 支气管肺泡灌洗液病理表现(瑞氏染色,400×)
4.影像学检查
妇科彩超:子宫萎缩、充血,宫旁充血;左卵巢稍大(1.9cm×2.6cm×1.3cm),呈实性中等回声。
甲状腺B超:甲状腺轻度不均质改变,双侧颈部扁平状小淋巴结。
腹部CT:肝右叶被膜下点状钙化,未见其他异常;双肺间质性病变,双侧胸腔积液。
盆腔CT:附件肿物切除术后,膀胱右后壁增厚。
5.会诊讨论
患者虽然应用激素后短期症状有所缓解,但后期出现较多黏液泡沫痰,胸部影像学表现持续进展,由弥漫性磨玻璃影逐渐发展为实变影,并出现双侧胸腔积液,病程及影像学表现符合腺癌肺泡生长表现。故综合考虑,本病例肺部间质性表现为胃印戒细胞癌转移可能性大。
最后诊断:胃印戒细胞癌肺转移、头部皮肤转移。
(二)临床思辨
根据病理循证证据,考虑患者肺内病变为胃印戒细胞癌肺转移、头皮转移。
1.肿瘤标志物水平升高在肺间质病变疾病诊断中有何意义?
特发性肺间质病患者可出现肿瘤标志物升高,间质性肺病合并恶性肿瘤者可出现血CEA、CA125水平明显升高。故此指标可考虑作为肺间质病合并癌症的辅助诊断指标,可能对在间质病患者中筛查癌症或评估癌症风险有一定帮助。
2.本例患者肺内的病变到底是肺泡癌还是由胃印戒细胞癌转移至肺?
患者有短期咳大量泡沫白痰表现,结合影像学表现见多发小结节,融合成片,逐渐由磨玻璃影转化为实变影的过程,符合腺癌生长特点,综合胃镜镜下及病理表现、头皮病理及免疫组化表现,提示胃癌转移可能大;支气管肺泡灌洗液中虽未找到明确的肿瘤细胞,但看到个别类似印戒的细胞,为胃癌肺转移可能大。
活动后呼吸困难、干咳是弥漫性间质性肺疾病常见的临床症状。其临床特点、影像学及病理学表现多样,需综合分析各种临床资料进行鉴别诊断,在谨慎排除各类继发性肺间质病基础上再行诊断原发性或特发性肺间质病变。对于不常见的间质病表现,如胸痛、皮疹、胸腔积液、体重下降等临床征象,务必要谨慎对待,小心求证,不可随意忽略,必要时积极行活组织检查,以探究竟。胃癌导致肺转移大多以血行播散为主,其引起的肺淋巴管癌病是一种特殊的转移形式,较为少见,但胃印戒细胞癌是发生肺淋巴管癌病的常见肿瘤之一,影像学可表现为小叶间隔不规则增厚伴周边型小结节、纵隔淋巴结肿大和(或)胸腔积液。
(暴婧 高占成)
1.American Thoracic Society,European Respiratory Society.American Thoracic Society/European Respiratory Society international multidisciplinary consensus classification of the idiopathic interstitial pneumonias.Am J Respir Crit Care Med,2002,165:277-304.
2.Travis WD,Costabel U,Hansell DM,et al.American Thoracic Society,European Respiratory Society.An official American Thoracic Society/European Respiratory Society statement:update of the international multidisciplinary classification of the idiopathic interstitial pneumonias.Am J Respir Crit Care Med,2013,188(6):733-748.
3.Dai H,Liu J,Liang L,et al.Increased lung cancer risk in patients with interstitial lung disease and elevated CEA and CA125 serum tumour markers.Respirology,2014,19(5):707-713.













