(一)临床特点
现病史:患者赵××,男,57岁。汉族,已婚,干部,山西省籍。主因“间断发热3个月,发现皮下痛性结节2个半月”,于2013年7月29日入院。患者于3月前受凉后出现发热,体温波动在37.5~37.8℃,无咳嗽、咳痰,无胸痛、咯血,无喘憋等不适,于当地门诊及医院给予对症治疗体温正常,半月后再次发热一次,经抗感染、退热等对症治疗体温正常,后发现胸骨柄前皮下结节,有明显压痛,当地给予“封闭”治疗效果欠佳,间断给予“抗感染、止痛”治疗。半月余前行胸部CT提示右下肺软组织占位,增强后不均匀强化,考虑恶性肿瘤,右下肺阻塞性肺炎,胸骨柄右下方局限性骨质破坏。骨扫描提示胸骨放射性增高灶,考虑骨转移。当地医院考虑恶性肿瘤伴骨转移,但两次气管镜检查未见异常,于右下肺支气管做细胞刷检未见癌细胞。今为进一步诊治就诊于我院。患者目前精神状态良好,体力正常,食欲正常,睡眠正常,近3个月体重下降约17kg,大便正常,排尿正常,为进一步检查及治疗入院。
既往史:否认肝炎、结核、疟疾等传染病史;否认高血压、心脏病病史,否认糖尿病、脑血管疾病、精神疾病病史;2009年因腰椎间盘脱出行腰椎钛合金支架置入术;否认外伤史,否认输血史;应用“对乙酰氨基酚”后曾出现全身皮疹。否认食物过敏史,预防接种史不详。
个人史及家族史:生于山西晋城城区,久居于当地,无疫区、疫情、疫水接触史,无牧区、矿山、高氟区、低碘区居住史,无化学性物质、放射物、毒物接触史,无毒品接触史,间断吸烟1年,无饮酒史。适龄结婚,育有1子1女,子女体健。父母已逝,死因不详,1兄1姐1妹健在,均体健,家族中无传染病及遗传病史。
(二)入院查体
体温:36.1℃,脉搏:62 次 /分,呼吸:18次/分,血压:115/75mmHg。患者神志清楚,体型偏瘦,胸骨柄下端可见如核桃大小皮下肿物,质硬,活动度差,有压痛,浅表淋巴结未触及肿大,胸廓对称无畸形,双肺呼吸音清,未闻及干湿性啰音,心律齐,未闻及杂音,肝脾未触及肿大,双下肢无水肿。
(三)辅助检查
血常规:白细胞计数6.42×109/L,中性粒细胞0.56。
凝血:FIB 4.97g/l,D-dimer 0.66μg/ml。
生化:肝肾功能、电解质、血脂等均正常。
血清四项:乙肝核心抗体、表面抗体阳性。
肿瘤标记物:CA19-9 51.77U/ml,余大致正常。
血气分析(未吸氧):pH 7.35,PO2 75mmHg,PCO2 48mmHg,BE 0.1mmol/L,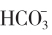 26.2mmol/L。
26.2mmol/L。
痰培养:草绿奈瑟菌属。
胸部CT(2013年7月16日山西王台医院)胸部CT示右下肺软组织占位性病变(增强后不均匀强化),考虑恶性肿瘤,右下肺阻塞性肺炎,胸骨柄右下方局限性骨质破坏。
骨扫描(2013年7月18日中国医科院肿瘤医院)胸骨放射性增高灶,考虑骨转移,余骨骼未见异常。
气管镜检查(2013年7月12日中国医科院肿瘤医院)未见异常。于右下肺支气管做细胞刷检未见癌细胞。
腹部超声:未见异常。
双下肢超声:未见血栓。
颈部、锁骨上超声:未见异常淋巴结。
腹股沟超声:左腹股沟区低回声结节考虑良性。
头颅MRI:脑内散发缺血灶。
入院诊断
1.肺癌伴骨转移可能性大。
2.腰椎间盘支架置入术后。
入院后完善相关检查,复查胸部CT(图1)考虑右肺下叶肺癌伴阻塞性炎症可能;建议结合临床对比前片及增强检查定夺;胸骨转移可能。
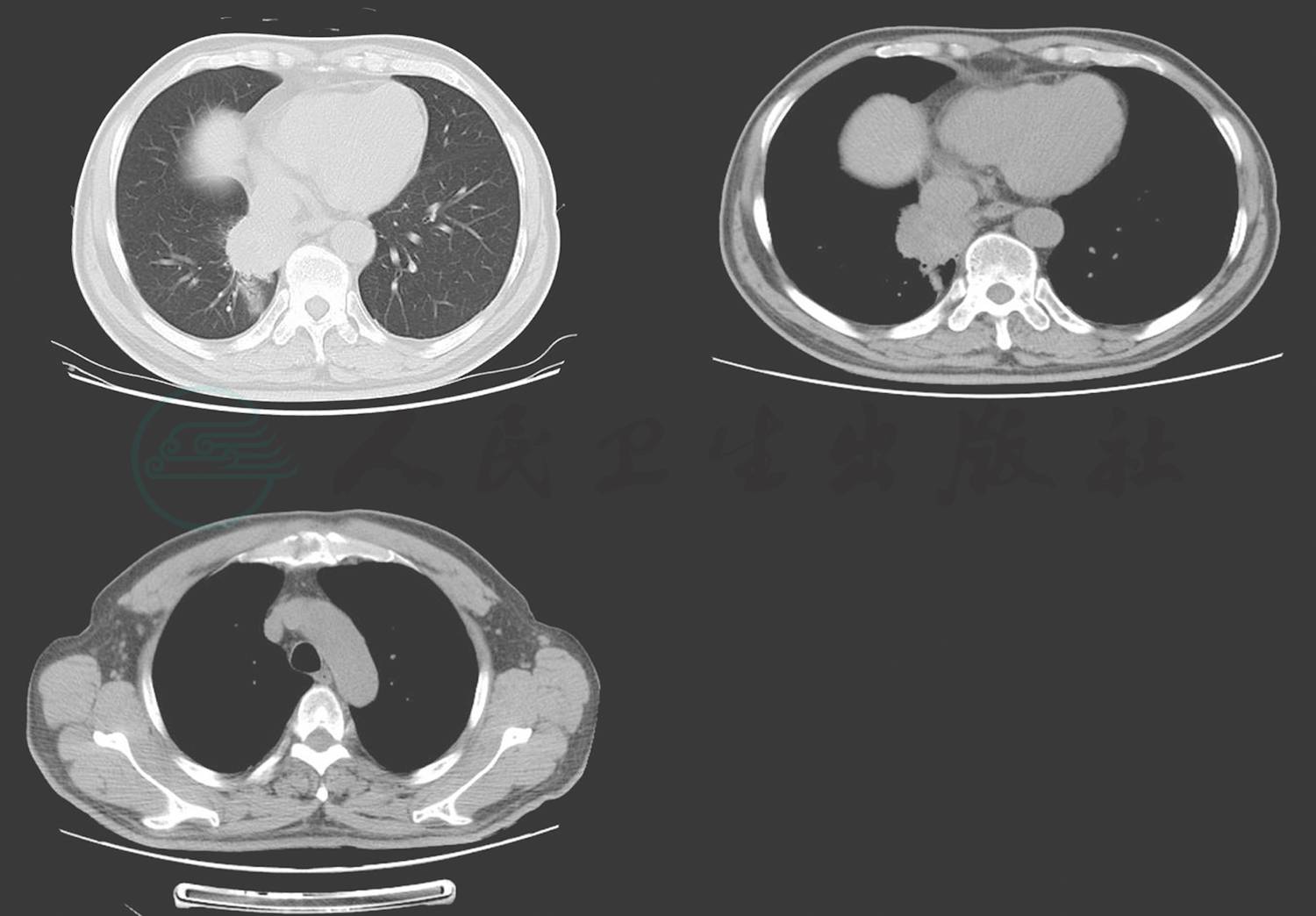
图1 胸部CT
行CT引导下肺穿刺活检术,病理回报上皮中-重度不典型腺瘤性增生。患者术后发热,先后给予头孢呋辛、亚胺培南西司他丁抗感染治疗后体温正常。查胸椎磁共振平扫+增强提示:胸骨及周围软组织异常,结合临床病史不除外转移可能;右侧胸腔少量积液。查PET/CT提示:右肺中叶及下叶中轴间质增粗,轻度放射性浓聚。右肺下叶体积缩小,下叶实质内见局限性浓聚,SUVmax:7.24,与周围实变组织边界欠清晰。右肺下叶近脊柱旁呈软组织密度,且密度不均,内见局限性放射性分布减低,周围放射性轻度摄取,SUVmax:3.19。纵隔及两侧肺门未见异常肿大淋巴结或淋巴结浓聚。胸骨体下缘及胸骨柄上缘髓腔内见局限性低密度影,边界尚清,放射性浓聚,SUV max:4.93,周边软组织肿胀。综上所见,首先非肿瘤性病变可能,累及肺及胸骨微动关节,建议胸骨及肺内高代谢病变穿刺活检除外其他。后行CT引导下胸骨穿刺活检,病理回报:少许骨小梁组织内见纤维组织增生,其内血管内皮细胞增生明显,并见少许炎性渗出,诊断肿瘤性病变证据不足。请胸外科会诊,考虑右下叶肺癌可能,并且胸骨部分骨质破坏可能。建议再行胸骨穿刺明确诊断。再次行CT引导下胸骨穿刺活检,病理回报(图2):(胸骨穿刺物)穿刺骨组织内见局灶朗格汉斯组织细胞增生、淋巴细胞、浆细胞、嗜酸性粒细胞及中性粒细胞浸润,间质血管内皮增生显著,未见转移癌。
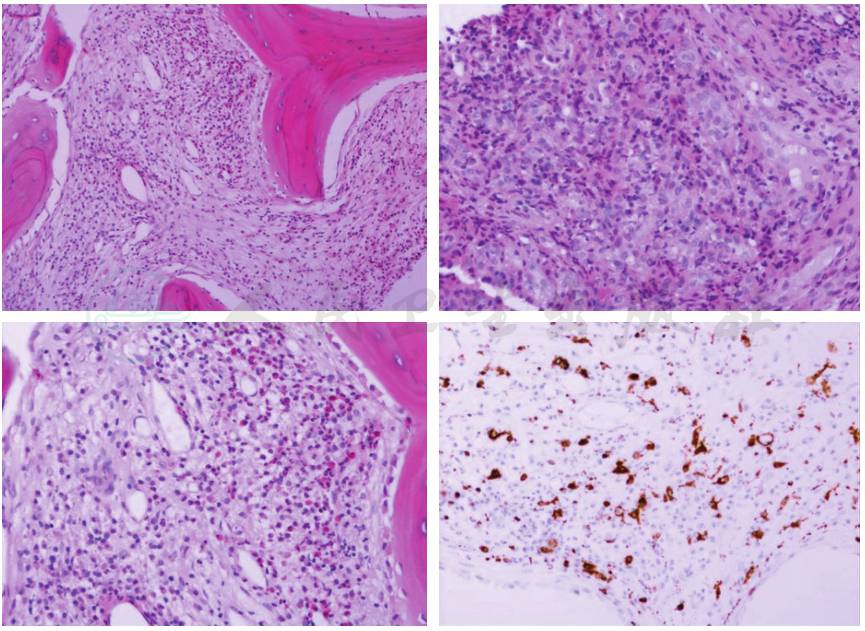
图2 胸骨穿刺活检病理
不除外朗格汉斯组织细胞增生症。血液科会诊建议全身化疗。胸外科会诊考虑诊断性胸腔镜手术治疗。与患者及家属沟通后,同意先明确肺内病灶性质再行化疗,要求转胸外科行胸腔镜手术。术中探查见右肺下叶内基底段可见肺实变,下肺韧带增厚,周围胸膜水肿,逐步打开下肺韧带,见到异常动脉由腹腔内发出至右肺下叶实变病灶。结合术前影像判断为肺隔离症,决定行右肺下叶切除术。术后病理回报:于距支气管3.5cm紧邻肺膜处见一囊实性病变区,与周围组织界尚清,符合右肺下叶肺叶内型隔离肺。回顾术前肺部增强CT,重建血管三维图像(图3),见由腹主动脉发出侧支血管供应胸部异常肺组织。将胸骨穿刺病理结果送至北大人民医院会诊,考虑为慢性骨髓炎性病变,建议随访观察。患者治疗好转出院,定期随访,病情稳定。
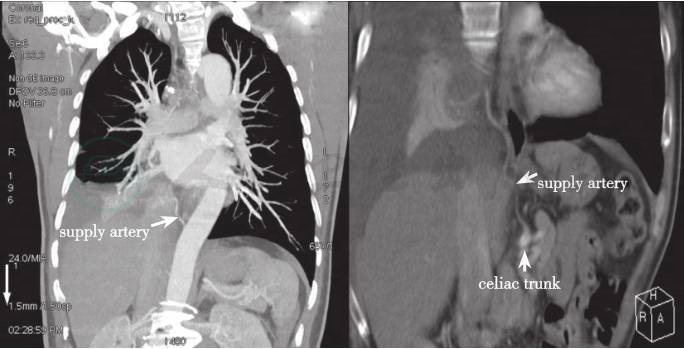
图3 肺部增强CT,重建血管三维图像
1.右下肺肺隔离症(叶内型)。
2.胸骨骨髓炎。
3.腰椎间盘支架置入术后。
肺隔离症(pulmonary sequestration,PS)是一种少见的先天性畸形,于1777年由Huber首次报道,占全部先天性肺发育畸形的0.15%~6.4%[1]。它是接受来自体循环异常分支动脉供血的无功能肺组织块。根据异常肺组织有无完整的胸膜与正常肺组织分界,分为叶内型和叶外型。CT表现以肿块影、囊肿影、肺内囊实性阴影为主,罕有以薄壁空洞为表现的肺段隔离症报道。叶内型肺隔离症的肺泡内可以有侧支气体交通,因此可经常出现痰中带血和病变部位的反复感染。高分辨率螺旋CT,尤其是其血管造影功能,在显示肺内病变的同时,可以通过三维血管重建显示异常供血动脉,对异常动脉的起源、走行和分支提供准确直观的信息,已经成为影像学诊断肺隔离症的金标准。为防止肺部感染反复发作或出现致命性大出血,本病一经确诊或高度怀疑,首选手术治疗。该患者经手术明确诊断为肺隔离症(叶内型),并得到根治。
朗格汉斯组织细胞增生症(Langenhans cell histiocytosis,LCH)是“孤儿病”,年发病率0.5~5.4/百万。发病机制假说认为是病毒感染或基因突变后淋巴细胞和组织细胞无规律地异常增殖,朗格汉斯组织细胞之间异常地相互作用所致。临床表现为多系统受累,尤其以肺、骨骼、中枢神经系统受累最为常见,而出现肺部囊状病变、骨质破坏、尿崩症等作为LCH的重要提示。肺部CT常为双肺弥漫性病变,以中上肺病变为主,早期表现为斑片、磨玻璃和小结节影,中晚期可出现空洞性肉芽肿及纤维瘢痕。与该病例特点不符,且病理诊断证据不够充分,通过随访观察,基本排除该诊断。
该患者为中年男性,因“发热伴肺部阴影合并胸骨破坏”前来就诊,进行多项检查后显示肿瘤性疾病可能性大,按照常规思路首先选择组织穿刺活检以明确诊断。先后进行三次不同部位活检,均未能找到肿瘤的病理诊断依据,且出现了出血、发热等术后并发症,一度疑诊为朗格汉斯组织细胞增多症。最后,通过胸腔镜手术才明确诊断为右下肺肺隔离症,整个检查过程十分曲折。该病例给我们几点启示:一是肺部阴影伴骨质破坏不一定为肿瘤性疾病,对于肺部阴影待查患者,建议增强肺部CT扫描后再进行穿刺活检。二是对于影像学表现不典型的肺部阴影待查病例,要注意排除肺隔离症,必要时要进行血管三维重建以辅助诊断。
(胡 晔)
1.Danieia G,Ralf E,Claus-Peter H,et al.Lung sequestration:A rare cause for pulmonary symptoms in adulthood.Respiration,2011,82(5)445-450.
2.Vassallo R,Ryu JU,Colby TV,et al.Pulmonary largerhans’cell histiocytosis.N Engl J Med,2002,342:1969-1978.













