男性,44岁。
间断视物模糊半年,发现血压高1天。
患者半年来无明显诱因间断出现视物模糊,未诊治。1天前加重伴头晕、头痛,测血压220/130mmHg,查眼底示“双侧眼底出血”,经急诊入院。自发病来无喘憋,夜间可平卧;无阵发性心悸、面红;无水肿,无尿量及尿色异常。
既往体健,每年体检血压及尿常规均正常。否认糖尿病、冠心病及脑血管病史。吸烟25年,20支/日。父母均患高血压。
身高172cm,体重 80kg(体重指数 27.0kg/m2),血压:左上肢 150/100mmHg,右上肢150/100mmHg,左下肢 170/100mmHg,右下肢 180/100mmHg,脉搏 76次/分,眼睑无水肿,结膜无苍白;双肺无异常体征;心界不大,各瓣膜听诊区未闻及杂音及附加音;双下肢不肿。颈部、腰腹部、未闻血管杂音,双下肢足背动脉搏动对称、无减弱。
入院后完善相关辅助检查:血常规 WBC 8.8×109/L,Hb 132g/L,PLT 228×109/L。ESR 7mm/h。尿常规:尿糖(-),蛋白 500mg/dl,镜检 RBC 6~8/HP,WBC 2~3/HP;24小时尿蛋白定量 4.2g。生化检查 TP 60.8g/L,ALB 38.9g/L,UA 360μmol/L,血糖4.65mmol/L,K+ 3.3mmol/L,Na+ 131.1mmol/L,Cl- 100.1mmol/L,CO2CP 25.2mmol/L,SCr 118μmol/L,TG 2.09mmol/L,Tcho 6.33mmol/L,HDL-C 1.16mmol/L,LDL-C 4.88mmol/L。CCr 68ml/min。禁水 12小时之后血渗透压 293mOsm/kg,尿渗透压476mOsm/kg。眼底检查示双侧视盘边界尚清,双侧视网膜动脉细,A∶V=1∶3,可见多处棉绒斑及线状出血。ECG大致正常。UCG提示左室肥厚,左室射血分数66%。肾脏B超:左肾12.3cm×5.4cm×4.3cm,实质厚1.8cm;右肾12.2cm×5.3cm×4.3cm,实质厚 1.8cm,双肾形态正常。
恶性高血压
由于患者合并大量蛋白尿,初步诊断考虑为“恶性高血压(MHT),肾实质性可能大”。在将患者的血压控制于140/90mmHg以下后,复查24小时尿蛋白仍为3.6g,遂于入院第7天行肾活检检查,结果提示“恶性高血压肾损伤”。对于患者的后续随访提示在血压控制良好的情况下,入院后第21天复查24小时尿蛋白为0.9g。此外,患者入院时存在低钾血症,完善肾素-血管紧张素-醛固酮系统检查提示血肾素、血管紧张素及醛固酮均升高;血儿茶酚胺、尿VMA及17羟皮质类固醇均正常。
该患者肾活检病理及内分泌系统的相关检查不支持肾实质性高血压及内分泌性高血压。而其高血压的特点为短期内出现、3种降压药物难以控制(顽固性高血压)以及恶性高血压,因此在除外了上述两种继发性高血压的情况下,高度怀疑肾血管性高血压。遂行肾动脉彩超检查,左肾动脉起始部血流束变细(0.22cm),局部呈杂色,峰值流速>400cm/s,提示左肾动脉起始部狭窄,阻力指数0.76。颈部及双下肢血管彩色超声多普勒未见明显异常。肾动态检查提示左肾 GFR 12ml/(min· 1.73m2),右 肾 GFR 45ml/(min ·1.73m2)。考虑到患者需要应用多种降压药物控制血压、左肾GFR下降但肾脏大小及结构尚可,存在介入治疗指征,遂与患者充分交代血管重建治疗的利弊后,决定进行肾动脉血管重建治疗。肾动脉造影检查显示左肾动脉起始部存在 90%狭窄,呈偏心性,位于肾动脉分为前后两支的分叉处(图1);因此难以行肾动脉支架植入术。经泌尿外科会诊后转科行自体肾移植。术后第3天始停用所有降压药物,血压波动于 115~125/70~80mmHg。术后肾动脉病理示“动脉粥样硬化”。目前随访至术后 8年,应用一种钙离子拮抗剂血压控制良好;24小时尿蛋白定量0.35g;SCr 123μmol/L。
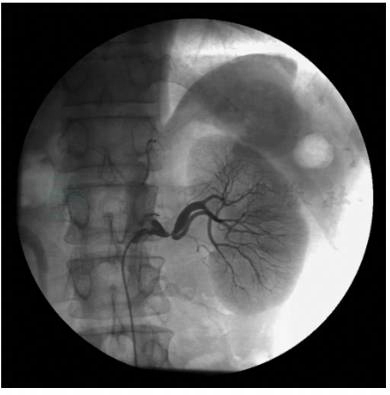
图1 肾动脉造影:左肾动脉起始部90%狭窄
动脉粥样硬化性肾动脉狭窄 肾血管性高血压 恶性高血压 慢性肾脏病3期
动脉粥样硬化性肾动脉狭窄(ARAS)的临床特征主要为高血压、肾功能损害和其他部位动脉粥样硬化的表现。在肾动脉狭窄≥50%的ARAS患者中,高血压患病率可达93%~95.8%。其高血压通常是原发性高血压与肾血管性因素混合参与的结果,常需应用两种或两种以上降压药物治疗方可控制满意;而在血管重建治疗后,降压药物的种类可减少,甚至毋需应用。ARAS患者肾功能受损通常是缓慢进展的过程,肾动脉狭窄引起的缺血性改变、高血压性肾动脉硬化、胆固醇栓塞以及继发性局灶节段性肾小球硬化等多种病变均参与其过程,如不干预,最终可进展至终末期肾脏病(ESRD)。许多研究表明,与肾功能正常的患者相比,肾功能受损的患者在行血管重建治疗后肾功能改善不理想,并且死亡率明显增高。在一些情况下,ARAS患者也可出现急性肾衰竭,如应用血管紧张素转换酶抑制剂(ACEI)、低血容量或胆固醇栓塞等。需提出的是,通常认为年龄大于50岁是ARAS的危险因素,但随着动脉粥样硬化性疾病发病年龄的提前,对于小于50岁的患者也应考虑ARAS的可能。
ARAS的治疗方式分为内科保守治疗和血管重建治疗。内科保守治疗是本病的基础治疗,无论是否行血管重建,都强调调整生活方式和药物治疗,后者主要包括抗血小板聚集、控制血压、控制血脂等。对于血管重建(包括PTRA、经皮腔内肾动脉成形术加支架(PTRAS)和手术治疗),不应仅以肾动脉狭窄程度≥70%~75%作为指征,而应该充分评价患者的临床情况和风险/获益比。2009年发表了肾动脉血管成形和支架植入研究(ASTRAL)将806例ARAS患者随机分为保守治疗和PTRAS治疗,进行为期5年的随访。结果显示,PTRAS组在血压和肾功能方面并未观察到明显获益,但有 23例患者出现了严重并发症。2013年底公布的CORAL研究(肾动脉狭窄心血管预后研究)对947例合并高血压和(或)慢性肾脏病的患者随机分为保守治疗和PTRAS治疗,平均随访43个月。两组在联合初级终点事件及全因死亡均无差别,仅在血压控制上,PTRAS组较保守治疗组降低收缩压-2.3mmHg,虽然差异有统计学意义,但临床意义不显著。基于现有的循证医学证据,ARAS的血管重建治疗未显示出明显优于保守治疗之处,应谨慎选择。特别是当出现肾动脉狭窄侧肾脏长径低于7.5~8.0cm;既往有胆固醇栓塞病史者;肾动脉狭窄侧肾脏 GFR<5ml/(min·1.73m2),或肾动脉彩色多普勒超声提示阻力指数>0.8,则不推荐血管重建治疗。
1.ARAS是老年人肾血管性高血压的主要病因,常伴有其他部位的动脉粥样硬化。
2.ARAS拟行介入治疗时应充分评价风险/获益比。不论是否行血管重建治疗,都应给予生活方式的调整和药物治疗,包括抗血小板聚集、调脂、稳定斑块等。
(张路霞 周福德)
1.Safian RD,Textor SC.Renal artery stenosis.New Engl J Med,2001,8,344(6):431-442.
2.ASTRAL Investigators,Wheatley K,Ives N et al.Revascularization versus medical therapy for renal-artery stenosis.N Engl J Med,2009,361(20):1953-1962.
3.王梅,王海燕.慢性缺血性肾脏疾病的诊断与治疗(三)动脉粥样硬化引起的肾动脉狭窄的诊断与治疗.中华内科杂志,2002,1:56-58.
4.Cooper CJ,Murphy TP,Cutlip DE,et al.Stenting and medical therapy for atherosclerotic renal-artery stenosis.N Engl J Med,2014,370(1):13-22.













