男性,51岁
间断低热、水肿5个月,发现血肌酐升高、血小板减低1个月。
5个月前无诱因低热,37.3~37.8℃,无明确感染征象,抗生素治疗7天无好转,出现颜面及双下肢水肿,外院予利尿治疗后水肿好转,仍间断低热。1个月前再次出现双下肢水肿,外院查尿红细胞88/HP,尿蛋白 1.9g/d。 血常规:WBC 3.7×109/L,Hb 132g/L,血小板52×109/L,SCr 188.6μmol/L。 自发病以来精神食欲差,近1个月尿量减少,600~900ml/d,大便正常,发病来体重下降约8kg。
无特殊。
体温37.6℃,脉搏91次/分,呼吸19次/分,血压135/70mmHg;双侧颈部、锁骨上、双腋窝、双腹股沟可触及数个肿大淋巴结,最大约3cm×3cm。双肺呼吸音粗,未闻及干湿啰音。心界不大,心律齐。腹软,脾肋下一指,双下肢中度水肿。
ESR 21mm/h,CRP 11.3mg/L↑。 生化:ALT及AST正常,ALB 32g/L。 LDH 266IU/L↑、HBDH 299IU/L↑、总胆红素10.8μmol/L、结合胆红素 1.80μmol/L。外周血涂片:破碎红细胞0.5%。Coombs试验阴性。
胸片:双侧胸腔积液伴右下肺不张。B超双肾大小正常,实质回声增强。脾大,腹水。
急性肾损伤
血栓性微血管病?
淋巴结肿大原因待查
患者中年男性,亚急性病程,临床表现为多系统受累:①低热、乏力、食欲减退、体重下降;②肾脏:血尿、蛋白尿,SCr上升,B超示双肾大小正常,考虑急性肾损伤;③血小板减低,虽无贫血,胆红素正常,但LDH、HBDH升高,外周血涂片破碎红细胞0.5%,提示血栓性微血管病(TMA)可能;④多处浅表淋巴结无痛性肿大,脾大、胸腔积液、腹水。
查 ANA、抗 dsDNA 和 ENA 谱(-)、ANCA(-)、抗 GBM 抗体(-)、抗血小板抗体(-),补体正常,无自身免疫病证据。血IgG 23.1g/L↑,IgA 4.09g/L↑,IgM正常,血免疫固定电泳:未见单克隆区带,不支持多发性骨髓瘤。该患者全身多处淋巴结肿大,故行淋巴结活检,淋巴结病理示:淋巴结滤泡增生,外套层扩大,呈葱皮样排列,生发中心及滤泡间血管增生,浆细胞增生,符合混合型Castleman病(图1)。
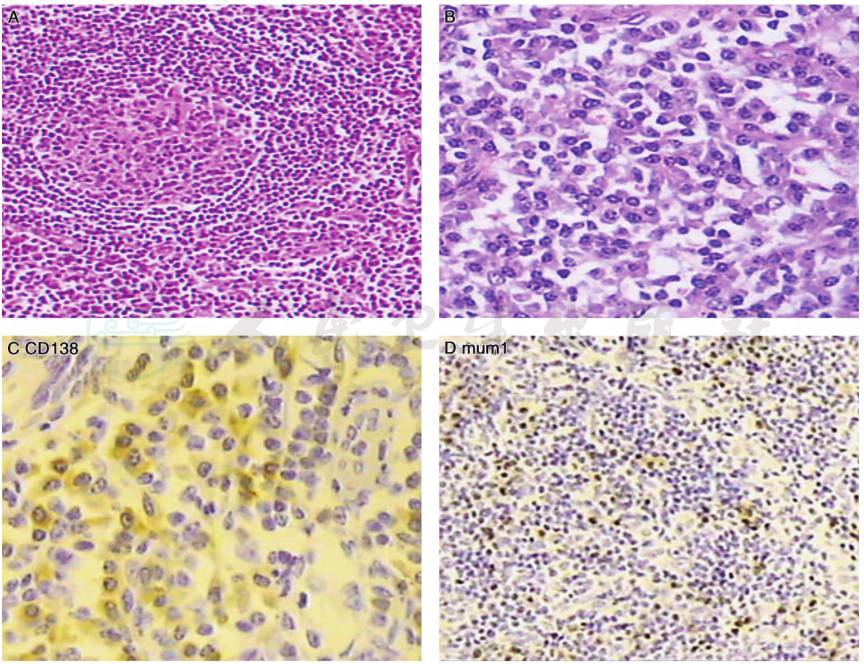
图1 Castleman病合并血栓性微血管病样病变:A:淋巴结浆细胞浸润(HE×200),B:淋巴结浆细胞浸润(HE×400),C:CD138阳性的浆细胞(免疫组化×400),D:mum1阳性的浆细胞(免疫组化×200)
为了明确肾脏病变及TMA诊断,输注血小板后行肾活检。肾脏病理学检查:免疫荧光:IgG(-),IgA(-),IgM(++),C3(-),C1q(-),FRA(-),Alb(-),颗粒样、团块状系膜区、毛细血管壁沉积。
光镜:肾小球内皮细胞弥漫节段增生,基底膜不规则增厚,节段性双轨征形成,毛细血管腔可见微血栓形成,肾小管上皮空泡及颗粒变性,灶状萎缩,肾间质灶状淋巴和单核细胞浸润伴纤维化,小动脉管壁增厚,内膜增生,符合血栓性微血管病样肾损伤(图2)。

图2 Castleman病合并血栓性微血管病样病变:肾小球缺血性皱缩,内皮细胞增生肿胀,微血栓形成,入球小动脉和小叶间动脉管壁增厚,内膜增生、黏液变性,管腔狭窄(PASM×200)
电镜:肾小球毛细血管基底膜增厚,内疏松层增宽伴疏松、颗粒状结构分布,内皮细胞肿胀,上皮足突节段融合,符合血栓性微血管病样肾损伤(图3)。
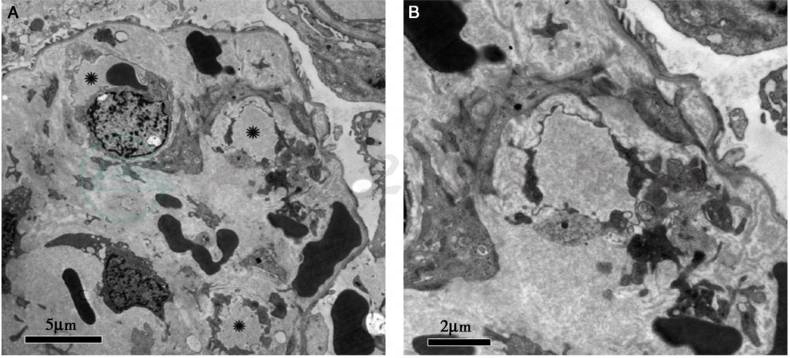
图3 Castleman病合并血栓性微血管病样病变:肾小球内皮细胞增生,红细胞破碎,GBM.内疏松层明显增宽(电镜×8 000)
予VP方案化疗:甲泼尼龙120mg静滴3天,之后泼尼松60mg/d口服。长春新碱1mg每周注射1次共4次。患者精神好转,乏力减轻,淋巴结减小,SCr恢复至80μmol/L,复查尿蛋白2.1g/d,PLT 96×109/L,CRP 2.2mg/L,IgG、IgA 恢复至正常水平。
目前患者门诊随访2年,维持泼尼松10mg/d口服,肾功能正常,尿蛋白仍1~2g/d。
Castleman病(混合型多中心型) 血栓性微血管病 血栓性微血管病肾损伤 急性肾损伤
Castleman病(CD)是一种少见的慢性淋巴细胞增生性疾病,研究提示与病毒感染特别是人类疱疹病毒8(HHV-8)的感染、白细胞介素-6(IL-6)及血管内皮细胞源性生长因子(VEGF)的水平异常相关。临床上,根据肿大的淋巴结累及单个或多个淋巴结区,分为单中心型(UCD)和多中心型(MCD)。最近有文献将无明确病因(即排除感染特别是病毒感染、肿瘤、自身免疫病)的MCD称为特发性MCD(iMCD)。组织学上,分为透明血管型、浆细胞型和混合型。透明血管型约占90%以上,表现为淋巴滤泡增生,滤泡周围淋巴细胞呈同心圆样排列构成葱皮样外观,滤泡间和副皮质区的小血管显著增生,血管壁增厚伴玻璃样变,多数无全身症状,淋巴结肿大多为单中心型;浆细胞型临床上多为多中心型淋巴结肿大,可见增生的淋巴滤泡间大量浆细胞浸润,多伴有全身性表现,如发热、乏力、体重下降、水肿、高球蛋白及低白蛋白血症、肝脾肿大、POEMS综合征等;混合型兼具上述两者的病理特点,临床表现与浆细胞型类似,新近定义的TAFRO综合征(血小板减少、全身水肿、骨髓纤维化、肾功能不全、器官肿大)多见于混合型MCD且免疫球蛋白水平多正常。
目前本病肾脏受累的机制尚未被完全阐明。肾脏受累者临床上多为多中心型、组织学上多为浆细胞型或混合型。北京大学第一医院总结了19例Castleman病肾脏受累的病例,95%出现不同程度的蛋白尿,74%出现血尿,63%出现急性肾损伤。曾有文献总结了已有的CD肾脏受累的病例报道,指出淀粉样变是最主要的肾脏改变,而我们总结的CD病例显示TMA样改变是最常见的肾脏受累表现,与法国的一项病例总结结果相似。目前认为VEGF在TMA样改变中起了作用,但具体机制尚待研究。本病合并肾脏受累的其他病理类型尚有膜性肾病、新月体性肾炎、急性间质性肾炎等。
需要指出的是,尽管本例患者未检出自身抗体,但浆细胞型或混合型Castleman病中,实验室检查常可发现多种自身抗体,如抗核抗体、ANCA、抗GBM抗体、Coombs试验阳性,ASO、RF升高等,这与异常增殖的浆细胞分泌抗体有关。因此,对于存在自身抗体合并淋巴结肿大的患者,不能满足于自身免疫性疾病的诊断,应争取获得淋巴结病理诊断,避免漏诊或误诊。
手术切除瘤体可使UCD患者的临床表现和实验室检查恢复正常。对于MCD,多采用化疗,但尚无统一的治疗方案。可试用的药物包括泼尼松、环磷酰胺、硫唑嘌呤、美法仑(马法兰)、长春新碱、秋水仙碱、利妥昔单抗等,近年来陆续有采用IL-6或IL-6受体的抗体成功治疗本病的报道。伴发的肾脏损害多随Castleman病的好转而好转。我们的研究显示,化疗可以改善多数肾脏受累患者的肾脏损伤,肾脏受累似乎并不影响患者的总体生存率。
1.Castleman病依据病理学特点分为透明血管型、浆细胞型和混合型,肾脏受累多见于后两者。
2.我国TMA样改变是Castleman病肾脏受累的常见病理类型。
3.针对Castleman病化疗,肾脏病变常随原发病的缓解而缓解。
(徐大民 刘 刚)
1.Xu D,Lv J,Dong Y,et al.Renal involvement in a large cohort of Chinese patients with Castleman disease.Nephrol Dial Transplant,2012,27(Suppl 3):iii119-125.
2.Komatsuda A,Wakui H,Togashi M,et al.IgA nephropathy associated with Castleman disease with cutaneous involvement.Am J Med Sci,2010,339(5):486-490.
3.El Karoui K,Vuiblet V,Dion D,et al.Renalinvolvement in Castleman disease.Nephrol Dial Transplant,2011,26(2):599-609.
4.Seida A,Wada J,Morita Y,et al.MulticentricCastleman’s disease associated with glomerular microangiopathy and MPGN-like lesion:does vascular endothelial cell-derived growth factor play causative or protective roles in renal injury? Am J Kidney Dis,2004,43(1):E3-E9.
5.Fajgenbaum DC,Uldrick TS,Bagg A et al.International,evidence-based consensus diagnostic criteria for HHV-8-negative/idiopathic multicentric Castleman disease.Blood,2017,129(12):1646-1657.













