男性,50岁。
关节肿痛8年,水肿3年,加重6个月。
8年前出现双手指间、双膝、双肩关节肿痛、晨僵,诊为“类风湿关节炎”,未规律诊治。3年前逐渐出现双下肢水肿,关节肿痛加重,外院查尿蛋白(+++),潜血(-),24小时尿蛋白定量 4.1g,血 ALB 26.4g/L,SCr 88μmol/L,ESR 118mm/h,诊为“慢性肾小球肾炎”,予雷公藤多苷治疗,效果欠佳。近1年来关节疼痛症状反复发作,考虑“类风湿关节炎”及“痛风”,间断应用雷公藤多苷及碳酸氢钠治疗。6个月前Scr波动于100~145μmol/L之间,2个月前查尿蛋白(+++),潜血(-),ALB 26.8g/L,SCr 150μmol/L,Egfr 46ml/(min·1.73m2)。 尿量不少,2 000~3 000ml/d,B超提示双肾偏大,为进一步诊治入院。
无特殊。
体温36.5℃,脉搏76次/分,呼吸18次/分,血压115/80mmHg;全身皮肤巩膜无黄染;浅表淋巴结未触及肿大;双肺听诊呼吸音清,未闻及干、湿啰音,心率76次/分,律齐,心音有力,未闻及病理性杂音;腹软,全腹无压痛及反跳痛,肝、脾肋下未触及,双下肢轻度可凹性水肿。
肾病综合征 慢性肾脏病3期
类风湿关节炎
患者为中年男性,既往8年类风湿关节炎,3年肾病综合征病史,曾应用雷公藤多苷治疗,效果不佳。类风湿关节炎合并肾脏疾病有肾小球疾病和肾小管疾病两类:①肾小球疾病常见IgA肾病、AA型淀粉样变性病,或因患者应用治疗类风湿关节炎的药物,如金制剂后出现膜性肾病。该患者无血尿,且无应用特殊药物病史,考虑不能除外AA型淀粉样变性病。②肾小管肾间质疾病,多与长期应用NSAIDs类镇痛药物或雷公藤多苷等药物有关。本例患者没有肾小管肾间质损害的临床表现。
入院后相关化验检查示:①肾脏:尿蛋白+++,镜检无红白细胞,尿糖(+),尿蛋白定量11.52g/d,ALB 23.3g/L(↓),SCr 150μmol/L。 Hb 100g/L,正细胞正色素性,网织红细胞正常,Coombs’试验阴性,便潜血阴性,考虑肾性贫血可能性大;②免疫炎症指标:ESR 136mm/h,RF 106U/mL,CRP 102mg/L,免疫球蛋白、补体水平正常,ANCA及抗GBM抗体阴性,ANA、抗dsDNA及ENA谱阴性,血/尿免疫固定电泳未见单克隆免疫球蛋白区带。③关节病变:双手关节X线片可见双手掌指及指间关节、双腕关节骨质破坏,关节间隙狭窄,符合类风湿关节炎改变。
为进一步明确病理诊断,患者行腹壁脂肪活检:无特殊蛋白沉积,刚果红染色阴性,未见淀粉样蛋白沉积。肾活检病理检查:免疫荧光 C1q(+),于系膜区及小动脉壁沉积,余免疫球蛋白阴性,κ和λ轻链染色均阴性;光镜下可见13个肾小球,特殊蛋白大量沉积,肾小球结构破坏,肾小管弥漫萎缩,多数蛋白管型。肾间质弥漫淋巴和单核细胞浸润伴纤维化。小动脉管壁增厚,特殊蛋白沉积,刚果红染色阳性。符合淀粉样变性肾病(晚期)(图1)。
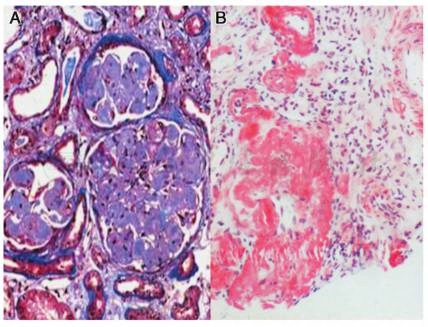
图1 AA型淀粉样变性肾病:A:肾小球大量特殊蛋白沉积,系膜结节样硬化(Masson×200);B:肾小球、小动脉的特殊蛋白刚果红染色阳性(刚果红染色×200)
补作免疫组化染色AA蛋白为阳性(图2);电镜:肾小球系膜区和基底膜大量淀粉样细纤维沉积(图3),肾间质及血管壁上也可见淀粉样纤维物质沉积。符合晚期淀粉样变性肾病。故考虑为AA型淀粉样变性病诊断明确。
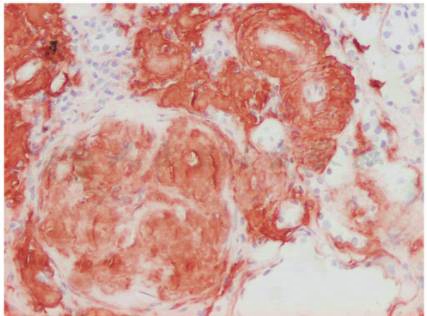
图2 AA型淀粉样变性肾病:肾小球和小动脉淀粉样AA蛋白阳性(免疫组化×200)

图3 AA型淀粉样变性肾病:肾小球系膜区和毛细血管基底膜淀粉样纤维沉积(电镜×8 000)
肾病综合征 淀粉样变性肾病(AA型) 慢性肾脏病3期 肾性贫血
类风湿关节炎
淀粉样变性病是一组由不同种类的淀粉样物质在细胞外沉积导致器官功能障碍的疾病,根据导致沉积的物质不同而分为30种不同类型。血清淀粉样蛋白A(SAA)沉积时称为AA型淀粉样变性病。血清淀粉样蛋白A是由肝脏合成的炎症反应蛋白,当患者存在慢性炎症性疾病(慢性感染如炎症性关节炎;自身免疫性疾病如类风湿关节炎、炎性肠病等)时,SAA浓度持续升高,部分患者会逐渐发展成为AA型淀粉样变性病,自出现炎症性疾病到发展为AA型淀粉样变性病平均需17年。
本病在确诊方面需要注意的是:免疫组化是确诊AA蛋白推荐的方法,而高锰酸钾氧化后刚果红染色不准确,国际上早已不再推荐使用。
AA型淀粉样变性病患者临床肾脏受累最突出(97%),表现为蛋白尿和肾功能不全;常见受累器官还有脾脏(89%)、肝脏(23%),而心力衰竭(0.9%)、肾上腺皮质功能不全(1.3%)少见。应用放射性碘元素标记血清淀粉样P物质(SAP,是组成所有类型淀粉样变沉积物的一种基质蛋白)可以帮助评价淀粉样物质累及脏器的范围。监测SAA蛋白浓度可以评价患者体内SAA负荷情况:血清SAA负荷低时淀粉样物质沉积可减少,相反,若SAA负荷较高,则加重,SAA血清水平与患者生存时间负相关。
对于AA型淀粉样变分型诊断的主要目的在于指导治疗:AA型不需要用针对单克隆浆细胞的肿瘤抑制治疗。其治疗分为针对慢性炎症的对因治疗,和针对并发症的对症治疗。根据炎症性疾病不同,对因治疗也不同,如类风湿关节炎的患者应用免疫抑制(环磷酰胺等)治疗、慢性结核或骨髓炎的患者应用抗感染治疗。近年,淀粉样物质基质蛋白如硫酸乙酰肝素、SAP等也作为治疗的靶点之一,例如阻止SAA与氨基多糖形成多聚体的新药eprodisate,有可能会延缓肾功能恶化,但尚需进一步疗效观察。对症治疗包括利尿、对ESRD患者进行肾脏替代治疗。
与AL型淀粉样变患者相比,AA型淀粉样变病患者预后较好,平均生存期为133个月,患者预后不良与高龄、低蛋白血症、起病时即进入终末期肾脏病阶段,以及随访过程中SAA浓度升高有关。
总之,AA型淀粉样变性病与慢性炎症性疾病相关,进展较慢,肾脏受累明显,确诊需依靠免疫组化检查染色AA蛋白,治疗主要诊断原发病,预后较AL型淀粉样变性病好。
1.AA型淀粉样变性病的主要病因是慢性炎症。
2.确诊AA型淀粉样变需要依靠病理,分型推荐AA蛋白免疫组化染色。
3.AA型淀粉样变性病的主要治疗以针对原发病治疗为主,患者预后相对较好。
(曲 贞 张 宏)
1.Lachmann HJ,Goodman HJ,Gilbertson JA,et al.Natural history and outcome in systemic AA amyloidosis.N Engl J Med,2007,356(23):2361-2371.
2.曲贞,郑欣,鄂洁,等.肾淀粉样变性病32例临床病理特点及误漏诊分析.中华实用内科杂志,2009,29(1):75-77.
3.Gillmore JD,Lovat LB,Persey MR,et al.Amyloid load and clinical outcome in AA amyloidosis in relation to circulation concentration of serum amyloid A protein.Lancet,2001,358(9275):24-29.
4.Dember LM,Hawkins PN,Hazenberg BP,Gorevic PD,Merlini G,Butrimiene I,et al.Eprodisate for the treatment of renal disease in AA amyloidosis.N Engl J Med,2007,356(23):2349-2360.













