女性,45岁。
间断胸闷、心悸4个月,双下肢水肿1个月。
患者4个月前无明显诱因出现活动后头晕、胸闷、心悸,无意识丧失,休息后可缓解;就诊当地查血红蛋白88g/L,诊为“缺铁性贫血”,予以补铁治疗后症状无明显好转。1个月前逐渐出现双下肢及眼睑水肿,伴尿量减少,500~800ml/d,并出现直立后晕厥,外院查血红蛋白 118g/L,尿蛋白(+++),RBC 0/HP,尿蛋白定量 8.81g/d,血 ALB 27.3g/L,SCr 65μmol/L,双肾体积正常,为进一步诊治入院。发病以来体重下降5kg。
患者3年来规律体检,血红蛋白100~110g/L,1年前体检尿检正常。无其他疾病史。
体温 36.5℃,脉搏 104 次/分,呼吸 18 次/分,血压 95/50mmHg(卧位)、70/40mmHg(立位),心率130次/分。全身皮肤巩膜无黄染;浅表淋巴结未触及肿大;双肺听诊呼吸音清,未闻及干、湿啰音,心界左大,心尖搏动点位于第5肋间锁骨中线外0.5cm处,心率104次/分,律齐,心音稍低,未闻及病理性杂音;腹软,全腹无压痛及反跳痛,肝、脾肋下未触及,双下肢轻度可凹性水肿。
肾病综合征 肾功能正常
患者为45岁中年女性,既往无慢性肾脏病史,此次起病以肾病综合征为主要表现,合并直立后晕厥、血压下降、心率增快等直立性低血压的表现,在临床过程中排除了容量不足等可导致直立性低血压的原因,在肾病综合征的情况下体重下降5kg,需考虑是否为恶性肿瘤相关肾脏疾病,包括实体瘤(如肺癌、乳腺癌、胃肠道肿瘤、甲状腺肿瘤等)和血液系统恶性肿瘤(如淋巴瘤、多发性骨髓瘤和系统性淀粉样变性病等)。检查方面需要系统地筛查血液系统、循环系统、消化系统等。
患者入院后相关实验室检查:①肾脏:尿蛋白(++++),RBC 0/HP,UTP 11.95g/d,ALB 12.5g/L(↓),SCr 54.9μmol/L。②血液系统方面:血清免疫固定电泳:可见单克隆IgGλ(+)单克隆轻链λ条带,冷球蛋白定性:阳性;冷球蛋白成分分析:单克隆免疫球蛋白IgGλ。骨髓活检:骨髓浆细胞异常增生(浆细胞占2%,骨髓间质内见较多幼稚样浆细胞增生、浸润,少见成熟浆细胞),伴轻链限制性表达[λ(++),κ散在个别细胞(+)],未见淀粉样物质沉积(刚果红染色阴性),头颅、骨盆平片未见骨质破坏、溶骨性改变。未达多发性骨髓瘤诊断标准。③心脏方面:入院后持续低血压,反复晕厥数次,应用多巴胺等升高药物效果不佳。心电图:肢体导联低电压。超声心动图:左心室壁增厚(室间隔及左室后壁厚度:1.3cm,回声稍强),左室射血分数正常(69%),右室壁增厚(右室前壁厚度0.6cm),二尖瓣、三尖瓣轻度反流,少量心包积液。BNP 1 431pg/ml(↑)。患者室壁增厚程度与血压不平行,提示可能存在心脏淀粉样物质沉积。④消化系统方面:腹部B超肝脏形态、大小正常,实质回声欠均匀。脾脏大小正常。 肝酶升高:ALP 225IU/L(↑),GGT 204IU/L(↑),前白蛋白 128.8mg/L(↓)。提示可能存在肝脏淀粉样物质沉积。⑤实体肿瘤筛查:胸片未见占位,查体未发现甲状腺及乳腺占位。血清肿瘤标记物阴性。
为进一步明确病理诊断,患者行肾活检,病理显示:免疫荧光:IgM(++)、C3(+)、λ(++)、κ(-);系膜区颗粒样沉积,其余免疫球蛋白均为阴性;光镜:17个肾小球,肾小球系膜区、节段性毛细血管壁可见无细胞结构性特殊蛋白沉积,刚果红染色阳性。小动脉管壁增厚伴淀粉样蛋白沉积(图1),偏振光显示为双折光苹果绿色(图2)符合淀粉样变性肾病。电镜:肾小球系膜区及节段性基底膜无细胞性不规则增宽,可见直径8~10nm的淀粉样纤维沉积,上皮足突弥漫融合,未见电子致密物(图3),符合淀粉样变性肾病。该病理结果证实患者为淀粉样变性病的诊断。患者病理λ轻链染色阳性,结合患者血清单克隆免疫球蛋白轻链λ阳性,考虑患者为轻链型(AL型)淀粉样变性病。
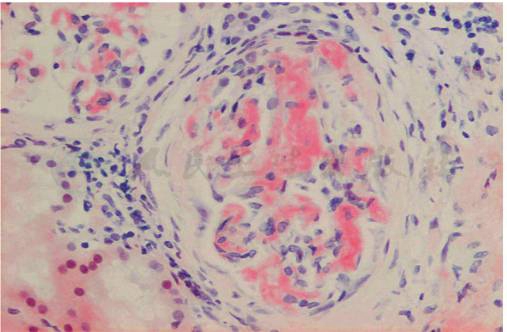
图1 AL型淀粉样变性病:肾小球系膜区大块刚果红染色阳性的特殊蛋白沉积(刚果红染色×400)
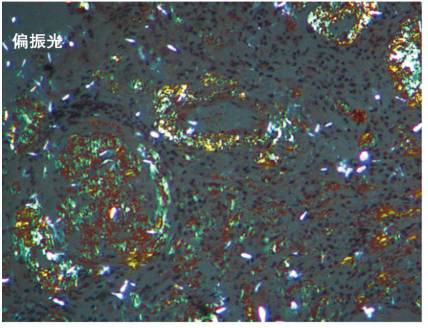
图2 AL型淀粉样变性病:刚果红阳性的肾小球和小动脉显示绿色偏振光(偏振光×200)
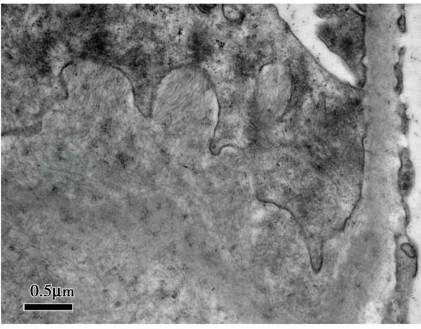
图3 AL型淀粉样变性病:肾小球系膜区可见排列紊乱的细纤维丝,直径约8~10nm,即淀粉样纤维,未见电子致密物(电镜×30 000)
患者后转入血液科继续治疗,因患者循环系统受累明显,凝血功能下降,考虑由于淀粉样变肝脏合成功能受累;间断出现腹泻考虑为淀粉样变消化道受累,未行骨髓移植。予以地塞米松20mg每日1次,共治疗4天,并间断予血浆、蛋白等扩容、支持治疗,患者后出现低血压、意识丧失、心率20次/分,考虑为心源性休克,最终死亡。
AL型淀粉样变性病
淀粉样变性病是一组由不同种类的淀粉样物质在细胞外沉积导致器官病理和功能障碍的疾病,是中老年人继发性肾病综合征的重要原因之一。淀粉样变性病根据沉积物质不同而分为30种不同类型,其中最常见的是由免疫球蛋白轻链沉积所导致的AL型淀粉样变性病(light chain amyloidosis)。
AL型淀粉样变性病与单克隆免疫球蛋白轻链在器官异常沉积有关,其中λ链比κ链更常见,部分患者与多发性骨髓瘤等浆细胞疾病有关。临床表现为多系统受累,肾脏:以肾病综合征多见,可有肾小管损伤;循环系统:包括低血压、心脏肥厚、恶性心律失常等;器官肿大:肝脏、脾脏、舌体肿大;胃肠道系统:食欲减退、腹泻、消化道出血或溃疡等。北京大学第一医院总结32例系统性淀粉样变性病患者,其中31例为AL型,主要提示该病的临床线索为:40岁以上肾病综合征患者若出现以下情况要警惕AL型淀粉样变:①低血压或血压较基础值下降>20mmHg;②血、尿免疫固定电泳出现单克隆免疫球蛋白轻链;③合并器官肿大;④体重下降。其中,血尿免疫固定电泳意义更大,其对于40岁以上大量蛋白尿患者诊断AL型淀粉样变的敏感性和特异性分别为81.3%和97.6%。
病理检查是确诊淀粉样变的金标准:淀粉样物质刚果红染色呈现砖红色;在偏振光显微镜下表现为双折光苹果绿色;电镜下表现为直径8~10nm的排列紊乱的细纤维丝。不同部位活检阳性率有所差别,包括肾脏(>90%)、腹壁脂肪(60%~80%)、直肠黏膜(50%~70%)、骨髓(50%~55%)、皮肤(50%)等多部位,肾脏活检的阳性率最高,原因可能与肾脏病理常规进行电镜检查,可发现早期淀粉样变性病有关。
诊断后还要进行分型,推荐应用免疫荧光或组化的方法进行免疫球蛋白轻链、AA蛋白等染色,原来的高锰酸钾氧化法已被淘汰。值得注意的是,AL型淀粉样变患者沉积的免疫球蛋白轻链往往为变异轻链,应用单克隆抗体染色轻链阴性时仍不能除外,可试用多克隆抗体行免疫荧光或免疫组化染色。
AL型淀粉样变性病的发病机制为异常增多的单克隆免疫球蛋白形成异常的β片层样结构并在组织内沉积,最终造成器官功能障碍。部分AL型淀粉样变性病继发于多发性骨髓瘤。单克隆免疫球蛋白是否形成淀粉样物质,与其突变基因位点有关。其中λ型更为常见。但合并κ型时更易合并血管和肝脏受累,临床进展更快。
原发性AL型淀粉样变性病治疗主要针对抑制单克隆免疫球蛋白合成。对于符合移植条件的患者(无明显心脏受累,少于3个脏器受累,年龄<70岁,血肌酐<150μmol/L),可选择行自体或异基因造血干细胞移植,术后可根据患者情况继续应用如硼替佐米或沙利度胺联合地塞米松,接受骨髓移植的患者其血液系统一年内有效率可达77%;对于无条件接受骨髓移植的患者,可选择地塞米松联合米尔法兰(马法兰),或环磷酰胺-硼替佐米-地塞米松的方案。其他治疗组合包括沙利度胺/来那度胺-环磷酰胺-地塞米松、硼替佐米-地塞米松、米尔法兰(马法兰)-来那度胺-泼尼松,均被证明有效。患者预后与受累脏器相关,心脏受累者预后最差,平均生存期在小于1年,而无心脏受累者平均生存期在8年左右。
总之,AL型淀粉样变性病是中老年人继发性肾病综合征的常见病因之一,需要根据患者血压、脏器肿大、体重下降、合并单克隆免疫球蛋白轻链等线索积极进行病理检查明确诊断及分型。早期诊断至关重要,这有赖于肾脏病理的细致观察。确诊后需要评估患者受累脏器决定治疗方案,行骨髓移植或化疗,其预后与受累脏器情况相关。
1.AL型淀粉样变性病的重要临床表现:40岁以上的肾病综合征患者出现血压下降、器官肿大、体重下降要警惕该病。
2.血、尿免疫固定电泳发现单克隆免疫球蛋白轻链提示该病可能性大。
3.确诊需要依靠病理,肾活检阳性率最高,电镜有助于发现早期淀粉样变性病,推荐使用免疫荧光或组化的方法进行分型。
(曲 贞 刘 刚)
1.Falk RH,Comenzo RL,Skinner M.The systemic amyloidosis.N Engl J Med,1997,337(13):898-909.
2.Qu Z,Zheng X,Wang SX,et al.Clinical and pathological features of renal amyloidosis:an analysis of 32 patients in a single Chinese centre.Nephrology (Carlton),2010,15(1):102-107.
3.Zhou FD,Zhang LX,Yao Y,et al.Immunofixation electrophoresis was highly specific for the diagnosis of renal light-chain amyloidosis.Am J Med Sci,2013,345(1):18-21.
4.Yao Y,Wang SX,Zhang YK,et al.A clinicalpathological analysis in a large cohort of Chinese patients with renal amyloid light-chain amyloidosis.Nephrol Dial Transplant,2013,28(3):689-697.
5.Dogan A.Amyloidosis:Insights from proteomics.Annu Rev Pathol.2017,24:277-304.
6.Gertz MA.Immunoglobulin light chain amyloidosis:2014 update on diagnosis,prognosis,and treatment.Am J Hematol,2014,89(12):1132-1140.
7.Grogan M,Dispenzieri A,Gertz MA.Light-chain cardiac amyloidosis:strategies to promote early diagnosis and cardiac response.Heart,2017,103(14):1065-1072.













