男性,23岁。
肉眼血尿20天,咯血10天。
20天前受凉后发热,体温38℃,伴咳嗽,咳少量白痰。2天后出现持续全程肉眼血尿,伴尿中泡沫增多。双下肢对称可凹性水肿,进行性加重,尿量不少。当地医院查尿蛋白(+++),红细胞满视野,血白蛋白23g/L,血肌酐143μmol/L。B超示双肾体积增大、皮质增厚,外院给予泼尼松40mg/d无好转。10天前患者出现咳嗽,痰中带鲜血,3~4次/天,10~20ml/d,未予处理。5天前患者自觉尿量减少,约500ml/d。3天前至我院查血红蛋白84g/L、血肌酐593μmol/L,血钾6.01mmol/L,同时出现少尿,急诊给予甲泼尼龙500mg冲击1次,血液透析1次,收入病房。
体健。
体温 36.6℃,脉搏 85次/分,血压 130/70mmHg,呼吸24次/分。双肺呼吸音粗,双下肺可闻及较多细湿啰音。心脏和腹部查体未见异常。双膝关节以下轻度可凹性水肿。
血 WBC 8.27×109/L,PLT 238×109/L,Hb 81.0g/L。ESR 26mm/h。尿 RBC满视野,为变形红细胞,尿蛋白定量 4.67g/d。血 SCr 634.0μmol/L,BUN 26.3mmol/L,ALB 24.3g/L,肝功能正常。RF阴性,CRP阳性,ANCA阴性,ANA、抗dsDNA、ENA阴性,抗GBM抗体阳性(百分结合率98%)。动脉血气分析:pH 7.352,PO269mmHg,PCO238mmHg,SaO293%。 胸片:两肺满布粟粒状模糊影,以两肺中下野为著,部分融合成团片状,肺野透过度差(图1)。
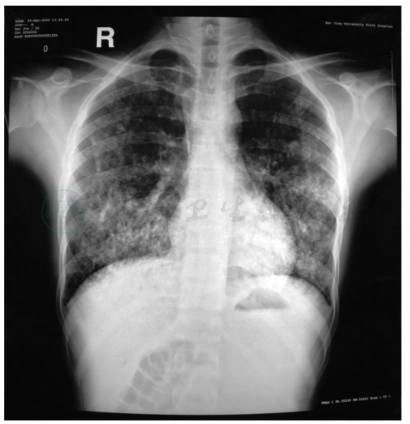
图1 胸部正位片:双肺粟粒状模糊影,以两肺中下野为著
抗肾小球基底膜病 急进性肾炎(Ⅰ型) 急性肾衰竭 高钾血症 肺出血 间质性肺疾病
患者血肌酐短期内迅速升高,出现少尿,B超提示双肾体积增大、皮质增厚,符合急性肾衰竭。根据患者出现血尿、大量蛋白尿、水肿及快速进展的肾功能损害,提示为肾小球疾病所致,符合急进性肾炎综合征。患者在出现急性肾衰竭的同时有肺出血,提示为多系统受累的疾病所致。进一步查ANCA、ANA、抗dsDNA、ENA均阴性,可以除外ANCA相关性小血管炎、系统性红斑狼疮。临床表现及辅助检查亦不支持抗磷脂综合征、血栓性微血管病、心衰、结核等疾病。同时查血清抗GBM抗体阳性,因此诊断为抗肾小球基底膜病,累及肾脏及肺,目前呈急性肾衰竭合并肺出血。
患者入院后立即给予血浆置换治疗,每日1次,每次3 000ml。患者入院第2天出现大咯血,予以机械通气辅助呼吸。入院第6天进行肾穿刺活检以明确肾脏病理诊断。免疫荧光:IgG(+++)、C3(+++)沿毛细血管壁线条样沉积(图2);光镜:19 个肾小球,毛细血管壁严重破坏,GBM断裂,100%新月体形成,16个细胞性新月体,3个细胞纤维性新月体。
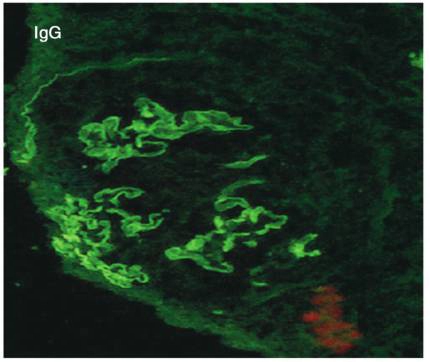
图2 Ⅰ型新月体性肾小球肾炎:肾小球新月体形成,IgG沿肾小球毛细血管壁呈线样沉积(免疫荧光×400)
肾小管多灶状萎缩,肾间质弥漫水肿伴多灶状淋巴、单核细胞浸润,少量中性粒细胞浸润,小动脉无明显病变(图3)。电镜:肾小球细胞性新月体形成,基底膜皱缩,未见电子致密物。肾小管上皮细胞微绒毛脱落。肾间质淋巴和单核细胞浸润。符合Ⅰ型新月体性肾小球肾炎。患者共进行12次血浆置换治疗,直至血清抗GBM抗体转阴。同时继续甲泼尼龙500mg/d,共3天,环磷酰胺50mg每日2次口服。10天后咯血停止,但肾功能未恢复,进入终末期肾脏病(ESRD),依赖透析。
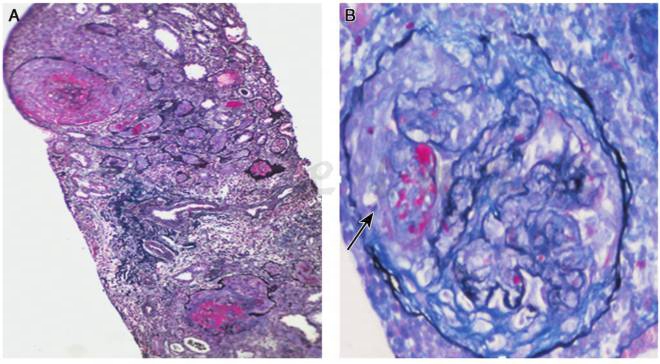
图3 Ⅰ型新月体性肾小球肾炎:肾小球毛细血管袢破坏,细胞纤维性新月体形成(↑),(A:PASM×100,B:PASM ×400)
抗肾小球基底膜病 急进性肾炎(Ⅰ型)急性肾衰竭→CKD 5期 肺出血 间质性肺疾病
本病例提供了一个典型的抗肾小球基底膜(glomerular basement membrane,GBM)病的范例,表现为肺出血-肾炎综合征,同时抗GBM抗体阳性,又称Goodpasture病。该病多病情凶险,起病急、进展快、预后差。肺受累可引起大咯血而危及生命。肾脏受累多为急进性肾炎Ⅰ型,表现为血尿、蛋白尿,肾功能进行性下降,较早出现少尿和无尿,短期内不可逆地进展至终末期肾衰竭。
抗GBM病的确诊依靠在血清中检出抗GBM抗体,或肾脏免疫病理学检查见到IgG和(或)C3沿肾小球毛细血管袢呈线样沉积。国内在开展抗GBM抗体血清学检测之前,诊断一直依靠肾活检免疫病理学检查,因此不能做到早期诊断。更为重要的是,并非所有患者的免疫病理均表现为典型的IgG、C3沿肾小球毛细血管袢呈线条样沉积,北京大学第一医院的研究发现仅有60%的患者有此表现。因此,对于有肺出血和尿检异常或肾功能损害的患者,不应等待肾活检结果,应提倡早期对抗GBM抗体进行血清学检测。应用人可溶性GBM蛋白为抗原的ELISA法是国内外通用和公认的抗GBM抗体的血清学检测方法。该法敏感性(95%)和特异性(99%)高,简便易行,结果客观。抗GBM病病情进展急骤,预后差,因此,根据典型的临床表现和可靠的血清学检测结果就可以进行诊断并立即开始治疗。及时创造条件尽早行肾活检,对于判断病情及估计预后有重要意义。
抗GBM病总体预后较差。确诊时SCr>600μmol/L或依赖透析、肾小球新月体比例100%提示预后不良。但如合并肺出血,仍应予以积极治疗。血浆置换是明确能够改善预后的治疗方法。其疗效与患者的临床表现、开始治疗的早晚和治疗是否充分密切相关。充分的血浆置换,置换量应为每天50ml/kg(最多4L),共14天或置换至血清抗GBM抗体转阴。血浆置换同时给予激素及免疫抑制治疗。该病人确诊时SCr>600μmol/L,肾小球新月体比例100%,虽然经过积极的血浆置换和免疫抑制治疗,仍然进入ESRD。
1.决定抗GBM病预后的关键在于早期诊断,急性肾衰竭或咯血者应及时检测血清抗GBM抗体。
2.及时肾活检利于判断病情活动和预测预后。
3.血浆置换是改善预后的首选治疗方法,应尽早充分进行。同时给予激素和免疫抑制治疗。
(崔 昭 陈 旻)
1.Cui Z,Zhao MH,Xin G,et al.Characteristics and prognosis of Chinese patients with anti-glomerular basement membrane disease.Nephron Clin Pract,2005,99(2):c49-55.
2.刘娜,赵明辉,章友康,等.急进性肾炎中抗肾小球基底膜抗体的检测及其临床意义.中华肾脏病杂志,1998,14(4):292-295.
3.Cui Z,Zhao J,Jia XY,et al.Anti-glomerular basement membrane disease:outcomes of different therapeutic regimens in a large single-center chinese cohort study.Medicine (Baltimore),2011,90(5):303-311.
4.Huart A,Josse AG,Chauveau D,et al.Outcomes of patients with Goodpasture syndrome:A nationwide cohortbased study from the French Society of Hemapheresis.J Autoimmun,2016,73:24-29.














