患者女性,38岁,因“反复咳嗽、胸闷、气喘6年”入院。患者反复发作性咳嗽、胸闷、气喘6年,感冒、寒冷、紧张时均可诱发,吸入“沙美特罗氟替卡松(舒利迭)”或“布地奈德福莫特罗(信必可)”症状可缓解,没有季节性发作特征,多在夜间、凌晨时发作。曾多次于当地医院住院就诊,予静脉应用“甲泼尼松龙、二羟丙茶碱”等治疗后症状缓解。患者近1年几乎每天发作咳嗽、胸闷、呼吸困难,多在夜间或凌晨发生,明显影响睡眠,吸入“布地奈德福莫特罗”症状可暂时缓解,次日再次发作。现为进一步诊治,拟诊“难治性哮喘”收治入院。
入院查体
T 37℃,P 88 次/min,R 18 次/min,BP 130/88mmHg,神志清晰,步入病房。 全身皮肤、黏膜无黄染,无肝掌、蜘蛛痣,未见皮下出血点,未见皮疹。全身浅表淋巴结无肿大。胸廓对称无畸形,胸骨无压痛;触觉语颤对称,未触及胸膜摩擦感,双肺叩诊呈清音,两肺满布哮鸣音,未闻及胸膜摩擦音。心率88次/min,律齐;各瓣膜听诊区未闻及病理性杂音。腹平坦,腹壁软,全腹无压痛,无肌紧张及反跳痛,肝脾肋下未触及,腹部移动性浊音阴性。双下肢无水肿。生理反射正常,病理反射未引出。
既往史及个人史
否认外伤史、手术史、输血史,否认肝炎、结核等传染病史,否认高血压,糖尿病史。否认吸烟饮酒史。有“过敏性鼻炎”,对“青霉素”过敏(皮试阳性),对“鱼、虾、蟹”过敏。
辅助检查
血常规(2017-03-11):白细胞:7.16×109/L,中性粒细胞:34.4%,淋巴细胞:32.5%,单核细胞:9.2%,嗜酸性粒细胞:22.8%,嗜碱性粒细胞:1.1%,血红蛋白:140g/L,血小板:265×109/L。
肺功能(2017-03-11):吸气肌肌力减退,呼气肌肌力减退,呼吸中枢驱动力增高,肺弥散功能中度减退。总呼吸道阻力增高,重度以限制为主的混合性肺通气功能障碍,小气道重度陷闭。呼气NO浓度均值:121μg/L。
外院鼻窦CT:双侧上颌窦、筛窦、蝶窦黏膜明显增厚。
初步诊断
难治性哮喘原因待查
问题1:患者是否符合难治性哮喘的诊断?
患者病情特点如下:38岁女性,反复发作性咳喘6年;查体满肺可闻及哮鸣音,血常规示嗜酸性粒细胞增高,肺功能示混合性通气功能障碍,小气道陷闭,FeNO明显升高,外院诊断哮喘和过敏性鼻炎;长期吸入激素和长效支气管扩张剂未控制,目前处于重度持续状态。根据2011年我国难治性哮喘诊断与处理专家共识,难治性哮喘的诊断需满足以下标准:①符合我国哮喘的诊断标准;②排除患者治疗依从性不良,并排除诱发加重或使哮喘难以控制的因素;③按照我国哮喘防治指南,采用4级治疗方案,即2种或2种以上控制性药物规范治疗和管理6个月以上,尚不能达到良好控制;符合以上3条标准可诊断为难治性哮喘。综合患者的临床特点可考虑难治性哮喘的诊断。
问题2:难治性哮喘的鉴别诊断与处理流程如何?
难治性哮喘在临床上需要与以下疾病相鉴别,如变应性支气管肺曲霉病(ABPA)、变应性肉芽肿性血管炎(CSS)等,哮喘仅是其系统性疾病的一个部分,对这部分患者吸入激素治疗难以奏效,需要全身激素治疗。另外,还有一些临床症状类似哮喘的疾病,如慢性阻塞性肺疾病(COPD)、支气管扩张症、慢性心功能不全、肺血栓栓塞症、囊性纤维化、声带功能障碍、α-抗胰蛋白酶缺乏症、复发性多软骨炎、气管异物和肿瘤以及OSAS等,临床上均可出现难以控制的气促或喘息,应仔细鉴别。为进一步明确诊断,我们完善了以下检查:
G 试验(2017-03-13):<10pg/ml。
血 IgE:279.2ng/ml。
血自身抗体系列、ANCA:均阴性。
变应原筛查(2017-03-13):大米:1+,大豆:1+,小麦:2+,鸡蛋:2+,牛奶:1+。
痰培养、真菌涂片(2017-03-11):均为阴性。
肺CT(2017-03-13):双肺多发渗出影,结节影和树芽征;广泛支气管壁增厚(图1)。

图1 胸部CT
A.双肺上叶弥漫性小结节影,伴树芽征,局部支气管扩张;B.纵隔窗未见明显异常;C.双肺多发磨玻璃影、结节影伴树芽征,支气管壁显著增厚伴扩张;D.纵隔窗未见明显异常
引自:主编:.呼吸与危重症医学疑难与危重病例精选.第1版.ISBN:978-7-117-30147-3
PET-CT(2017-03-15):①双肺弥漫性多发粟粒样结节伴FDG轻度增高,考虑为炎性病变,建议治疗后随访,余全身(包括脑)未见FDG代谢明显异常增高灶。②局部颅骨内板增厚,未见FDG代谢异常增高,考虑为良性建议随访。③双乳小叶增生。④肝脏脂肪浸润;肠炎。⑤子宫增大;双侧附件囊肿,建议妇科B超随访。⑥骨髓弥漫性FDG代谢轻度增高,考虑反应性改变,建议随访;颈、胸、腰椎体轻度骨质增生。
综合患者病情特点,需要与以哮喘为主要临床特征的两类疾病重点鉴别:
1.变态反应性支气管肺曲霉菌病(ABPA)
常以反复哮喘发作为特征,伴咳嗽、咳痰,痰多为黏液脓性,有时伴血丝,可分离出棕黄色痰栓;常有低热,肺部可闻及哮鸣音或干湿性啰音;X线可见浸润性阴影,段性肺不张,牙膏征或指套征(支气管黏液栓塞);外周血嗜酸性粒细胞明显增高;曲霉变应原皮肤点刺试验阳性,血清IgE水平通常比正常人高2倍以上,曲霉特异性IgE阳性。结合患者临床特征,血IgE不高,且无ABPA特征性影像学表现,因此,不支持变态反应性支气管肺曲霉菌病诊断。
2.嗜酸性肉芽肿性多血管炎(EGPA)
目前EGPA的诊断标准主要参考1990年美国风湿病学会提出的分类标准,包括临床表现、实验室检查、影像学检查及病理活检等。6条分类标准包括:①哮喘样症状(或喘息发作);②嗜酸性粒细胞增多(≥10%或绝对值≥1.5×109/L);③单发或多发性神经病变;④非固定性肺浸润;⑤鼻窦炎;⑥血管外嗜酸性粒细胞浸润。符合4条或以上者可诊断EGPA。我国2018年专家共识特别提出,该标准中的第1条“哮喘”的真正含义是指哮喘样表现,包括喘息、咳嗽、胸闷及呼吸困难等。结合病史及辅助检查,患者符合哮喘样症状,嗜酸性粒细胞增多,非固定性肺浸润,鼻窦病变4项诊断标准,EGPA诊断成立。EGPA一旦确诊,需详细评估呼吸系统、肾、心脏、胃肠道和/或外周神经等多器官受累情况。全身PET/CT提示肺部结节影和肠炎,但是患者无消化道症状;尚未发现神经系统等其他系统受累情况。
问题3:嗜酸性肉芽肿性多血管炎如何治疗?
EGPA的治疗取决于疾病的严重程度、受累的器官、病情是否活动等因素。参照最新全球专家共识,活动期全身型EGPA定义为新出现或复发或恶化的EGPA(不包括哮喘和/或耳鼻咽喉部表现),需要添加或增加激素用量和/或添加或更换其他免疫抑制剂。而参照我国支气管哮喘防治指南,活动期局限型EGPA的定义为喘息、咳嗽、胸闷等症状加重,并伴有呼气峰流速下降和/或外周血嗜酸性粒细胞升高。EGPA患者的预后与最初治疗方案相关。治疗方案包括:激素治疗(治疗EGPA的基础治疗,病情控制后可逐渐减量),激素联合免疫抑制剂治疗,靶向药物治疗(美泊利单抗等),其他吸入药物治疗(按照GINA4~5级的治疗方案),血浆置换、静脉丙种球蛋白治疗等。EGPA的预后取决于是否得到早期诊断和及时治疗。综合分析,患者属于活动期局限型EGPA,可单用全身激素治疗。
嗜酸性肉芽肿性多血管炎
1.甲泼尼龙40mg/d口服;
2.布地奈德福莫特罗(160/4.5μg)1吸/次,2次/d,吸入;
3.孟鲁斯特钠10mg/d,睡前服;
4.奥美拉唑40mg/d,口服;常规补钙。
1.1个月后门诊复诊患者咳嗽、胸闷症状明显好转。
2.患者2018年1月2日复查肺部CT较前(2017年3月)肺部渗出性病灶有所吸收,双肺多发结节明显减少;残留局部支气管壁增厚(图2)。给予激素减量维持,每3~6个月门诊随访。
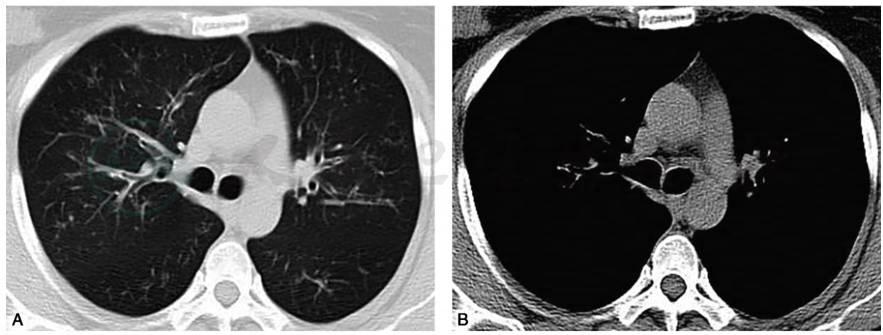
图2 患者长期口服激素并小剂量维持治疗,复查胸部CT
A.双肺渗出影、结节影和树芽征较前明显减少,仍残留有支气管壁增厚表现;B.纵隔窗未见明显异常
引自:主编:.呼吸与危重症医学疑难与危重病例精选.第1版.ISBN:978-7-117-30147-3
1.当支气管哮喘患者常规治疗后症状无法控制时,需要考虑难治性哮喘。难治性哮喘的原因包括以下几个方面:①在工作和生活环境中反复接触过敏源;②未规范或规律用药;③合并胃食管反流;④以哮喘为主要表现的其他疾病如:心源性哮喘、变应性支气管肺曲霉菌病和嗜酸性肉芽肿性多血管炎等。因此确诊难治性哮喘之前需行一系列鉴别诊断,最常需要鉴别的疾病为ABPA和EGPA。
2.EGPA的临床特征 平均发病年龄32岁,可用于鉴别嗜酸性肉芽肿性多血管炎的哮喘与普通人群的哮喘。肺是最常累及的器官,其次是皮肤。肺出血和肾小球肾炎发病率显著低于其他小血管炎。心脏是嗜酸性肉芽肿性多血管炎的主要靶器官,冠状动脉炎和心肌炎是患者致残和致死的主要原因。组织病理学可见坏死性小血管炎和嗜酸性粒细胞浸润型坏死性肉芽肿。EGPA临床分三期:前驱期可持续数年,可有过敏性鼻炎和哮喘;中期有显著的外周血嗜酸性粒细胞增高和嗜酸性粒细胞组织浸润;晚期是威胁生命的血管炎性期。
3.EGPA的影像学特点 最常见的肺部影像学表现包括双侧的、易变的、随机分布的非节段性实变影,实变区域易变,50%病变呈周围性分布,类似慢性嗜酸性粒细胞性肺炎或机化性肺炎。90%的患者高分辨CT可见双侧磨玻璃影或实变影,呈对称性分布,外周为主,少部分患者呈支气管周围分布或片状随机分布。另一个相对常见表现是大约50%的患者小叶间隔线清晰可见。小叶间隔增厚反映的是继发于心脏受损所致的小叶间隔水肿或小叶间隔嗜酸性粒细胞浸润。气道受累的表现包括小叶中央结节和树芽征,支气管扩张,支气管或细支气管壁的增厚。虽然上述表现常见于哮喘,但也常见于EGPA。嗜酸性粒细胞支气管壁浸润是导致管壁增厚的主要原因。心肌损害导致左心衰或嗜酸性粒细胞性胸膜炎,使得10%~50%的患者胸部CT可见单侧或双侧胸腔积液。其他少见的表现包括弥漫网状影或大小不等的结节影,很少发生空洞。
(章鹏 夏敬文 李圣青)
[1]Global Initiative for Asthma Report.Global strategy for asthma management and prevention (updated 2018)[EB/OL].[2019-10-21].https://www.ginasthma.org.
[2]MOUTHON L,DUNOGUE B,GUILLEVIN L.Diagnosis and classification of eosinophilic granulomatosis with polyangiitis (formerly named Churg-Strauss syndrome) [J].J Autoimmun,2014,49(2):99-103.
[3]中华医学会呼吸病学分会哮喘学组.难治性哮喘诊断与处理专家共识[J].中华结核和呼吸杂志,2010,33(8):572-577.
[4]嗜酸性肉芽肿性多血管炎诊治规范多学科专家共识编写组.嗜酸性肉芽肿性多血管炎诊治规范多学科专家共识[J].中华结核和呼吸杂志,2018,41(7):514-521.
[5]顾兴,张红军,刘伟,等.变应性肉芽肿性血管炎一例及文献复习[J].中华肺部疾病杂志(电子版),2017,10(2):235-236.
[6]GROH M,PAGNOUX C,BALDINI C,et al.Eosinophilic granulomatosis with polyangiitis (Churg-Strauss)(EGPA) Consensus Task Force recommendations for evaluation and management[J].Eur J Intern Med,2015,26(7):545-553.













