患儿,女,10岁。
主诉:反复咳嗽、口腔溃疡、结膜充血8个月,呼吸困难、青紫7个月。
现病史:患儿8个月前无明显诱因出现咳嗽,声咳,无痰,无喘息,无呼吸困难,无发热,同时口腔溃疡,疼痛明显,影响进食,于当地诊所静脉滴注头孢类抗生素1周,外用治疗口腔药物(具体不详),患儿咳嗽及口腔溃疡症状无明显好转,家属未予重视。7个月前患儿无诱因出现呼吸费力,表现为端坐呼吸,大汗,偶有喘息,喉部可闻及“咝咝”声,就诊于当地市级医院,予患儿静脉滴注头孢菌素和盐酸氨溴索等治疗,期间患儿咳嗽及呼吸困难有所缓解,但反复发作,发作时表现为呼吸困难,端坐呼吸,满头大汗,不能平卧,说话不成句,间断予吸氧、静滴激素、氨茶碱,雾化布地奈德和溴化异丙托溴铵及抗生素治疗2个月,患儿咳嗽症状基本消失,但仍有呼吸困难,喜坐位,夜间有时不能平卧,体力活动明显受限,平地走路距离不超过50m。4个月前,患儿再次呼吸困难加重,头颈部肿胀,颜面青紫,不能平卧,转入北京治疗,期间给予吸氧,全身糖皮质激素治疗,雾化布地奈德、异丙托溴铵,期间间断有低热,37.2~37.7℃,热型无规律,应用阿奇霉素、头孢曲松、头孢哌酮舒巴坦,曾怀疑合并真菌感染静脉滴注氟康唑,同时予两性霉素B雾化治疗,后改为替考拉宁并口服小剂量红霉素治疗4个月余,仍有低热,呼吸困难无好转,端坐呼吸,家属要求出院。北京住院期间追问病史,近6个月右侧腹痛,腹部超声提示腹部约7cm×8cm肿物,局部穿刺活检诊断“炎性肌纤维母细胞瘤”,因患儿有呼吸困难及低氧血症,未手术治疗及化疗。出院诊断为“间质性肺炎?弥漫性泛细支气管炎?支气管扩张,腹腔占位病变性质待查:炎性肌纤维母细胞瘤?口腔溃疡”,出院1个月家中口服甲泼尼龙片(8mg/d,每天1次)、卡托普利(12.5mg/次,每天2次)治疗至今。现患儿为求进一步诊治就诊于笔者医院。患儿病来间断有低热,体温不超过38℃;病后一直有口腔溃疡,口腔颊部及舌部溃疡,病初口腔内广泛溃疡(图1),近3个月溃疡明显减轻,曾有疼痛,影响饮食,现已适应,不再影响进食;同时伴有结膜充血,无眼痛,无畏光,无视物不清,无脓性分泌物。间断右下腹疼痛,钝痛,可忍受,无呕吐,食欲尚好,大、小便正常。
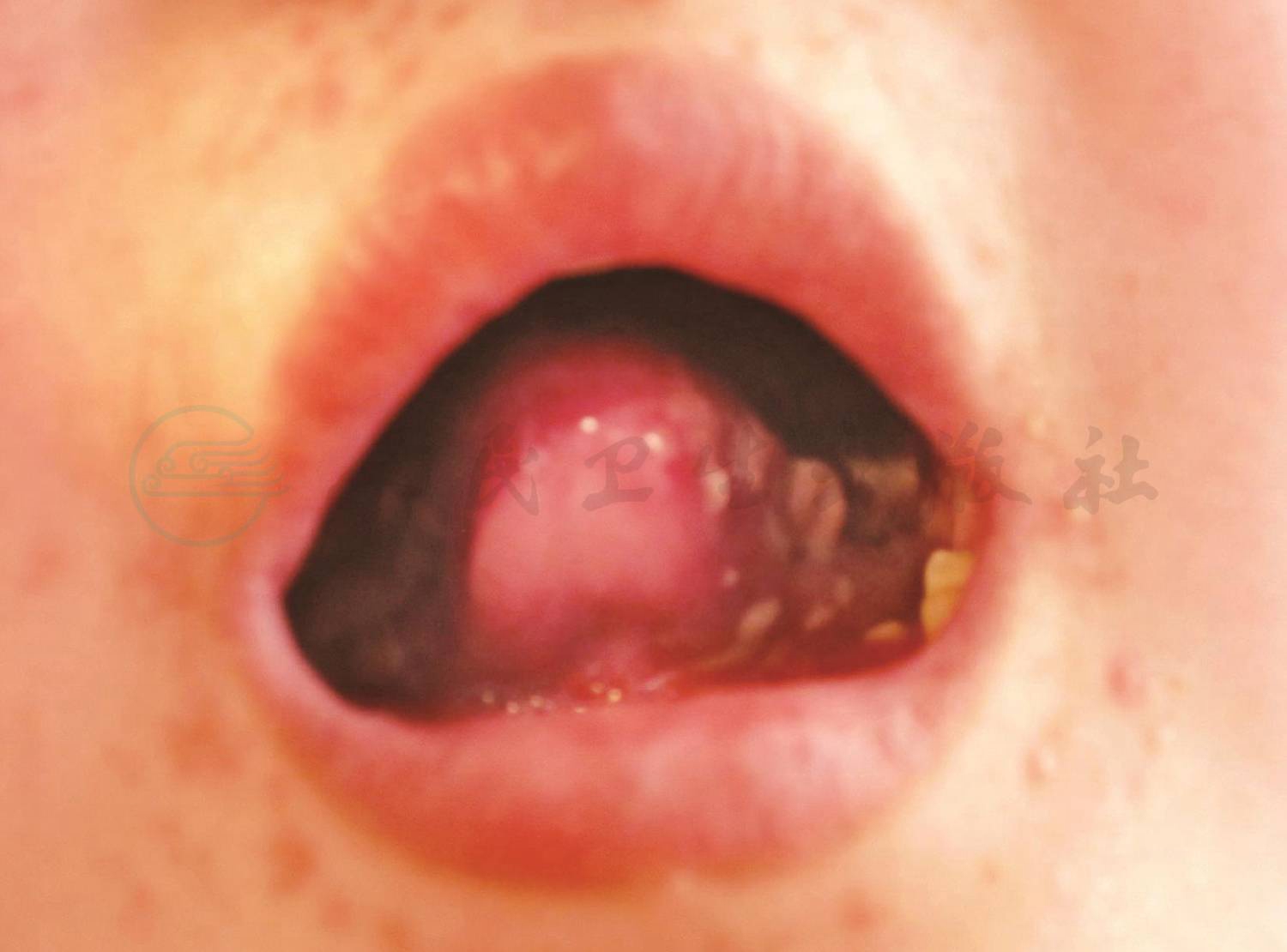
图1 口腔内广泛溃疡
既往史:患儿生后1岁因血管瘤行肌注局部栓塞治疗。3岁时患肺炎。既往平均每年患2~4次感冒。6岁起过水痘。既往无湿疹史,无喘息史,无慢性咳嗽病史。
过敏史:否认食物及药物过敏史。
个人及家族史:G1P1,足月剖宫产,生后无窒息,生长发育同正常同龄儿,疫苗按时接种,平时无揉眼睛、揉鼻子习惯,无湿疹史。有鼻炎史。否认遗传代谢病史。
入院查体及相关检查:体温36.9℃;脉搏141次/min;呼吸38次/min;血压129/65mmHg。鼻导管吸氧下2L/min,经皮血氧饱和度92%,离氧后经皮血氧饱和度可降至84%。神志清楚,一般状态差,鼻导管吸氧下轮椅推入病房。呼吸促,鼻翼扇动阴性,轻度三凹征,可见肋间肌参与呼吸。库欣综合征面容,满月脸,毛发较密集,面颊部皮肤红润,口唇明显发绀,可见暗紫色小血管影;双侧结膜充血,无分泌物。咽不赤,扁桃体无肿大,舌尖及舌两侧可见多发溃疡、肉芽样突起及纵行的条索样瘢痕,溃疡表面有薄层淡黄色分泌物,颊部黏膜无破溃、见陈旧暗红色瘢痕。双肺听诊呼吸音弱,肺底可闻及较密集细小水泡音,未闻及哮鸣音,呼吸相延长。心音有力,律齐,未闻及病理性杂音。腹软不胀,右下腹轻压痛,可触及质硬包块,因脂肪厚,边界触诊不理想,无反跳痛,无腹壁肌紧张,肝脾肋下未触及,外阴部及肛周黏膜无溃疡及瘢痕。四肢末梢温,四肢肌力及肌张力正常,膝腱反射及跟腱反射正常引出,颈软,克氏征、布氏征及双巴氏征阴性。可见杵状指/趾。
辅助检查:
1.(住院前4个月外院化验检查)血常规:WBC 9.04×109/L;N 64.9%;EO 0.2%。CRP 20mg/ml。ESR、ASO、PCT正常。肝肾功心肌酶正常;MPAb 1:160;G试验、GM试验阴性;痰抗酸染色无异常,PPD(72小时)(+)。3次痰培养:第1次流感嗜血杆菌30%,咽部正常菌群70%;第2次痰培养无致病菌;第3次痰培养咽部正常菌群90%,副流感嗜血杆菌10%。ANCA 阴性,ANAs:1:20,阳性;ENA谱 阴性;NSE、AFP、VMA正常。总 IgE:29.4U/ml。过敏原:烟曲霉特异性IgE阳性(外院)。
2.影像学及其他辅助检查 外院肺CT(图2)提示:肺内广泛间实质浸润,少许气胸,纵隔及皮下积气。外院纤维喉镜检查示鼻咽喉未见明显异常;鼻窦CT未见异常。支气管镜检查及肺泡灌洗回报:右下基底段深部亚支内分泌物堵塞。经支气管镜支气管内膜活检未见明确病变。24小时食管pH测定提示轻度病理性酸反流。外院腹部B超(图3):右侧髂窝处5.9cm×4.5cm×3.9cm包块,考虑肿瘤占位。腹部增强CT:右下腹盆腔内富血供实性占位,神经源性肿瘤?纤维瘤?骨髓检查可找到少许吞噬有核细胞的网状细胞,考虑与感染或肿瘤有关。口腔黏膜活检:慢性炎症。B超引导下腹腔穿刺活检术,(外院)病理检查提示腹腔炎性肌纤维母细胞瘤。
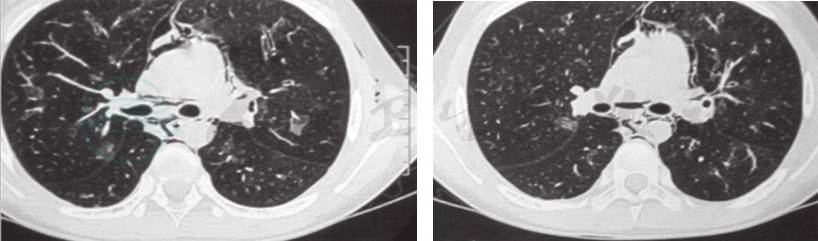
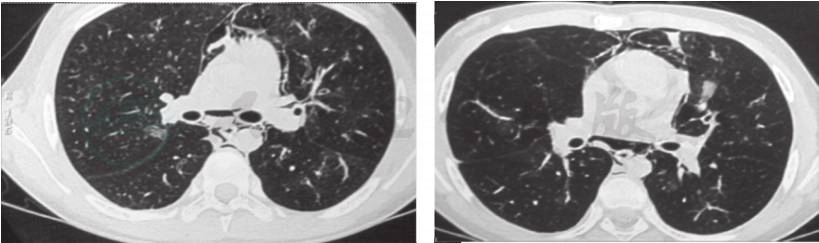
图2 入院前外院肺CT,提示:肺内广泛间实质浸润,少许气胸,纵隔及皮下积气
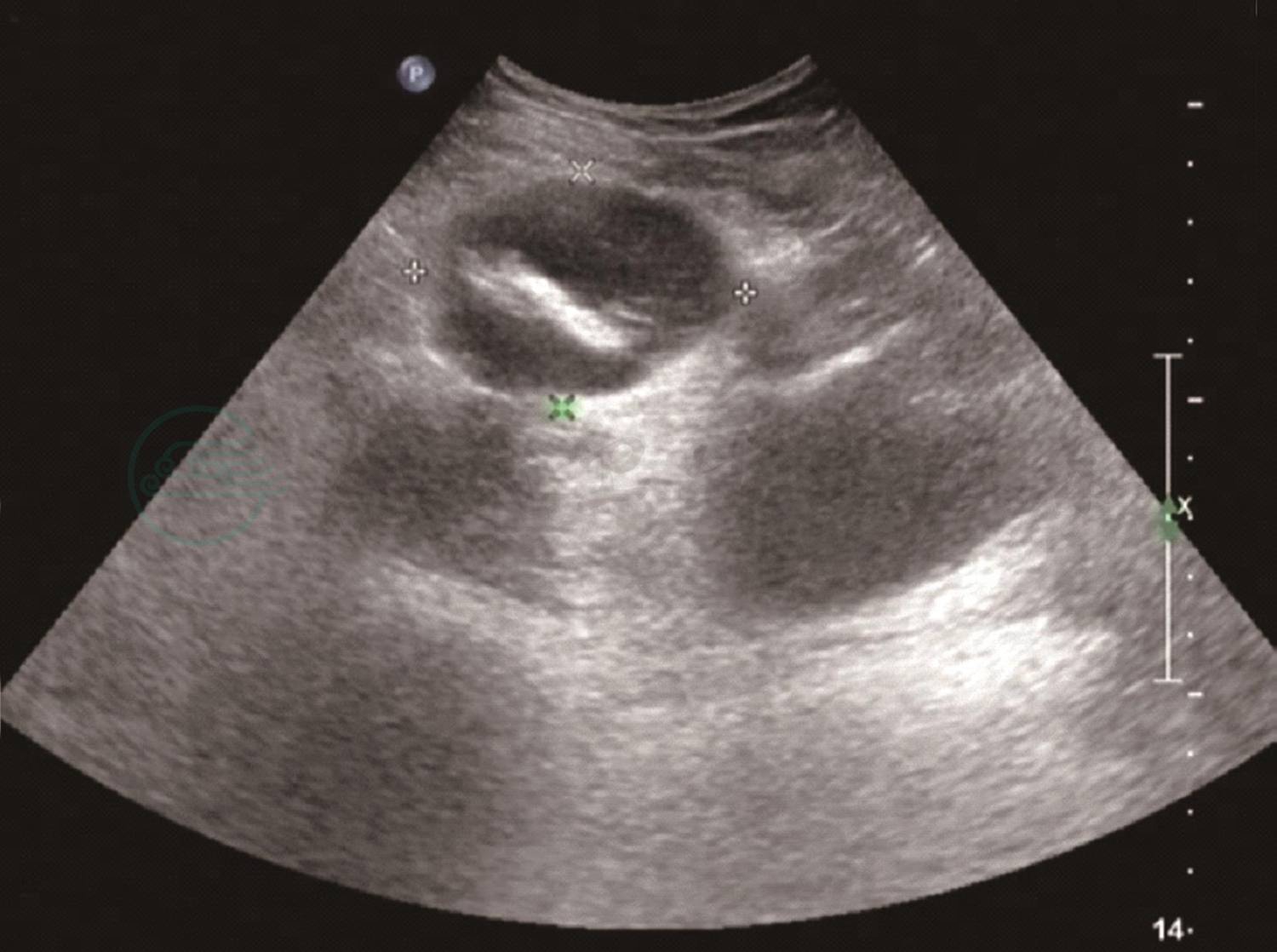
图3 外院腹部超声提示:右侧髂窝处5.9cm×4.5cm×3.9cm包块,考虑肿瘤占位
入院后给予心电、血氧监测。鼻导管吸氧2L/min下,经皮氧饱和度维持在TcSO2 93%~94%,夜间斜卧下无憋醒。患儿体力活动高度受限,缓慢步行约行走10m。考虑患儿为慢性间质性肺疾病,小剂量阿奇霉素200mg/d,每天1次,口服[5mg/(kg·d)];原有剂量甲泼尼龙8mg/d,晨起1次口服维持;布地奈德1mg联合复方异丙托溴铵2.5ml,每天3次雾化吸入;同时加强口腔、眼部护理。
入院后完善各项检查,化验结果如下:
1.动脉血气分析(鼻导管吸氧下2L/min) pH 7.41;PaCO2 52.6mmHg;PaO2 61.7mmHg;BE -6.9mmol/L,存在低氧及高碳酸血症。
2.血常规 白细胞9.8×109/L;中性粒细胞58.5%;淋巴细胞32.1%;嗜酸性粒细胞0.1%;血红蛋白142g/L;血小板379×109/L,正常。
3.免疫球蛋白(除IgA 0.655g/L↓)、淋巴细胞绝对计数正常,不支持免疫缺陷病。总IgE 10.76U/ml。
4.CRP 4.87mg/L;ASO<25U/ml,血沉20mm/h,血清补体无异常。抗核抗体弱阳性,抗核抗体系列阴性,ANCA阴性,α1抗胰蛋白酶正常,不支持SLE及ANCA相关的血管炎等免疫性疾病。
5.肝炎病毒无异常,血清呼吸道病毒系列、HIV+TPPA+RPR均阴性。
6.痰细菌培养(2次),呼吸道正常菌群生长;1,3-β-D葡聚糖<10pg/ml,GM试验阴性,不支持肺部细菌及霉菌感染。
7.肺炎支原体抗体1:1280,肺炎支原体抗体IgM阳性,考虑近期有肺炎支原体感染,入院第二天给予阿奇霉素400mg每天1次静脉滴注。
8.胸部增强CT(呼气位)(图4) ①双肺上叶前段炎症性病变;②双肺散在小片状磨玻璃密度影,渗出性病变?③双肺透亮度增高,双肺多发支气管扩张,弥漫性空气潴留征象;④弥漫性脂肪肝。
9.肺功能 肺通气功能降低(IVC实测值/预计值)为25%;FEV1实测值/预计值为16%;FEV1/FVC实测值/预计值为47%;PEF实测值/预计值为10%),支气管舒张试验阴性(改善率FEV1 13%;PEF 19%)。
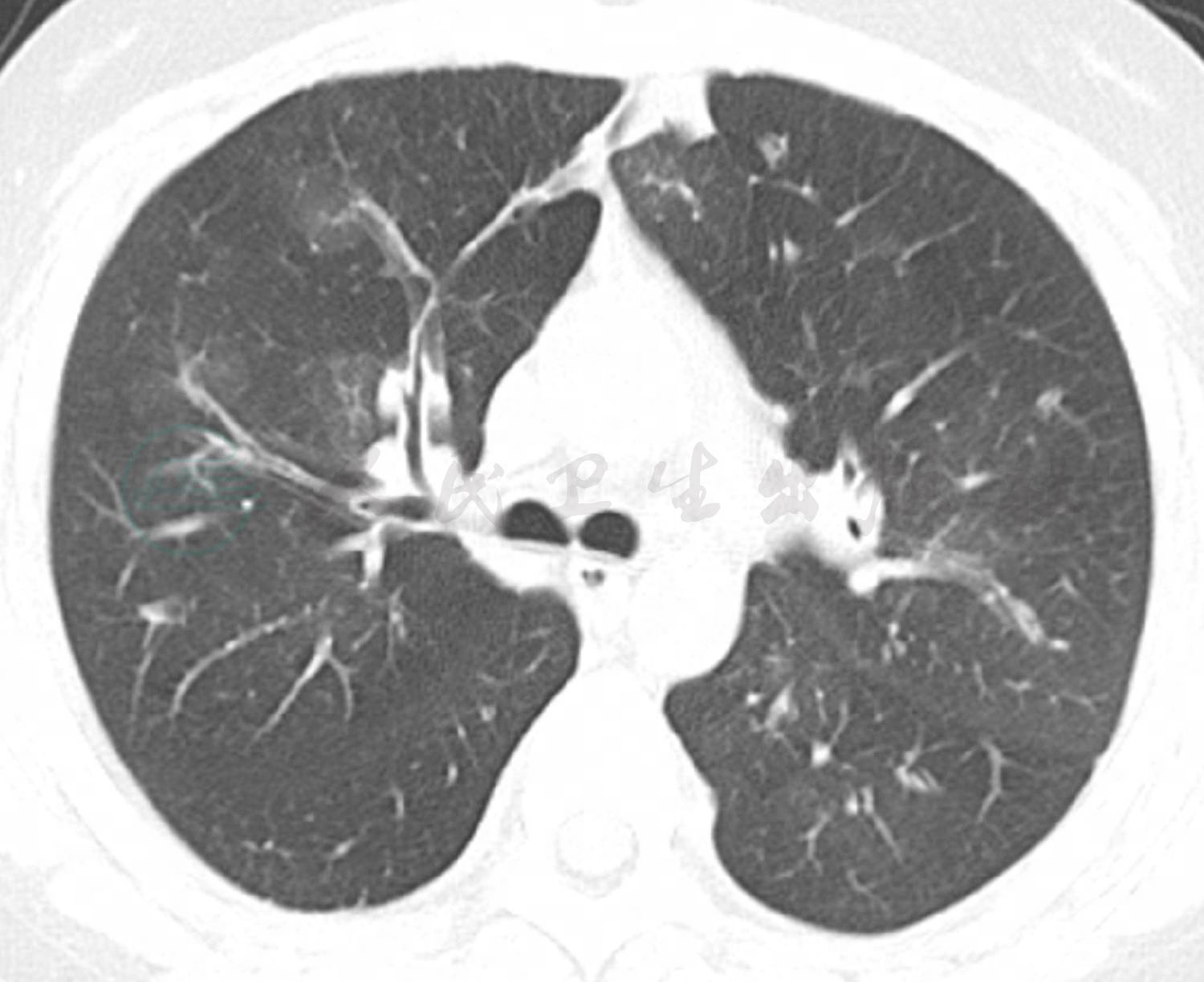
图4 入院后复查增强肺CT
10.肺弥散功能 阻塞为主混合性肺通气功能障碍,小气道功能重度减退,肺弥散功能中度减退(VC实测值/预计值为43.3%;FEV1实测值/预计值为17.6%;FEV1/FVC实测值/预计值为40.4%;MMEF75/25实测值/预计值为6.3%;TLCO实测值/预计值为46.6%)。
11.腹部超声(图5) 右下腹髂窝处实性肿物5.48cm×4.0cm×4.2cm。肿物内呈低回声,中央部伴条状强回声。CDFI可检出血流信号。
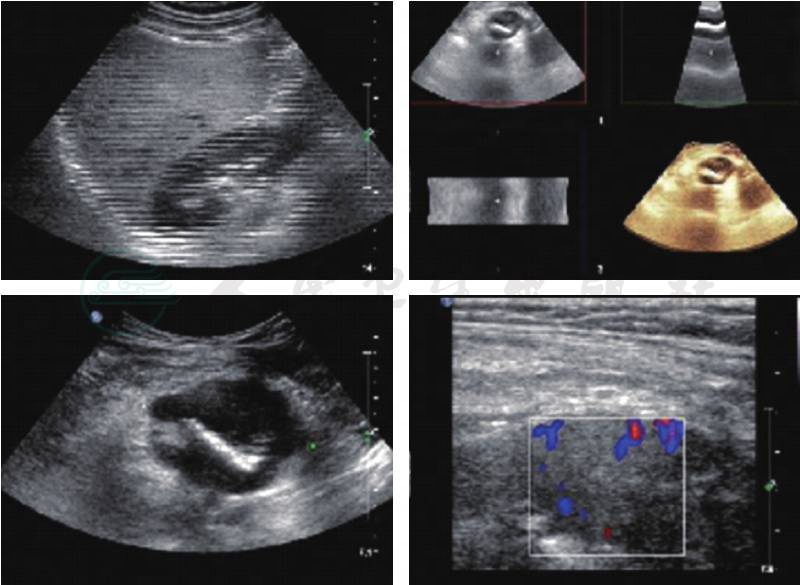
图5 腹部彩超提示:右下腹髂窝处实性肿物
12.窦性心动过速,心率130次/min。
入院第2天,血支原体1:1280,考虑有肺炎支原体的感染,加用静脉滴注阿奇霉素400mg/d连续5天静脉滴注;肺炎支原体主要是侵入支气管黏膜上皮,引起气道炎症性、可能加重气道损伤和狭窄;另外考虑到患儿可能为全身系统性免疫性疾病,患儿已用激素7个月余,但激素效果不佳,目前仍小剂量激素维持中,考虑到激素副作用,且患儿未曾用过丙种球蛋白,故加用大剂量静脉注射丙种球蛋白20g,每天1次,静脉滴注,连用3天(总量1.5g/kg)。应用3天丙种球蛋白后患儿自觉症状有所缓解,夜间可以平卧,但仍有呼吸困难;体力活动也有所改善,由原来平地步行不足10m,应用丙种球蛋白后可以步行约50m;左眼球结膜充血消失,口腔溃疡减轻。
通过肺部呼气相薄层CT、肺功能以及临床表现,初步确定肺部表现为BO。住院期间完善检查并请多科室会诊,并查阅国内外文献,排除白塞病、WG、SLE、Steven-Johnson综合征。因外院已做肿物及口腔活检,家属不同意再做相关有创检查,故未复查骨穿及口腔黏膜及肿物的活检。腹腔超声右下腹实性肿物;因患儿肺部病变过重,肺功能低下,不能耐受麻醉,因此采用姑息治疗。住院8天,考虑到患儿肺损伤已经形成,没有有效的治疗方法,目前没有感染表现,应用丙种球蛋白后症状较前略有缓解,患儿家属要求出院。
患儿出院后,试图以一元论解释患儿的呼吸困难、低氧、口腔溃疡、肿瘤一系列临床表现,经查阅大量文献,发现罕见病副肿瘤性天疱疮(paraneoplastic pemphigus,PNP)在患肿瘤的基础上可出现患儿所有症状,并且查阅到炎性肌纤维母细胞瘤导致PNP的相关文献。结合本例患儿的临床特点,我们高度怀疑本病为副肿瘤性天疱疮,遗憾患儿在院期间没能做PNP相关的大鼠膀胱为底物的间接免疫荧光检查及病理活检。
电话随诊:3年后,曾因感冒后呼吸困难加重、不能平卧住院治疗给予静脉滴注激素,抗生素治疗,呼吸困难好转,可以平卧即离院。这3年一直于家中低流量吸氧中,体力活动仍明显受限,仍有口唇发绀,只限于在自家屋院中散步。上次住院应用丙种球蛋白后口腔溃疡及结膜充血消失。在家中一直每天1次口服小剂量激素15mg。
5年后(患儿14岁)再次来院复查,停口服激素近2年,患儿体力活动耐受性较前明显提高,可慢走500~1000m,夜间无憋醒。但胸部CT较前仍气体潴留明显,支气管扩张(图6);肺功能较前无明显改善。查血天疱疮抗体阳性1:160。支持副肿瘤性天疱疮合并BO诊断。
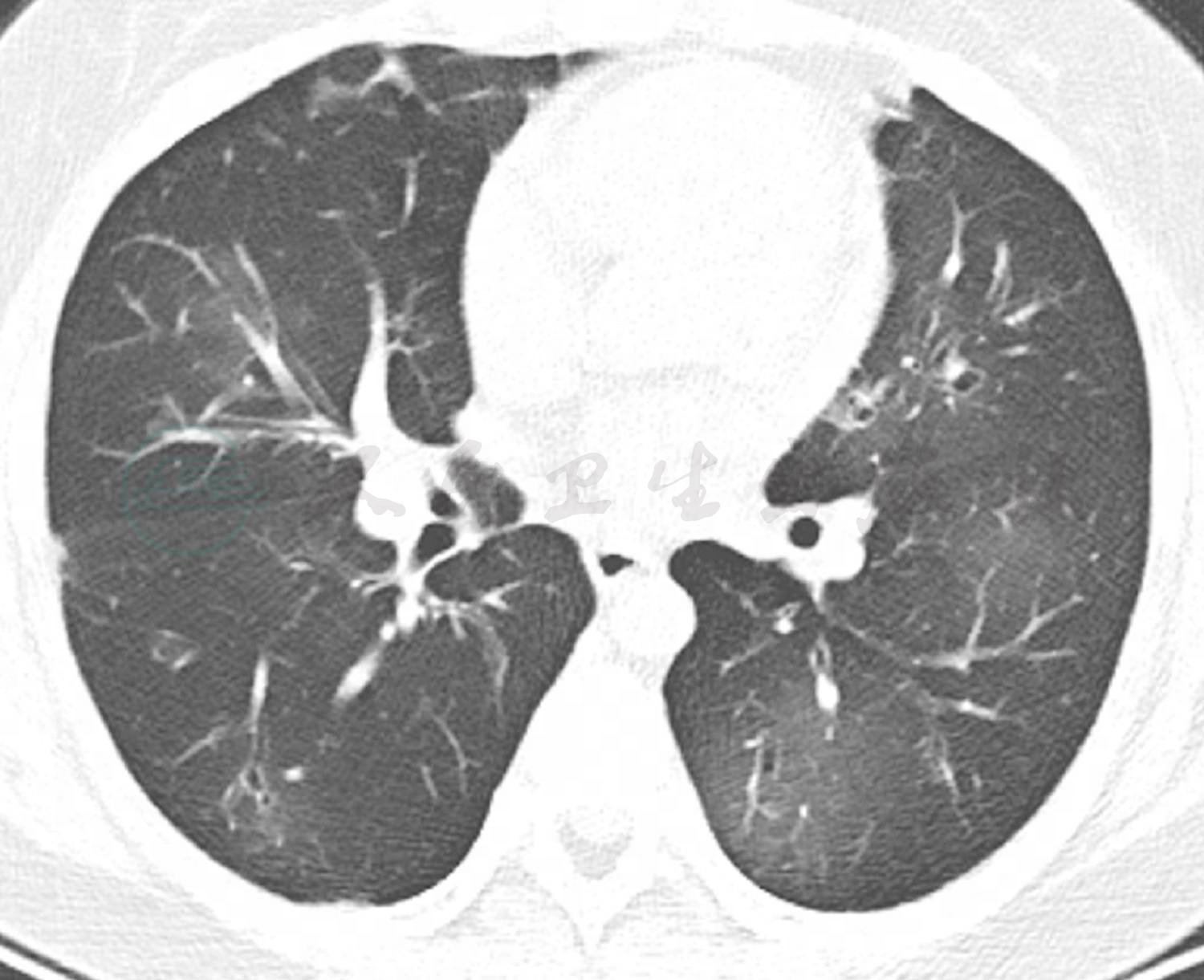
图6 出院5年后复查肺CT
1.副肿瘤性天疱疮
诊断依据:①疼痛性口腔溃疡8个月,结膜充血。②右下腹钝痛11个月,右侧中下腹可触及质硬的包块。腹部超声:右下腹实性肿物。外院腹部CT:右下腹盆腔内富血供实性占位;腹腔穿刺活检病理检查提示腹腔炎性肌纤维母细胞瘤。③合并闭塞性细支气管炎。表现为咳嗽8个月余,进行性呼吸困难、低氧7个月。查体:呼吸困难,口唇发绀,双肺呼吸音弱,肺底可闻及较密集细小水泡音,未闻及喘鸣音,呼吸相延长,肺功能以阻塞为主的混合型通气功能下降,呼气位肺CT示双肺大量气体潴留、马赛克征阳性,心影受压缩小、支气管壁增厚,支气管扩张。④血清天疱疮抗体阳性(1:160)。
2.炎性肌纤维母细胞瘤
诊断依据:①右侧腹痛6个月。②查体:右侧中下腹可触及质硬的包块。③超声示右下腹包块。穿刺活检病理回报:成肌纤维母细胞瘤。
3.Ⅱ型呼吸衰竭
诊断依据:明显的呼吸困难,口唇发绀、不吸氧经皮血氧饱和度84%,动脉血气PACO2 52.6mmHg。
4.肺炎支原体感染
诊断依据:MPAb 1:1280,MP-IgM阳性。
副肿瘤性天疱疮(paraneoplastic pemphigus,PNP)是一种与肿瘤伴发的自身免疫性皮肤黏膜疾病,于1990年由Anhalt等首先描述。除皮肤黏膜损伤外,PNP 可累及多个内脏器官。因此,近年来的研究多引用副肿瘤性自身免疫多器官综合征(paraneoplastic autoimmune multiorgan syndrome,PAMS)这一名词,以更好地概括该疾病的临床表现和免疫病理学特征的异质性。研究证实PNP是一种由体液免疫及细胞免疫共同参与的异源性自身免疫综合征,其发病机制尚不十分明确。一种学说提出PNP患者的肿瘤可以导致细胞因子失调,从而引发对经典天疱疮抗原(如DSG1或DSG3)的自身免疫反应,随后继发对棘层松解过程中所暴露的表皮细胞质内桥粒斑蛋白(plakin家族)的自身免疫反应。细胞因子分泌紊乱刺激B淋巴细胞分泌增殖及产生免疫球蛋白。
国外文献报道,PNP最常见的伴发肿瘤依次为非霍奇金淋巴瘤、慢性淋巴细胞白血病、Castleman病及胸腺瘤等。国内最常报道的伴发肿瘤为Castleman病。国内尚无PNP伴发炎性肌纤维母细胞瘤的报道。
本病好发于成年人。临床上多以疼痛性、进行性的口腔黏膜溃疡为首发症状。其他常见的黏膜损伤部位包括眼结膜、外阴、咽喉部,甚至胃肠道黏膜。口唇、眼结膜及外阴黏膜同时受累者约占50%;约80%患者出现皮肤损害,皮损呈多样性表现,有类似寻常型天疱疮的松弛性大疱和糜烂、类天疱疮样的张力性大疱、扁平苔藓或多形性红斑样的靶形皮肤损害。有近 90%的患者于初诊时被误诊为白塞病、扁平苔藓或重症多形红斑型药疹。皮肤组织病理示棘层松解,角质形成细胞坏死或液化变性及真皮浅层致密的以淋巴细胞为主的炎性细胞浸润;直接免疫荧光示IgG和/或C3在表皮细胞间和/或基底膜带沉积;血清内存在针对多种能够识别复层鳞状上皮、移行柱状上皮和单层上皮蛋白的自身抗体,因此,对疑诊患者,用患者血清倍比稀释做以大鼠膀胱为底物的间接免疫荧光检查;或检测血清包斑蛋白(envoplakin,分子量210kD)、周斑蛋白(periplakin,190kD)蛋白条带,可作为诊断PNP的特异性的筛选指标。
有报道约30%以上的PNP患者呼吸系统受累,主要表现为BO,并可逐渐发展为呼吸衰竭,这也是PNP患者的主要死因之一。其支气管活检提示存在呼吸道纤毛柱状上皮与基底细胞层剥离,黏膜下层炎症细胞浸润,进而堵塞细支气管腔。另外有研究发现PAMS的自身抗体可在支气管上皮沉积。病变主要发生在直径为0.4~0.9mm的终末支气管,受累支气管腔高度狭窄(>80%),呈限制性通气功能障碍,临床呈不可逆的进行性呼吸困难,药物治疗无效。即使肿瘤完整切除,术后虽皮肤黏膜症状好转,但BO仍持续存在。
诊断:目前采用的诊断标准是Camisa和Helm在1990年Anhalt等提出的诊断标准的基础上完善的,主要标准有:①多形性皮肤、黏膜损害;②内脏肿瘤;③典型血清免疫沉淀试验。次要标准有:①大鼠膀胱移行上皮为底物的间接免疫荧光试验(IIF)阳性表达;②损害周围组织直接免疫荧光法示IgG和补体C3沿表皮细胞间和基底膜带沉积;③至少有一个受累部位组织活检结果提示棘层松解改变。符合以上3条主要标准或2条主要标准者加2条次要标准者即可确诊PNP。本患儿没有组织病理学检查,但血清天疱疮抗体阳性(1:160),结合黏膜改变、内脏肿瘤,因而是确诊病例。
PNP/PAMS的治疗主要包括针对潜在肿瘤和皮肤黏膜病变的治疗。闭塞性细支气管炎是导致PNP患者死亡的主要原因之一,研究表明,手术完整切除肿瘤对患者的长期生存至关重要。围手术期给予丙种球蛋白阻断循环中自身抗体可显著降低严重闭塞性细支气管炎的发病风险。对于不可切除的肿瘤,针对原发病的治疗通常效果不佳,大剂量激素仍是最重要的治疗手段之一,其常与环孢素、硫唑嘌呤、环磷酰胺及氨甲蝶呤等免疫调节剂联合应用。因此,准确而及时的诊断、早期手术切除肿瘤,及时阻断肿瘤引起系列免疫性损伤为主的综合治疗手段是挽救患者生命的关键。
(陈 宁)













