近年来随着对乳腺癌生物学特性的深入研究,乳腺癌的治疗已经进入由局部到全身治疗并重的多学科综合治疗时代;同时外科治疗观念也发生了巨大变革,逐渐缩小手术范围以至保留乳房的局部切除,已经成为乳腺癌手术治疗的一种重要方式。大量的研究证实:对于早期乳腺癌进行保乳手术其远期生存率与改良根治术相同,是治疗乳腺癌的安全选择;同样有适应证的选择肿瘤较大的A、ⅡB、ⅢA期的临床患者,通过有针对性的个体化治疗—术前新辅助化疗(new adjuvant chemotherapy,NCT)—可使原发肿瘤缩小降期,从而增加了保乳机会,提高了治疗效果。
患者,女性,43岁,于2008年6月间无意中发现右乳腺肿物,逐渐增大,无疼痛,无局部皮肤溃烂,无乳头溢液,无畏寒发热,无胸闷腹痛等症状,遂来笔者单位就诊。
乳腺超声检查示(2008年6月3日):右乳外上象限近乳晕区皮肤增厚,结构紊乱,见条片状低回声结节,大小约5.2cm×3.2cm×4.0cm,右腋下见1.6cm低回声结节,内见淋巴门。(2009年6月4日)穿刺病理:浸润性导管癌Ⅱ级。术前分期(ⅢA期,T3N1M0)。
2009年6月11日起于笔者单位化疗科行3周期化疗,采用ET方案:表柔比星+紫杉醇(EPI+PTX),化疗剂量为表柔比星75mg/m2,紫杉醇175mg/m2,静脉点滴,每3周为1个周期。3周期后达到临床部分缓解,收入外科病房。
专科查体
双侧乳房对称,乳房皮肤无红肿及“橘皮样”改变,乳房浅表静脉无扩张,双侧乳头无凹陷,未见溢液。右乳外上象限可触及一肿物,大小约3.0cm×3.0cm,质硬,欠光滑,无压痛,边界欠清,活动度差,酒窝征(-),左侧乳腺未触及明显肿物,右侧腋窝触及一枚肿大淋巴结,大小约1.5cm×1.5cm,质硬,无压痛,活动度可。左侧腋窝及双侧锁骨上窝未触及肿大淋巴结。
辅助检查
超声:右乳外上象限近乳晕区皮肤增厚,结构紊乱,见条片状低回声结节,大小约5.2cm×3.2cm×4.0cm,右腋下见1.6cm 低回声结节,内见淋巴门。肝脏脂肪肝表现。
乳腺MRI:右乳外上象限不规则网片状影,散在分布,边界不清,时间-信号曲线呈“缓升”型,符合化疗基本消退后改变。右腋窝多发小淋巴结,性质待定(图1,图2)。
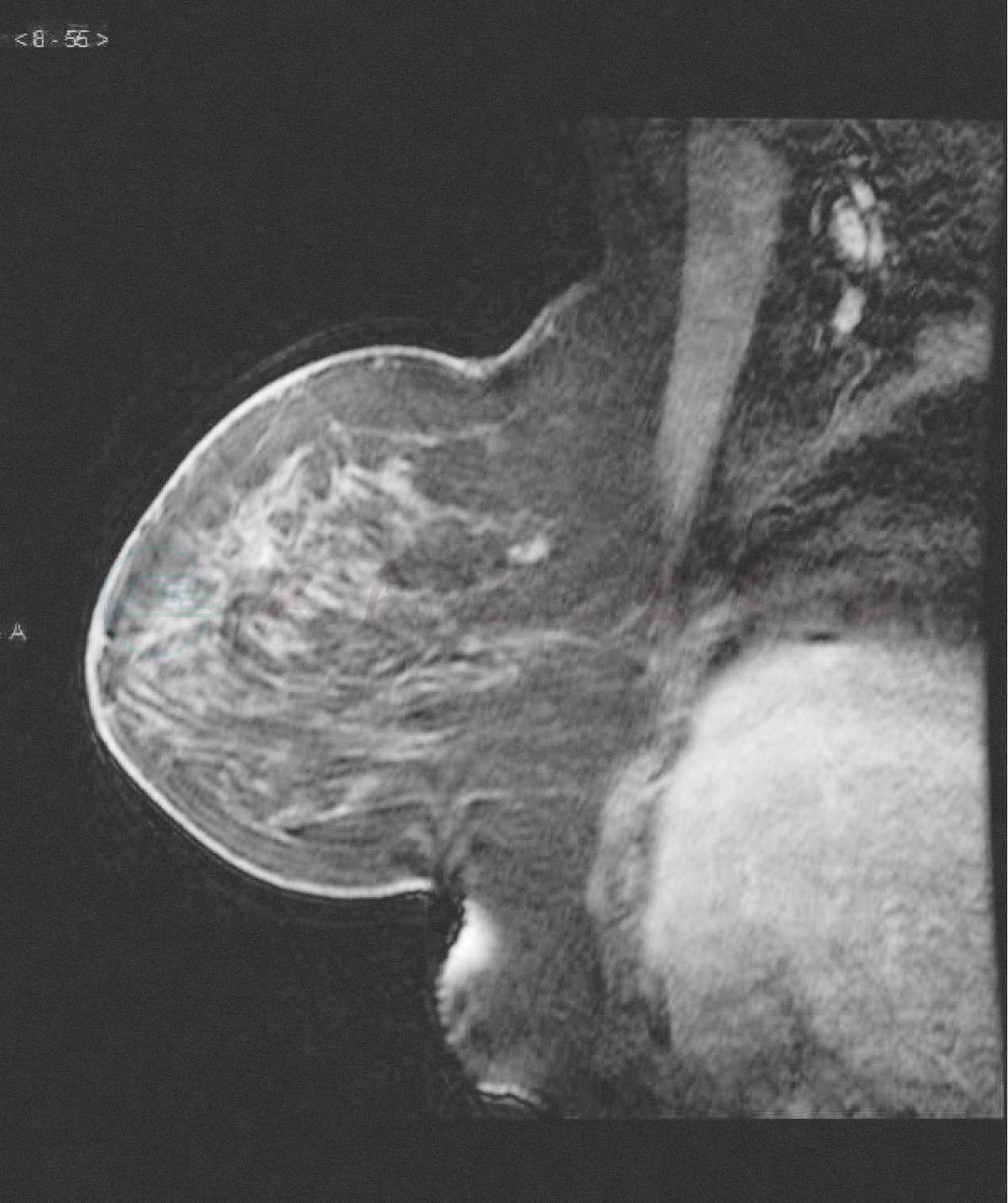
图1 右乳外上象限不规则网片状影
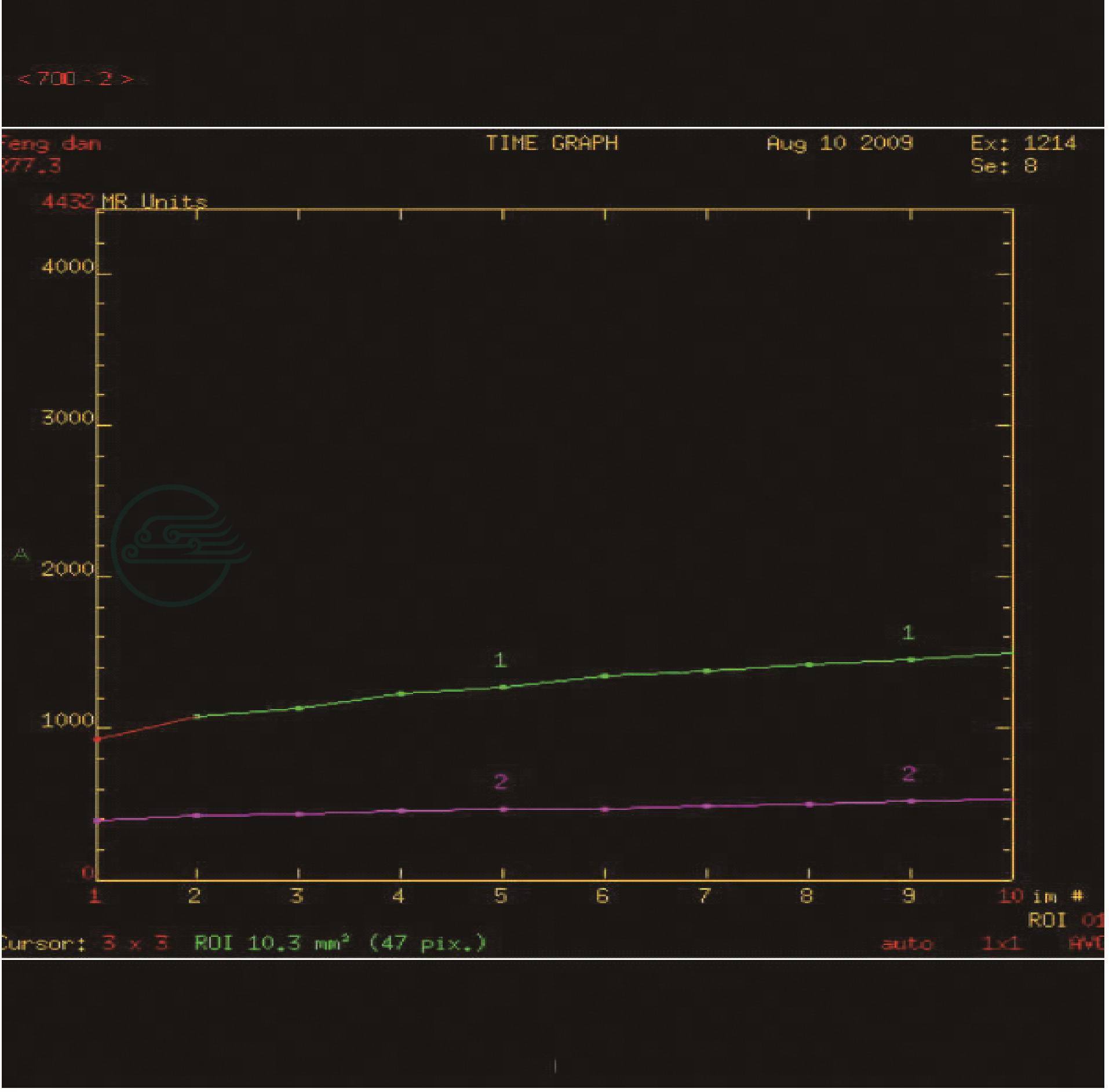
图2 时间-信号曲线呈“缓升”型
粗针穿刺病理:右乳浸润性导管癌Ⅱ级,ER(-),PR(-),C-erbB-2(+++)。
综合以上病史、查体及术前检查,术前诊断明确:右乳腺癌(ⅢA期,T3N1M0)新辅助化疗后。手术指征充分:本例乳腺癌化疗后缩小明显,达到临床部分缓解;患者腺体相对较大;且患者保乳要求强烈;术前检查无保乳的禁忌证;遂决定行右乳癌保乳术。
操作细节
患者取平卧位,气管内插管全麻成功后,右侧上肢外展,常规消毒铺巾。本例诊断明确按无瘤原则应先行腋窝淋巴结清扫,后行乳腺癌切除术。
1.切口选择
腋窝淋巴结清扫切口:取平行于右腋褶线的斜切口,长约5~6cm(切口前端不应超越胸大肌外侧缘,后端不超越背阔肌外侧缘,否则将影响美容效果)。
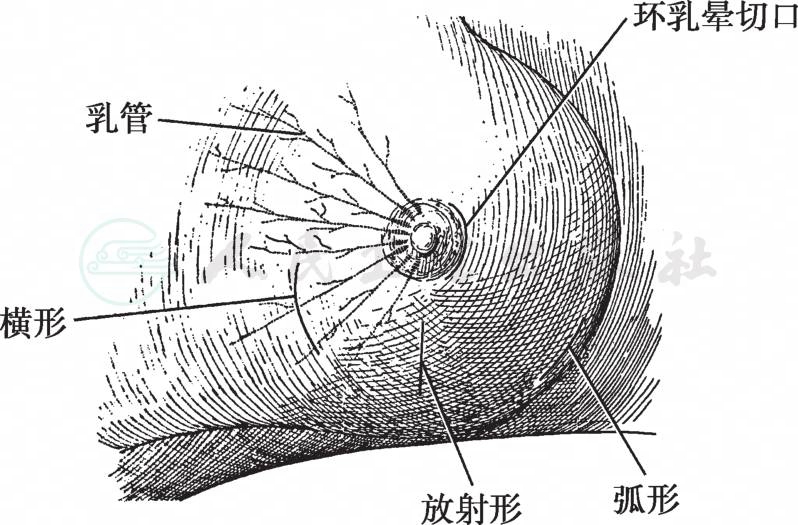
图3 乳腺癌切除切口
乳腺癌切除切口:切口的选择取决于病变的部位。肿瘤位于乳腺上象限者,选择与乳晕平行的弧形切口;肿瘤位于乳腺下象限者可选择以乳头为中心的放射状切口(但这类切口有可能因术后瘢痕挛缩造成乳腺外形改变),通常也可选择沿langer线的弧形切口(图3)。也有术者对于肿瘤位于外上象限者与腋窝淋巴结清扫采用同一个切口。我们的经验认为,除尾叶肿瘤或肿瘤极近腋窝外,一般外上象限肿瘤也应取两切口。因为有时勉强选同一切口,会增加腋窝清扫和肿瘤切除的难度;同时也有可能造成腋窝解剖不完全或增加肿瘤切缘不净的风险;再有因为腋窝和乳腺术区相连,为保证腋窝无积液而术后采取负压吸引和加压包扎,通常会造成乳腺外上区段的塌陷,导致美容效果差。本例患者肿瘤位于外上象限近内侧,因而另取肿瘤上方弧形切口。
2.切除范围及要点
(1)腋窝淋巴结清扫术:取右腋褶线的斜切口,常规游离皮瓣,厚度约0.5cm。向内至胸大肌外缘,向上至腋静脉水平,向外至背阔肌外缘,向下至第4、5肋间水平。打开喙锁筋膜,以电刀或组织剪打开腋静脉鞘,显露腋静脉,淋巴结清扫应至Berg腋淋巴结分级标准Ⅰ级(胸小肌外)、Ⅱ级(胸小肌深面)水平。助手以拉钩将胸大、小肌向上内侧牵起,可先清除胸小肌深面淋巴脂肪组织及腋静脉周围的淋巴脂肪组织,然后顺胸壁由上而下清扫。于胸小肌外侧缘后方与第二肋间隙交界处可见一直径约1.5~2mm粗细神经穿出肋间,走行与胸长神经相垂直,此神经即为肋间臂神经(图4)。若未发现腋窝淋巴结明显肿大融合、或与之有黏连、或者未钳夹、误扎时,则应尽量保留该神经。继续完成腋窝清扫术,沿胸壁向下,将标本向外牵拉,锐性分离前锯肌和侧胸壁脂肪层之间的间隙,注意保护胸背血管向前锯肌的分支及胸长神经的前锯肌分支,继续向下,在此间隙的外侧(脂肪内)显露胸长神经主干,将胸长神经主干释放回胸壁。继续沿背阔肌和肩胛下肌的表面间隙向外分离,直至显露出肩胛下血管主干,胸背神经与之伴行。此时腋窝重要血管神经已解剖完成。彻底清扫腋静脉下、肩胛下血管与胸长神经之间(内三角区)和肩胛下血管外侧区(外三角区)淋巴脂肪组织,外三角区内注意显露结扎副乳动脉(常易出血);整块切除腋窝淋巴脂肪组织下标本。确切止血,腋窝置硅胶管引流一枚,于切口下腋中线清扫区最低处(4、5肋间水平)另戳孔引出,接负压引流球。皮下可吸收线间断缝合,可吸收线皮内连续缝合皮肤。至此完成腋窝淋巴结清扫。
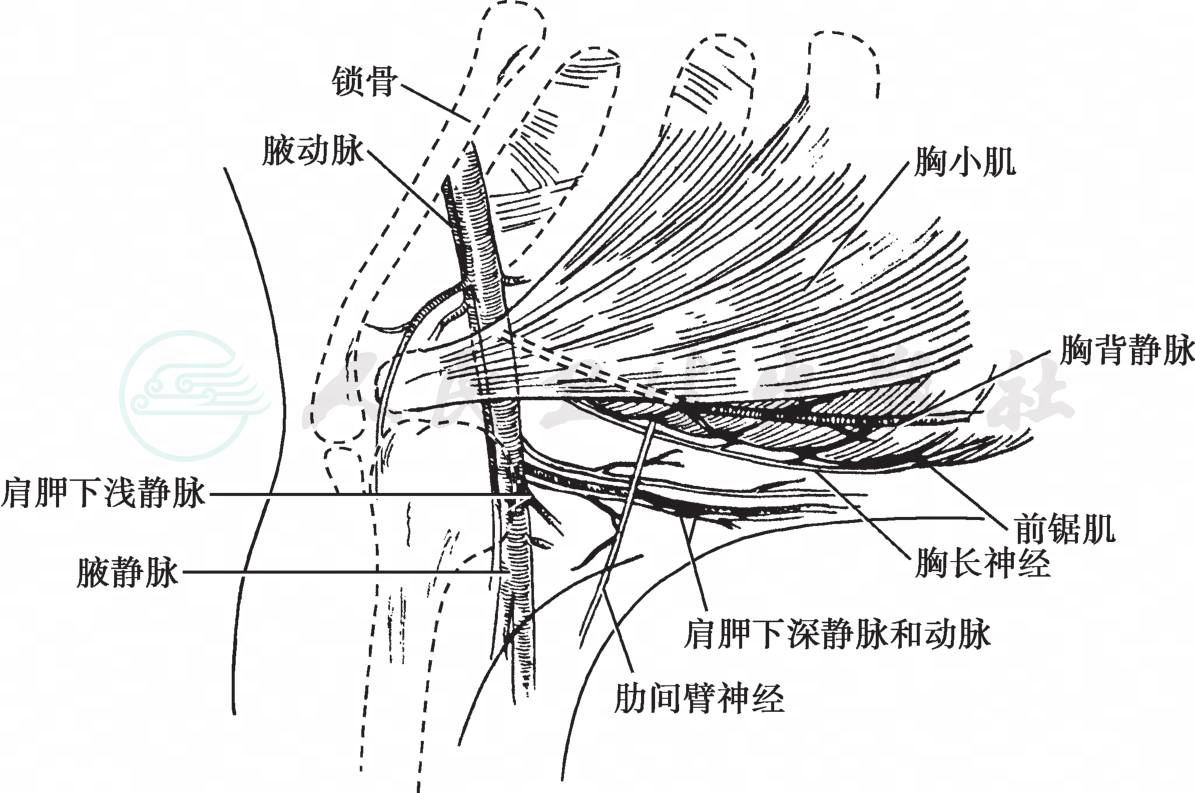
图4 腋窝解剖
(2)乳腺癌区段切除术:取右乳外上象限肿物上方弧形切口,长约6cm。游离皮瓣,厚度0.5cm,游离至肿物边缘外2cm,垂直向下环形切除肿瘤及周围2cm正常组织,包括肿块基底、胸肌筋膜。如肿瘤侵犯胸肌表面则切除部分胸大肌。切除肿瘤始终掌握切缘在同一平面,避免切成锥桶状。
切除标本离体前以缝线标记好上、下、左、右及基底5个切缘方向送冰冻病理检查。若任一切缘冰冻病理检查结果为阳性则该侧扩大切除1~2cm组织后,再送冰冻病理检查。原则上,一侧切缘补切2次仍阳性时,或腺体一次以上的补切(切缘阴性后)造成腺体残余量不足可能会导致外形严重改变时,则考虑放弃保乳治疗。本例首次5个切缘均阴性。遂于瘤床区上、下、左、右、基底5处放置金属标志物(如银夹或钛夹,避免使用顺磁性金属,导致术后无法行MRI检查),以利术后局部推量放疗。
残腔一般可不缝合,以免造成乳房扭曲变形。彻底止血后,可通过术后正常组织渗出液填充,逐步组织机化,恢复支持形态。但对于残腔过大影响外观者,可将周围腺体在皮下脂肪侧和基底侧切断Cooper韧带,分别游离,通过部分缝合腺体,来缩小残腔。以可吸收线间断缝合皮下组织。皮肤同样应以可吸收线皮内缝合,这种缝合方式可避免局部在组织张力大或愈合不良导致正常拆线后的切口裂开。对于残腔未缝合的,皮下缝合应确实、无漏针,以避免术后因残腔内渗出液压力增高时从切口渗液,腐蚀切口缝线,造成切口裂开或感染,导致美容效果不佳或失败。无菌敷料覆盖,不用加压包扎。
组织学检查结果及疗效观察
1.术后病理
大体检查:乳腺组织一块,富含脂肪,总大小8cm×5cm×5cm。切面见灰白、灰黄组织散在穿插分布。其中可触及质硬、偏韧区,界限不清,大小约2.3cm×1.5cm×1.5cm,呈灰粉灰白色,分布均匀,少部分颗粒状。
病理结果:右乳腺浸润性导管癌Ⅲ期,3周期化疗后。
右乳肿物:乳腺组织中仍可见分化差的浸润性导管癌残存,伴较多导管内癌成分,并可见脉管内瘤栓,癌细胞中度退变,间质纤维化,可见淋巴细胞和泡沫细胞反应,符合中度治疗后改变(Miller and Payno grading system,primary site,grade 3)。残存肿瘤大小2.3cm×1.5cm×1.5cm﹝残存浸润癌比例<60%﹞。上、下、内、外及基底切缘未见癌。
右腋窝清扫标本:淋巴结转移癌(1/15),治疗后改变。
免疫组化:ER(-),PR(-),C-erB-2(+++),p53(+++),Ki-67<5%(+)。
2.术后治疗
患者术后恢复好,术后5天腋窝日引流量小于20ml,拔除引流。术后7天解除腋窝的加压包扎。术后10天再次换药腋窝无积液。右乳切口愈合情况良好,乳腺外形无明显改变。
3.术后综合治疗措施及疗效观察
右乳腺癌(ⅢA期,T3N1M0)新辅助化疗后,术后3周,患者行TAC(多西他赛/多柔比星/环磷酰胺)方案继续化疗6个周期。化疗结束后进行全乳和锁骨上区放疗+瘤床推量放疗(全乳/锁骨上区50Gy/25f,瘤床推量10Gy/5f)。
术后随访:
患者生活质量好,患侧乳腺外形满意。未见复发和转移征象。













