患者,女,24岁,汉族人。主诉:妊娠32周,间断性腹痛、腹泻、大便带血半月余。
入院情况
患者于半月前进食果冻后出现间歇性腹痛、腹泻,大便为黄色糊样便,带少量鲜血,10余次/日,腹痛休息后可缓解,无寒战发热,无恶心、呕吐,无其他不适。当地诊所按“急性胃肠炎”给予输液治疗5天(具体药物不详),无明显好转,遂转入当地县医院,给予止泻,营养支持治疗8天,无好转。2012年6月14日突然出现腹痛,腹泻加重,20~30次/日,为鲜血便,伴发热,体温最高38℃,遂到我院急诊就诊,查血常规示:白细胞11.2×109/L,中性粒细胞76.4%;血小板396×109/L,血红蛋白69g/L。粪常规:潜血阳性,虫卵阴性,红细胞2~5/HP,白细胞30~45/HP。生化Na+、K+、Ca2+、Glu正常。给予抗炎、止泻等治疗,无好转,于6月15日以“便血待查”转入消化科。患者发病以来食欲食量、精神状态、体力情况均较差,体重下降10kg,小便无异常。患者既往体健,无肠道寄生虫病史,无食物及药物过敏史。家族史及个人史:孕2产0流1,月经: 14(7~8)/(28~30) 2011-11-1。入院查体: T 36.8℃,P 70次/分,R 18次/分,BP 120/70 mmHg。一般状况良好,贫血貌,全身皮肤无黄染,未见皮疹及出血点,无肝掌、蜘蛛痣。巩膜无黄染,心肺无异常。腹膨隆,妊娠32周,腹部柔软,上腹部轻压痛,无明显压痛、反跳痛,腹部无包块。肝脾肋下未触及,Murphy征阴性,肾区无叩击痛,移动性浊音阴性。肠鸣音活跃,8次/分。双下肢轻度水肿。入院后化验肝肾功能:总胆红素12μmol/L,结合胆红素2.1μmol/L,白蛋白18.8g/L,丙氨酸转氨酶8U/L,碱性磷酸酶87U/L,天冬氨酸转氨酶14U/L,肌酐39μmol/L,尿素氮1.6mmol/L。C反应蛋白60.4mg/L。尿常规正常。粪常规:潜血阳性,WBC>50/HP,RBC满视野。痢疾阿米巴滋养体、痢疾阿米巴包囊、结肠阿米巴滋养体、鞭毛虫、钩虫、蛲虫、肺吸虫、虫卵阴性。
初步诊断
①便血原因待查
慢性结肠炎,细菌性痢疾,感染性腹泻,炎症性肠病
②晚期妊娠
鉴别诊断
该患者腹泻原因需要排除以下几种病
①急性胃肠炎
主要临床表现为恶心、呕吐、腹痛、腹泻、发热等,严重的还会引起呕血、便血等症状。起病急,有暴饮暴食或吃不洁腐败变质食物史。粪便检查可分离出致病菌,抗生素治疗有效,通常在4周内消散。
②肠阿米巴病
由阿米巴原虫寄居于结肠内引起的疾病。起病较缓,腹痛、腹泻,粪便暗红色或紫红色果酱样,有腥臭。主要侵袭右结肠,也可累及左侧结肠,结肠溃疡较深,边缘潜行,溃疡间黏膜多正常。粪便检查发现有阿米巴包囊呈小滋养体或大滋养体。而患者曾行痢疾阿米巴滋养体、痢疾阿米巴包囊、结肠阿米巴滋养体检查,均为阴性,可基本排除此病。
③炎症性肠病
是一种病因不明的慢性非特异性肠道炎症性疾病,主要包括溃疡性结肠炎(UC)和克罗恩病(CD)。临床上前者为结肠性腹泻,常呈血性,口炎与腹部包块少见;后者腹泻表现不定,常有腹痛和营养障碍,口炎、腹部包块和肛门病变常见。内镜和影像学检查,前者为直肠受累、弥漫性、浅表性结肠炎症;后者以回肠或右半结肠多见,病变呈节段性、穿壁性、非对称性,典型者可见鹅卵石样改变、纵行溃疡和裂沟等。组织学上,前者为弥漫性黏膜或黏膜下炎症,伴浅层糜烂溃疡;后者为黏膜下肉芽肿性炎症,呈节段性分布或灶性隐窝结构改变,近段结肠偏重等特征。
如若患者条件允许,可行肠镜检查明确诊断。
患者入院当晚出现不规律宫缩,阴道流液,经本院产科会诊,考虑胎膜早破,先兆早产。转入产科治疗,患者经保胎治疗后,胎动、胎心恢复正常,无继续阴道流液现象,但仍持续大便带血,15次/日,伴间断发热,体温最高40℃。产科建议患者剖宫手术治疗后肠镜检查明确。患者家属拒绝,要求继续内科查明病因。强烈要求先行肠镜检查。向患者家属讲明晚期妊娠为内镜检查的禁忌,可能诱发早产。患者仍强烈要求,并签署知情同意书,于6月18日行直肠镜检查(见图1),见:进镜达距肛门15cm,所见肠黏膜弥漫性充血水肿,血管纹理消失,散在点状糜烂及大小不等不规则深凹陷溃烂,表面附白苔,内镜触碰黏膜易出血。病理示:直肠溃疡,肉芽组织增生伴急慢性炎细胞浸润,周围黏膜急慢性炎。考虑:炎症性肠病(溃疡性结肠炎可能性大)。
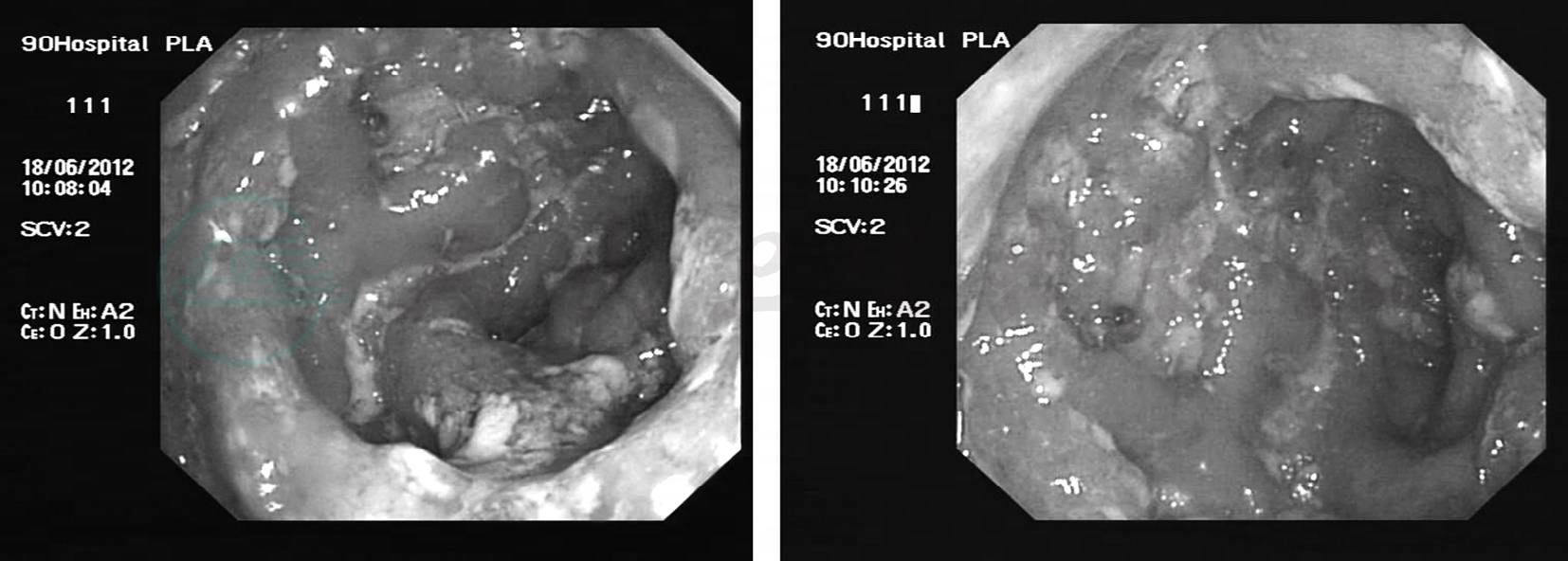
图1 肠镜下的表现
患者及家属拒绝外科治疗,于6月19日再次转入消化科。向患者家属讲明药物可能对胎儿的影响。患者要求积极药物治疗,承担一切不良后果。遂给予美沙拉秦颗粒1g口服4次/日,固本益肠片2.4g,口服,3次/日,口服酪酸梭菌活菌胶囊1260mg,口服,2次/日、复方谷氨酰胺肠溶胶囊0.4g,口服,3次/日,抗炎、保护肠道黏膜、调节肠道菌群、促肠黏膜修复治疗,并给予营养支持治疗。进一步化验检查排除伤寒、霍乱、菌痢、结核、肠阿米巴等传染性疾病。先后行3次大便培养、血培养,未查见致病细菌、霍乱弧菌、病毒、真菌,结核抗体,PPD试验阴性,肥达试验、外斐反应、嗜异性凝集试验、冷凝集试验均阴性,风湿免疫指标抗O、类风湿因子、ANA、CCP、dsANA、AMA-M2、sp100、LKM-1、gp210、LC-1、SLA均正常,抗RA33抗体阳性(61.4Au/ml,参考值阳性:>30)。结合内镜及病理结果,诊断:溃疡性结肠炎(急性暴发型,重度)。后组织普外科、产科、肾内科、感染科、药理科、心内科及消化科全院会诊,建议给予激素冲击治疗。于6月22日起给予0.9%氯化钠注射液100ml+氢化可的松注射液100mg,静滴,2次/日激素治疗,加用0.9%氯化钠注射液250ml+复方丹参注射液30ml改善微循环。患者体温降至正常,大便次数减少,脓血减少,于6月26日将激素调整为泼尼松片,口服,30mg/早,20mg/晚,6月30日起,患者开始出现黄色稀便。但患者大便次数仍较多,粪质少。考虑直肠病变及晚期妊娠胎儿压迫所致肛门刺激征明显。加用0.9%氯化钠注射液100ml+云南白药胶囊2粒+康复新液20ml+复方黄柏液10ml+美沙拉秦缓释颗粒保留灌肠1/晚。患者自7月7日起开始解墨绿色稀便。7月6日复查肝肾+生化示:总胆红素10μmol/L,结合胆红素2.8μmol/L,白蛋白28.9g/L,丙氨酸转氨酶22U/L,碱性磷酸酶126U/L,天冬氨酸转氨酶23U/L,肌酐39μmol/L,尿素氮0.8mmol/L。复查大便常规示:粪常规:潜血阳性,WBC 30~35/HP,RBC10~15/HP。痢疾阿米巴滋养体、痢疾阿米巴包囊、结肠阿米巴滋养体、鞭毛虫、钩虫、蛲虫、肺吸虫、虫卵阴性。于7月7日复查直肠镜(见图2)示:进镜达距肛门30cm,所见乙状结肠弥漫性充血水肿溃烂,附白苔,表面见结节状增生,局部见假息肉形成,直肠黏膜弥漫性充血水肿,黏膜质脆易出血,原凹陷溃烂较前明显好转。
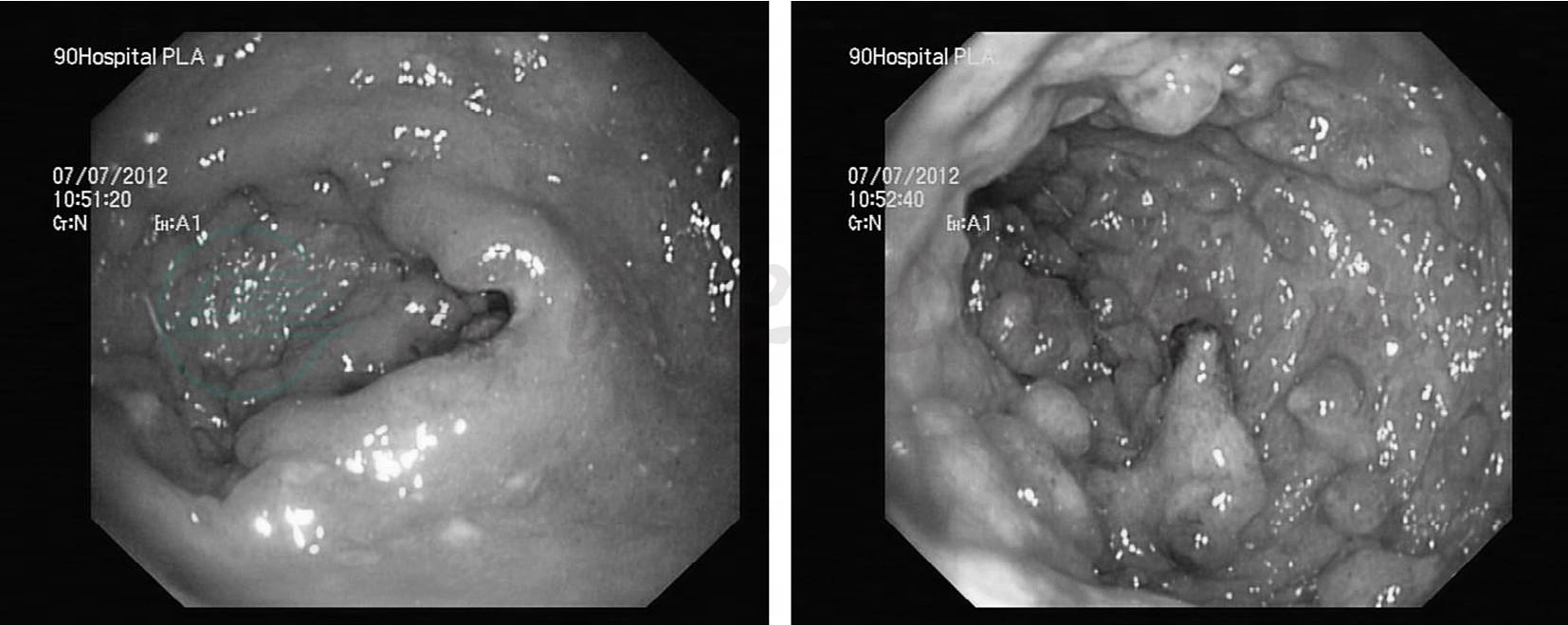
图2 肠镜下的表现
7月12日复查血常规示:白细胞6.06×109/L,中性粒细胞占78.7%;血小板282×109/L,红细胞: 2.79×1012/L,血红蛋白74g/L。
患者7月13日晚突然出现规律宫缩,RHR155~170次/分,阴道流血,查体:宫口开放5~6cm,先露头“0+1”。遂转入产科生产。于晚20:45自娩一男婴,1分钟Apgar评分10分,体重2450g。患者产后第2天(7月14日)出现发热,体温最高39℃,伴全腹部疼痛,恶心、呕吐,急查血常规示:白细胞29.12×109/L,中性粒细胞90.2%;血小板166×109/L血红蛋白82g/L。查体:BP 96~85/55~70mmHg,P 150~180次/分。全腹压痛,无反跳痛,子宫缩复好,量少。肠鸣音弱,遂行腹部立位平片示:消化道穿孔。遂急诊外科手术探查:见腹腔盆腔大量粪液及肠液流出,全程结肠浆膜面充血水肿,活力尚可,盲肠前壁见0.5cm破口,旁见3cm破口,局部不规则,血运差,遂常规行“剖腹探查+回盲部切除+回肠/结肠造口术”择期行Ⅱ期手术。病理示:结肠溃疡、破裂、出血,溃疡深及浅肌层,肠壁全层急慢性炎伴间质水肿,符合溃疡性结肠炎并破裂改变。患者术后继续给予抗炎、补液、纠正白蛋白及抗炎、促进肠黏膜修复及营养支持治疗。患者脓血便较前重,且出现腹部切口哆裂,遂于7月26日再次复查肠镜(见图3)示:进镜达降结肠,因肠黏膜充血水肿溃烂,管腔狭窄变形,无法继续进镜。退镜所见降结肠、乙状结肠、直肠(距齿状线4cm以上)弥漫性充血水肿溃烂,管腔狭窄,见结节状增生及大量坏死组织,黏膜广泛发蓝,呈缺血样外观。距齿状线4cm以下直肠黏膜弥漫性充血水肿,表面覆大量血迹,未见明显溃烂。
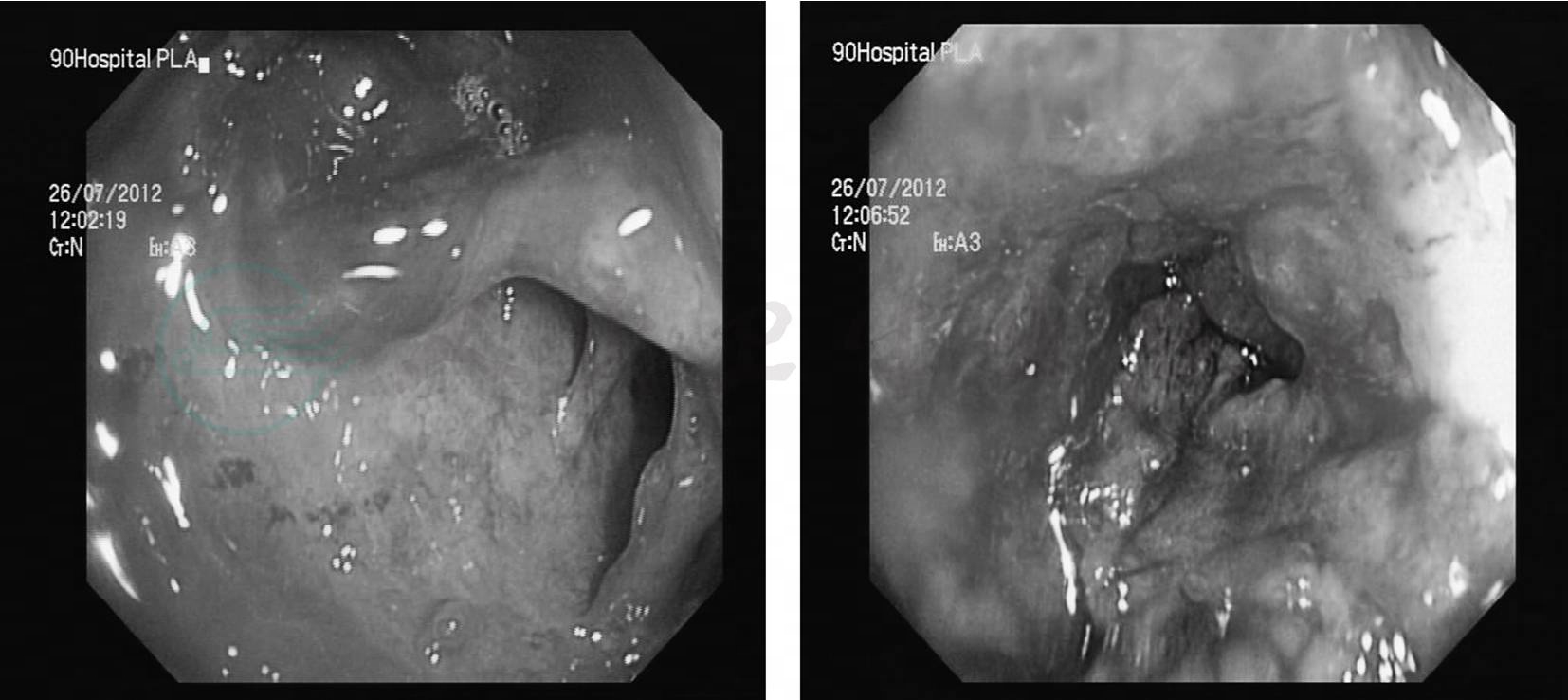
图3 肠镜下的表现
建议患者行全结肠切除术及肛门再造术,患者家属因患者年轻拒绝,要求保留肛门。经全院会诊后,于7月30日行“全麻全结肠结肠(保留直肠、肛管)+腹壁切口全层减张缝合术”。术后病理示:结肠黏膜急慢性炎伴多灶溃疡形成,肉芽组织增生,溃疡深达浅肌层,周围黏膜呈多灶性炎性息肉改变。
术后出现直肠残端瘘,经抗感染、外科换药、清创引流、静脉营养支持及局部应用美沙拉秦栓剂后腹壁切口愈合,大便正常,于2012年8月25日出院。出院后一直电话随访至今,大便一直正常。男婴生长良好,8月龄时体重13kg,身高、智力发育同同龄幼儿。建议患者复查肠镜,患者至今未至。
最终诊断
妊娠晚期急性暴发型溃疡性结肠炎(重度)。
文献复习
溃疡性结肠炎(UC)是一种病因尚不十分清楚的慢性非特异性的炎症性肠病。我国尚缺乏普通人群的流行病学统计资料,但近十年本病的就诊人数呈逐步增加趋势。UC已成为我国的常见消化道疾病。欧美及我国先后多次对该病的诊治指南进行修订。但对儿童及围妊娠期患者的处理,缺乏足够的认识和经验。
UC缺乏诊断的金标准,主要结合临床表现、内镜和病理组织学进行综合分析,并在排除感染性和其他非感染性结肠炎的基础上作出诊断。①临床表现:UC常发生于青壮年,临床表现为持续或者反复发作的腹泻、黏液脓血便伴腹痛、里急后重和不同程度的全身症状,病史多在4~6周以上。可有皮肤、黏膜、关节、眼和肝胆等肠外表现。②结肠镜检查并活检:是UC的主要诊断依据,病变多从直肠开始,呈连续性、弥漫性分布,表现为:黏膜血管纹理模糊、紊乱或消失,黏膜充血水肿质脆,自发性出血及接触性出血和脓性分泌物附着,亦常见黏膜粗糙,呈细颗粒样改变,病变明显处见弥漫性、多灶性糜烂或溃疡,可见结肠袋变浅,变钝以及假性肉、黏膜桥等。③组织学表现:固有层内弥漫性急慢性炎性细胞浸润、隐窝结构改变、黏膜表面溃烂、浅溃疡形成及肉芽组织增生。
对于轻症UC患者的治疗,氨基水杨酸类制剂是基础药物,常用的有柳氮磺胺吡啶片、巴柳氮、奥沙拉嗪钠、美沙拉秦等制剂,没有证据显示不同类型的5-ASA制剂疗效上的差别,对于治疗无效且病变广泛者,考虑口服激素治疗。中度UC:氨基水杨酸类制剂仍是主要药物,足量5-ASA治疗(2~4周)无效或控制不佳者,应考虑应用激素,按泼尼松0.75~1mg/(kg·d)给药,症状缓解后逐渐减量及停药。对于激素无效及依赖患者,加用硫嘌呤类药物,包括:硫唑嘌呤(AZA)及6-硫基嘌呤(6-MP),一般AZA剂量为1.5~2.5mg/(kg·d)。对于激素及免疫抑制剂治疗无效或激素依赖或不能耐受上述药物时,可考虑英夫利昔或阿达木单抗生物治疗。重度UC病情重,发展快,处理不当会危及生命。应给予积极补液、营养支持治疗,避免水电解质紊乱及酸碱平衡失调,病情严重应暂禁食,予胃肠外营养,排除肠道细菌感染,检查是否合并艰难梭菌及CMV感染,中毒症状者可考虑静脉应用广谱抗生素。首选静脉用激素治疗,甲泼尼龙40~60mg/d或氢化可的松300~400mg/d。静脉足量应用激素治疗5~7天无效进行转换治疗,一种是立即外科手术治疗;一种是药物“拯救”治疗,环孢素(CsA) 2~4mg/(kg·d)静脉滴注,4~7天,有效者,待症状缓解后改为口服(6个月以内),无效者行手术治疗。国外曾报道英夫利昔单抗作为“挽救治疗”方案有一定疗效。
妊娠合并急性暴发型溃疡性结肠炎临床少见,但病情极其凶险,严重威胁母婴安全。
虽然,国外有回顾性研究表明,妊娠合并UC的孕妇产褥期并发症发生率同正常人群。UC患者同正常妇女有相同的生育能力,怀孕不增加UC的复发率,但UC活动期可增加习惯性流产的风险。有研究表明,UC女性患者怀孕生产的后代中,没有发现低体重出生儿的风险增加,或胎儿宫内发育迟缓的迹象。但妊娠期初发UC住院患者,早产风险增加。妊娠溃疡性结肠炎病情缓解后,由于分娩这一应激因素,病情可以复发,甚至暴发。
所以,应高度重视此类患者的诊治,确保母婴安全。妊娠合并溃疡性结肠炎的治疗不同于一般溃疡性结肠炎患者。目前对于妊娠期UC的用药存在争议。根据美国食品和药品管理局(FDA)药物安全的分级标准,理论上对于妊娠合并重度溃疡性结肠炎,比较合适的治疗是5-ASA加皮质类固醇。临床应用最多的皮质类固醇是泼尼松和甲泼尼龙。这些药物虽然可以少量透过胎盘屏障,但在胎儿体内迅速代谢降解,因此,对胎儿的影响很小。
有学者报告低剂量巯基嘌呤(25mg/d)联合别嘌呤醇(100mg/d)+美沙拉秦颗粒4g/d治疗妊娠合并妊娠患者效果良好,并且不增加妊娠相关并发症发生。但也有学者报道别嘌呤醇存在潜在的致畸作用,而其他学者的对孕妇新生儿的研究却没有发现别嘌呤醇的类似不良反应。
有学者曾报道英夫利昔单抗(IFX)用于治疗妊娠女性溃疡性结肠炎是有效的,对母婴均是安全的。但近期的1篇个案报道却证实IFX可以通过胎盘屏障进入胎儿,在生后26周内的胎儿体内,可以检测到治疗剂量的IFX,直至产后28周才消失。因此,IFX对妊娠期母婴的安全性需要进一步的临床验证。
虽然妊娠不是溃疡性结肠炎手术的绝对禁忌证,但有报道,妊娠期间手术可以增加母婴的病死率,因此,对于UC患者,尽量推迟外科手术时间是非常必要的。
该患者确诊为急性暴发型溃疡性结肠炎后,给予激素治疗早期是有效果的,但分娩这一应激因素使原病情加重,因肠道溃疡较深,分娩过程中腹压过高导致肠壁穿孔是该患者最终难免手术的原因。
妊娠合并溃疡性结肠炎的病例国内报道较少,治疗尚缺乏相关经验,应该在国外相关报道基础上总结我们的经验,通过前瞻性研究,探索用药的安全性和规范性,减少孕产妇及新生儿并发症的发生,制定规范化的妊娠期溃疡性结肠炎的诊疗规范,为更多类似患者服务。













